Диффузионное горение газа. Структура диффузионного пламени.
Диффузионное горение газов – сложный процесс, характеризующийся взаимодействием химических реакций с процессами переноса и конвекцией.
Факел, который образуется при истечении топлива в среду окислителя (или окислителя в среду топлива, горючего). Его называют - диффузионным факелом - (диффузионное горение, диффузионное пламя). Для этого типа главную роль играет явление диффузии, смешения (молекулярной, турбулентной).
При диффузионном режиме горения tпреобр определяется гидродинамикой геометрической области преобразования, т.е. определяется интенсивностью процесса смешения, а также родом горючего и окислителя.
tсмеш >> tхим.р.:диффузионный режим горения (tпреобр≈tсмеш)
Диффузионное горение имеет место в условиях, когда горючее и окислитель диффундируют в зону р-ции с противоположных сторон; таково, напр., Г. свечи, фитиля. Если при этом константа скорости k р-ции Г. много меньше константы скорости диффузии 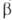 реагенты успевают перемещаться и р-ция протекает в обычном кинетич. режиме (относительно низкотемпературном). При
реагенты успевают перемещаться и р-ция протекает в обычном кинетич. режиме (относительно низкотемпературном). При  реагенты взаимод. тотчас же после их поступления в зону р-ции, прежде чем они полностью перемешаются, и р-ция протекает в режиме Г., т.е. при высоких т-рах. Отношение диффузионных потоков реагентов определяется стехиометрией р-ции; концентрации горючего и окислителя в зоне р-ции малы, осн. компонент смеси-продукты сгорания, к-рые диффундируют в области, занятые горючим и окислителем (рис. 4). Выделяющееся при р-ции тепло передается горючему и окислителю, к-рые поступают в зону р-ции нагретыми до высокой т-ры. В отличие от Г. перемешанных смесей, т-ра диффузионного Г. зависит от отношения
реагенты взаимод. тотчас же после их поступления в зону р-ции, прежде чем они полностью перемешаются, и р-ция протекает в режиме Г., т.е. при высоких т-рах. Отношение диффузионных потоков реагентов определяется стехиометрией р-ции; концентрации горючего и окислителя в зоне р-ции малы, осн. компонент смеси-продукты сгорания, к-рые диффундируют в области, занятые горючим и окислителем (рис. 4). Выделяющееся при р-ции тепло передается горючему и окислителю, к-рые поступают в зону р-ции нагретыми до высокой т-ры. В отличие от Г. перемешанных смесей, т-ра диффузионного Г. зависит от отношения 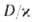 . При
. При  она совпадает с т-рой Г. перемешанной стехиометрич. смеси горючего и окислителя, с уменьшением -падает. По этой причине диффузионное Г. не реализуется в конденсиров. средах, для к-рых значенияочень малы; помимо газофазных систем, диффузионное Г. характерно для гетерог. р-ций на пов-сти (Г. твердых в-в, гетерог.-каталитич. Г.). Массовая скорость m диффузионного Г. определяется скоростью диффузии реагентов в зону р-ции. Рост m с увеличением скорости диффузии возможен лишь до определенного предела. Это предельное значение m близко по величине к массовой скорости Г. в пламени, распространяющемся по стехиометрич. смеси горючего и окислителя. По достижении предельного значения m p-ция переходит в низкотемпературный кинетич. режим (происходит срыв Г.). От начальной т-ры реагентов Т0 m практически не зависит, однако при нек-ром минимальном для данного набора остальных параметров значении Г0 диффузионное Г. невозможно.
она совпадает с т-рой Г. перемешанной стехиометрич. смеси горючего и окислителя, с уменьшением -падает. По этой причине диффузионное Г. не реализуется в конденсиров. средах, для к-рых значенияочень малы; помимо газофазных систем, диффузионное Г. характерно для гетерог. р-ций на пов-сти (Г. твердых в-в, гетерог.-каталитич. Г.). Массовая скорость m диффузионного Г. определяется скоростью диффузии реагентов в зону р-ции. Рост m с увеличением скорости диффузии возможен лишь до определенного предела. Это предельное значение m близко по величине к массовой скорости Г. в пламени, распространяющемся по стехиометрич. смеси горючего и окислителя. По достижении предельного значения m p-ция переходит в низкотемпературный кинетич. режим (происходит срыв Г.). От начальной т-ры реагентов Т0 m практически не зависит, однако при нек-ром минимальном для данного набора остальных параметров значении Г0 диффузионное Г. невозможно.
|
|
|
|
|
|

Рис. 4. Распределение концентрации окислителя (1), горючего (2), продуктов реакции (3) и т-ры смеси (4) во фронте диффузионного горения; х-пространственная координата, ТГ-адиабатич. т-ра горения.
Пламя, которое образуется при истечении топлива в среду окислителя, называется диффузионным.

Рис.4 Форма диффузионного пламени а) при избытке окислителя, б) при избытке горючего.
Ламинарное диффузионное пламя наблюдается при ламинарном истечении горючего и окислителя.
22. Турбуле́нтность, устар. турбуле́нция (лат. turbulentus — бурный, беспорядочный), турбуле́нтное тече́ние — явление, заключающееся в том, что при увеличении скорости течения жидкости или газа в среде самопроизвольно образуются многочисленные нелинейные фрактальные волны и обычные, линейные различных размеров, без наличия внешних, случайных, возмущающих среду сил и/или при их присутствии. Механизм турбулентного распространения пламени и величина f/T зависят от масштаба турбулентности. В случае мелкомасштабной турбулентности, когда длина пути смешения мала по сравнению с шириной зоны ламинарного горения, считают, что фронт пламени в потоке имеет некоторое среднее положение и среднюю толщину и, так же как при горении в ламинарном потоке, сгорание происходит путем распространения непрерывного фронта пламени. Увеличение же скорости турбулентного распространения пламени вызвано увеличением скорости горения на единице поверхности такого осредненного фронта пламени. Это происходит вследствие того, что на процессы молекулярного переноса накладываются процессы турбулентного переноса, увеличивающие коэффициент переноса до ам + ат, где ат — коэффициент турбулентной температуропроводности. Скорость турбулентного распространения пламени определяется интенсивностью тепло- и массообмена и скоростью химического реагирования горючей смеси в потоке в специфических условиях зоны турбулентного горения, обусловливаемых ее аэродинамической и тепловой структурой.
|
|
|
23. Пла́мя — явление, вызванное свечением раскалённой газообразной среды, в ряде случаев содержащей плазму и/или диспергированные твёрдые вещества, в которой происходят физико-химические превращения реагентов, приводящие к свечению, тепловыделению и саморазогреву.
24. Излучение светящихся пламен складывается из излучения трехатомных газов и излучения раскаленных частичек сажи, образующихся в результате крекинга углеводородов. Наличие сажи в пламени резко меняет его эмиссионные характеристики. Сажистые частицы имеют непрерывный спектр излучения. В тех областях спектра теплового излучения пламени, где нет полос поглощения трехатомных газов, излучают только сажистые частицы.
|
|
|
Излучение светящегося пламени складывается из излучения трехатомных газов СО2 и Н2О и сажистых частиц.
25. Под скоростью горения жидкости понимается количество ее, выгорающее в единицу времени. Зависит от режима горения(ламинарного, турбулентного). Когда течение потока паров становится турбулентным ( при d 8Q см и выше), количество тепла, передаваемое на единицу поверхности жидкости, с повышением диаметра резервуара изменяется очень незначительно, в связи с чем и скорость горения увеличивается мало. Это положение очень важно, так как хранение нефтепродуктов и других горючих жидкостей чаще всего происходит в резервуарах диаметром выше 80 см. Поскольку скорость горения жидкости в таких резервуарах незначительно изменяется при увеличении их диаметра, следовательно, интенсивность подачи огнегасительных средств на единицу свободной поверхности жидкости является практически постоянной. Увеличение начальной температуры Т0 жидких ВВ имеет двойной эффект. Во-первых, с ростом Т0 возрастает скорость горения жидкости.
26. Вблизи от капли по сферической поверхности устанавливается зона горения, диаметр которого получается в 1-5 раз больше размера капли. Испарение капли протекает за счет теплоты излучения из зоны горения. В пространстве между каплей и зоной горения находится пары жидкого топлива и продукты горения, в пространстве вне зоны горения – воздух и продукты горения. В зону горения изнутри диффундирует пары топлива, а снаружи кислород. Здесь эти компоненты вступают в химическую реакцию, которая сопровождается выделением теплоты и образованием продуктов сгорания. Из зоны горения телота переносится наружу и к капле, а продукты сгорания диффундируют в окружающее пространство между каплей и зоной горения.
Так как скорость горения капли жидкости топлива определяется наиболее медленной стадией процесса - скоростью испарения, то время её выгорания можно расписать на основе уравнения теплового баланса её испарение за счёт теплоты, полученной из зоны горения. Таким образом, продолжительность выгорания капли, испоряющейся при лучистом нагреве от окружающей зоны горения, пропорциональна первой степени её начального радиуса.
Вопрос 45.
Деструкция - разложение органических веществ и превращение их в неорганические с высвобождением энергии.
27. Ключевым фактором, определяющим пожарную опасность материалов, является сырье, из которого они изготовлены. Наиболее часто встречающиеся минеральные строительные материалы - это природный камень, бетон, кирпич, керамика, асбоцемент, стекло и т.д. Они относятся к негорючим (НГ), но даже при небольшом добавлении полимерных или органических веществ - не более 5-10% от массы - их свойства меняются. Увеличивается пожарная опасность, и из НГ они переходят в категорию трудносгораемых. В последние годы широкое распространение получила продукция на основе полимеров, принадлежащая к неорганическим материалам и являющаяся горючей. При этом от объема и химического строения полимера зависит принадлежность конкретного материала к группе горючести. Выделяют два основных типа полимерных соединений. Это реактопласты, образующие при нагревании коксовый слой, который состоит из негорючих веществ и защищает материал от воздействия высоких температур, препятствуя горению. Другой тип - это термопласты (плавятся без создания теплозащитного слоя).
Вне зависимости от типа, полимерные строительные материалы нельзя перевести в разряд негорючих, но возможно снизить их пожарную опасность. Для этого применяются антипирены - различные вещества, которые способствуют повышению огнестойкости. Все органические материалы относятся к группе горючих, а их пожарная опасность повышается при добавлении различных полимеров. Например, лакокрасочные материалы не только повышают горючесть, но и способствуют более быстрому распространению пламени по поверхности, увеличивают дымообразование и токсичность. В этом случае к СО (угарному газу) - основному продукту горения органических материалов - добавляются и другие токсичные вещества.
28. Производства, связанные с получением и переработкой металлов, их сплавов, гидридов металлов и металлоорганических соединений характеризуются повышенной пожарной и взрывопожарной опасностью. Горение металлов, их сплавов, металлосодержащих веществ, в т.ч. металлоорганических веществ согласно ГОСТ 27331-87 подразделяются на 3 класса:
класс Д1 – горение легких металлов (алюминий, магний и их сплавы, кальций, титан), условно «тяжелых» металлов (цирконий, ниобий, уран и др.);
класс Д2 – горение щелочных металлов (литий, натрий, калий и др.);
класс Д3 – (металлоорганические соединения: алюмо-, литий-, цинк- органика, гидриды алюминия, лития и др.). Каждый из перечисленных металлов и их гидридов в обычном состоянии представляет собой твердое вещество, кроме металлоорганических соединений (МОС), представляющих собой жидкости.
Из особенностей металлов, которые имеют прямое отношение к их пожаро-, взрывоопасности и горению необходимо отметить следующие:
склонность к самовозгоранию при обычных условиях (т.е. пирофорность);
способность взрываться в состоянии аэровзвеси;
взаимодействие горящих металлов с водой, некоторыми газовыми огнетушащими составами: хладонами (хлорфторуглеводороды), азотом (например, магний) и др.
Способностью самовоспламеняться обладают щелочные металлы, стружка, металлические порошки, имеющие неокисленную активную поверхность, гидриды металлов, МОС (классы пожаров Д2, Д3).
Наиболее пожаро-, взрывоопасными металлами, горение которых происходит по классу Д1, являются легкие металлы в виде продуктов их переработки: порошков разной дисперсности, стружки. Металлы в виде изделий различной конфигурации (листы, профили и т.п.) поджечь практически невозможно, если обеспечиваются условия преобладания теплоотвода над теплоприходом.
29. Различают беспламенное горение твердых веществ (кокс, сажа, древесный уголь, щелочные и щелочноземельные металлы) и горение с образованием пламени (древесина, торф и т. д.). Скорость горения данного вещества зависит от температуры, давления, величины удельной поверхности вещества, скорости диффузии кислорода через пограничный .слой и скорости окислительных реакций и. Поскольку основой является реакция окисления, при уменьшении толщины пограничного слоя увеличивается скорость горения. Это и происходит в условиях пожара при увеличении скорости воздушных потоков, омывающих поверхности горящих веществ.
30. По скорости взрывчатого разложения различают:
быстрое сгорание,
собственно взрыв,
детонацию, происходящую с наибольшей скоростью и поэтому сопровождающуюся максимальным разрушительным действием.
Быстрым сгоранием взрывчатого вещества обычно называют процесс, скорость распространения которого по массе ВВ не превышает нескольких метров в секунду, а иногда - даже долей метра в секунду. Характер действия в этом случае - более или менее быстрое нарастание давления газов и производство ими работы разбрасывания или метания окружающих тел. Если процесс быстрого сгорания происходит на открытом воздухе, то он не сопровождается сколько-нибудь значительным эффектом.
Примером такой формы взрывчатого разложения может служить сгорание на открытом воздухе бездымного пороха.
Пороха (особенно бездымные) в закрытом объеме, например в патроннике ружья, разлагаются более энергично, чем на открытом воздухе, причем горение в этом случае сопровождается резким звуком. Это - типичная форма взрывчатого разложения ВВ в форме быстрого сгорания.
Взрыв, называемый иногда обыкновенным взрывом или взрывом второго рода, - это процесс, который может протекать с переменной скоростью, но значительно большей, чем в первом случае, в среднем со скоростью сотен метров в секунду.
Взрывчатые вещества, разлагающиеся в этой форме, характеризуют резкий подъем давления в месте взрыва, удар газов по окружающей среде или производство работы: раскалывание и дробление преграды на небольших расстояниях от места взрыва.
Примером этой формы взрывчатого разложения может служить вызванный лучом огня взрыв прессованного пироксилина в оболочке, протекающий со скоростью нескольких сотен метров в секунду.
Детонацией, или взрывом первого рода, называют процесс, который распространяется по массе вещества с максимальной скоростью, измеряемой обычно тысячами метров в секунду. Например, скорость детонации прессованного тротилового заряда составляет около 6700 м/сек.
Характер действия при детонации - особенно резкий скачок давления и удар газов, сопровождающийся сильнейшим разрушительным эффектом. Здесь налицо не раскалывание, а дробление преграды на мельчайшие куски.
Взрывчатых веществ очень много. По своему применению все они разбиваются на три большие группы:
инициирующие,
бризантные (дробящие),
метательные (пороха).
Инициирующие ВВ употребляются для снаряжения различных капсюлей, которые служат инициаторами взрывных процессов. Взрывчатое превращение этих веществ вызывается незначительным механическим или тепловым воздействием и, как правило, протекает в форме детонации.
Благодаря очень малому заряду дробящего вещества в капсюле ружейного патрона (0,004-0,005 г) он не оказывает сильного разрушительного действия и не может служить детонатором.
Бризантные ВВ в их чистом виде применения в охотничьих боеприпасах не находят.
31. По́рох — многокомпонентная твёрдая система, способная к закономерному горению параллельными слоями без доступа кислорода извне с выделением большого количества тепловой энергии и газообразных продуктов, используемых для метания снарядов, движения ракет и в других целях. Горение параллельными слоями, не переходящее во взрыв, обусловливается передачей тепла от слоя к слою и достигается изготовлением достаточно монолитных пороховых элементов, лишённых трещин. Скорость горения порохов зависит от давления по степенному закону, увеличиваясь с ростом давления, поэтому не стоит ориентироваться на скорость сгорания пороха при атмосферном давлении, оценивая его характеристики. Регулирование скорости горения порохов очень сложная задача и решается использованием в составе порохов различных катализаторов горения. Горение параллельными слоями позволяет регулировать скорость газообразования. Газообразование пороха зависит от величины поверхности заряда и скорости его горения.
Величина поверхности пороховых элементов определяется их формой, геометрическими размерами и может в процессе горения увеличиваться или уменьшаться. Такое горение называется соответственно прогрессивным или дегрессивным. Для получения постоянной скорости газообразования или её изменения по определённому закону отдельные участки зарядов (например ракетных) покрывают слоем негорючих материалов (бронировкой). Скорость горения порохов зависит от их состава, начальной температуры и давления.
32. Взрывчатыми могут быть конденсированные (твёрдые и жидкие) вещества, газы, а также взвеси частиц твёрдых или жидких веществ в газах. Во взрывной технике применяются конденсированные и водонаполненные ВВ, преимущество которых заключается в значительной концентрации энергии в единице объёма. В сочетании с большой скоростью процесса это позволяет получать при взрыве огромные мощности. Резко расширяясь, сжатый газ наносит по окружающей среде удар огромной силы. Происходит взрыв. Материалы, находящиеся вблизи от заряда, подвергаются дроблению и сильнейшей пластической деформации (местное, или бризантное, действие взрыва); вдали от заряда разрушения менее интенсивны, но зона, в которой они происходят, гораздо больше (общее, или фугасное, действие взрыва).
33. Состав продуктов взрыва — качественное и количественное содержание химических веществ, образующихся из взрывчатого вещества (ВВ) в результате взрыва. Состав продуктов взрыва определяется в основном составом ВВ (рецептурой ВВ) и условиями взрывания. При нулевом и положительном кислородном балансе для ВВ, состоящих из углерода, водорода, азота и кислорода, в основном в продуктах взрыва углерод окисляется до СО2, водород до Н2О, азот выделяется в свободном виде. Кроме того, в небольших количествах идет образование окислов азота NO, NO2, N2O3, свободного водорода Н2, аммиака NH3, метана СН4. Чем больше кислородный баланс, тем больше образуется окислов азота. Если в состав ВВ входят металлы (например, алюминий), то в продуктах взрыва они присутствуют, как правило, в виде окислов (Al2O3). При наличии серы образуются SO2 и H2S, при наличии хлора — хлористый водород HCl и хлориды металлов. Если в состав ВВ входит калиевая, кальциевая или натриевая селитра, то в продуктах взрыва образуются твёрдые окислы К2О, СаО или Na2О. Кислоро́дный бала́нс — отношение количества кислорода, содержащегося во взрывчатом веществе (ВВ) к его количеству, необходимому для полного окисления всех остальных компонентов этого ВВ.
34. Основными параметрами ударной волны, определяющими ее поражающее действие являются: избыточное давление, скоростной напор и продолжительность фазы сжатия. Избыточное давление в ударной волне- разность между давлением во фронте ударной волны и в окружающей невозмущенной среде. Один из основных параметров ударной волны ядерного взрыва, характеризующий ее поражающее действие. Определяет характер и тяжесть поражения личного состава, повреждений военной техники и других объектов в данной области пространства. Значение и изменение избыточного давления во времени зависят от мощности и вида взрыва, удаления от его центра (эпицентра) и среды, в которой он произведен. Величина скоростного напора находится в прямой зависимости от скорости и плотности воздуха за фронтом ударной волны. Оба эти параметра зависят от избыточного давления волны и связаны c величиной этого давления (при идеальных условиях фронтом ударной волны) определёнными равенствами. Для сильных ударных волн скоростной напор больше избыточного давления, но при избыточном давлении менее 4,9 кг/см скоростной напор меньше избыточного давления ударной волны. Подобно максимальному избыточному давлению ударной волны, максимальный скоростной напор уменьшается по мере удаления от центра взрыва, хотя и иными темпами.
35. Детона́ция (нормальная) — сверхзвуковой комплекс, состоящий из ударной волны и экзотермической химической реакции за ней.
Механизм превращения энергии на фронте детонационной волны существенно отличается от механизма дефлаграции — волны медленного горения, сопровождающейся дозвуковыми течениями. Принципиальная возможность явления детонации следует из того, что при прохождении через фронт всякой ударной волны вещество нагревается. Если ударная волна достаточно сильна, то это нагревание может поджечь горючую смесь, что и приводит к детонации. Возникающая при этом поверхность нормального разрыва называется детонационной волной. Изменение термодинамических параметров среды при прохождении через фронт детонационной волны описывается детонационной адиабатой. Явление детонации лежит в основе действия бризантных взрывчатых веществ, широко применяемых как в военном деле, так и в гражданской хозяйственной деятельности при производстве взрывных работ. Волна Д. возбуждается интенсивным механич. или тепловым воздействием (удар, искровой разряд, взрыв металлич. проволочки под действием электрич. тока и т.п.). Сила воздействия, необходимого для возбуждения Д., зависит от хим. природы ВВ. К механич. и тепловому воздействию особенно чувствительны Инициирующие взрывчатые вещества, к-рые входят в состав капсюлей-детонаторов, используемых для возбуждения Д. вторичных (менее чувствительных) ВВ.
В однородном ВВ волна Д. обычно распространяется с постоянной скоростью, к-рая среди возможных для данного ВВ скоростей детонационной волны является минимальной. В этом случае зона хим. реакции перемещается относительно продуктов реакции со скоростью звука. Благодаря этому волна разрежения, возникающая при расширении газообразных продуктов, не может проникнуть в зону реакции и ослабить ударную волну.
36. Температу́ра взры́ва — максимальная температура, до которой нагреваются продукты химических реакций, протекающих при взрыве.
Температура взрыва зависит от состава взрывчвтого вещества (ВВ), параметров заряда ВВ (размеры, плотность, влажность и др.) и условий взрывания (наличие оболочки, способ инициирования и др.).
Температура взрыва для определенных условий может быть рассчитана или определена экспериментально. Для экспериментального определения используют оптические цветовые методы.
37. Ско́рость детона́ции — скорость распространения детонационной волны по заряду взрывчатого вещества (ВВ). Скорость детонации определяется составом и состоянием заряда, условиями взрывания. При одинаковых условиях скорость детонации постоянна и её значение — максимально возможное при этих условиях. Такое свойство делает скорость детонации одной из важнейших характеристик взрывчатых веществ. Минимальная скорость детонации для твердых (конденсированных) взрывчатых веществ 1,2 км/с. Обычная скорость детонации промышленных ВВ 2,5-6,5 км/с, а взрывчатых химических соединений 7-9 км/с. Чем выше скорость детонации, тем выше давление детонации и эффективность действия взрыва.
38. Взрывные работы
работы в народном хозяйстве, выполняемые воздействием Взрыва на естественные (горные породы, древесина, лёд) или искусственные (бетон, каменная и кирпичная кладка, металлы и др.) материалы с целью контролируемого их разрушения и перемещения или изменения структуры и формы. В. р. осуществляются с помощью взрывчатых веществ (См. Взрывчатые вещества) (ВВ) и средств взрывания, создающих начальный импульс для возбуждения взрыва ВВ (капсюли-детонаторы с огнепроводным шнуром, электродетонаторы), а также передающих начальный импульс на требуемое расстояние (например, Детонирующий шнур). Для размещения ВВ внутри разрушаемого объекта (заряжания) предварительно создаётся полость (Шпур, Скважина, камера), как правило, Бурением, поэтому совокупность процессов для выполнения взрывов часто называют буро-взрывными работами. Дозированное количество ВВ, помещённое в полость или на поверхность разрушаемого объекта и снабженное средством взрывания, называется Зарядом.
При Составлении энергетического баланса взрыва парогазовой среды следует различать долю горючего вещества, участвующего во взрыве, и расход энергии этого взрыва на формирование ударной волны.
39. Диффузионное и кинетическое горение.
40 Структура диффузионного пламени.
41. Продукты сгорания. Дым.
Продукты горения (сгорания)
Продукты горения – это вещества (газообразные, жидкие или твердые вещества) и соединения, образующиеся в результате сложного физико-химического процесса горения веществ (материалов).
Под продуктами горения чаще всего понимают дым, токсичные продукты горения, сажу и другие.
Продукты горения сухой травы
Знание свойств и количества продуктов горения необходимо для расчета теплоты сгорания, температуры горения и других показателей, используемых для оценки пожаровзрывоопасности веществ (материалов), объектов с наличием этих веществ (материалов).
Состав
Состав их зависит от состава горящего вещества и условий его горения. В условиях пожара чаще всего горят органические вещества (древесина, ткани, бензин, керосин, резина и др.), в состав которых входят главным образом углерод, водород, кислород и азот. При горении их в достаточном количестве воздуха и при высокой температуре образуются продукты полного сгорания: СО2, Н2О, N2. При горении в недостаточном количестве воздуха или при низкой температуре кроме продуктов полного сгорания образуются продукты неполного сгорания: СО, С (сажа).
Продукты сгорания называют влажными, если при расчете их состава учитывают содержание паров воды, и сухими, если содержание паров воды не входит в расчетные формулы.
Реже во время пожара горят неорганические вещества, такие как сера, фосфор, натрий, калий, кальций, алюминий, титан, магний и др. Продуктами сгорания их в большинстве случаев являются твердые вещества, например Р2О5, Na2O2, CaO, MgO. Образуются они в дисперсном состоянии, поэтому поднимаются в воздух в виде плотного дыма. Продукты сгорания алюминия, титана и других металлов в процессе горения находятся в расплавленном состоянии.
При неполном сгорании органических веществ в условиях низких температур и недостатка воздуха образуются более разнообразные продукты – окись углерода, спирты, кетоны, альдегиды, кислоты и другие сложные химические соединения. Они получаются при частичном окислении как самого горючего, так и продуктов его сухой перегонки (пиролиза). Эти продукты образуют едкий и ядовитый дым. Кроме того, продукты неполного горения сами способны гореть и образовывать с воздухом взрывчатые смеси. Такие взрывы бывают при тушении пожаров в подвалах, сушилках и в закрытых помещениях с большим количеством горючего материала. Рассмотрим кратко свойства основных продуктов горения.
Углекислый газ
Углекислый газ или двуокись углерода (СО2) – продукт полного горения углерода. Не имеет запаха и цвета. Плотность его по отношению к воздуху равна 1,52. Плотность углекислого газа при температуре Т = 0 °С и при нормальном давлении р = 760 миллиметров ртутного столба (мм Hg) равна 1,96 кг/м3 (плотность воздуха при этих же условиях равна ρ = 1,29 кг/м3). Углекислый газ хорошо растворим в воде (при Т = 15 °С в одном литре воды растворяется один литр газа). Углекислый газ не поддерживает горение веществ, за исключением щелочных и щелочно-земельных металлов. Горение магния, например, происходит в атмосфере углекислого газа по уравнению:
CO2 +2 Mg = C + 2 MgO.
Токсичность углекислого газа незначительна. Концентрация углекислого газа в воздухе 1,5 % безвредна для человека длительное время. При концентрации углекислого газа в воздухе, превышающей 3-4,5 %, нахождение в помещении и вдыхание газа в течение получаса опасно для жизни. При температуре Т = 0 °С и давлении р = 3,6 МПа углекислый газ переходит в жидкое состояние. Температура кипения жидкой углекислоты составляет Т = –78 °С. При быстром испарении жидкой углекислоты газ охлаждается и переходит в твердое состояние. Как в жидком, так и твердом состоянии, капли и порошки углекислоты применяются для тушения пожаров.
Оксид углерода
Оксид углерода или угарный газ (СО) – продукт неполного сгорания углерода. Этот газ не имеет запаха и цвета, поэтому особо опасен. Относительная плотность равна 0,97. Плотность угарного газа при Т = 0 °С и р = 760 мм Hg составляет 1,25 кг/м3. Этот газ легче воздуха и скапливается в верхней части помещения при пожарах. В воде оксид углерода почти не растворяется. Способен гореть и с воздухом образует взрывчатые смеси. Угарный газ при горении дает пламя синего цвета. Угарный газ является очень токсичным. Вдыхание воздуха с концентрацией угарного газа 0,4 % смертельно для человека. Стандартные противогазы от угарного газа не защищают, поэтому при пожарах применяются специальные фильтры или кислородные изолирующие приборы.
Вода
Всем известная вода – Н2О – также выделяется во время горения виде газа – как пар. Вода является продуктом горения газа метана – СН4. Вообще, вода и углекислота в основном выделяются при полном сгорании всех органических веществ.
Цианистый водород
Цианистый калий – сильнейший яд – соль синильной кислоты, также известной как цианистый водород – HCN. Это бесцветная жидкость, но очень летучая (легко переходящая в газообразное состояние). То есть при горении она тоже будет выделяться в атмосферу в виде газа. Синильная кислота очень ядовита, даже небольшая – 0,01 процент – концентрация в воздухе приводит к летальному исходу. Отличительной чертой кислоты является характерный запах горького миндаля. Но синильной кислоте присуща одна «изюминка» – отравиться ей можно, не только вдыхая непосредственно органами дыхания, но и через кожу. Так что защититься только средствами индивидуальной защиты органов дыхания и зрения не получится.
Акролеин
Пропеналь, акролеин, акрилальдегид – все это названия одного вещества, ненасыщенного альдегида акриловой кислоты: СН2=СН-СНО. Этот альдегид тоже является сильно летучей жидкостью. Акролеин бесцветен, с резким запахом, очень ядовит. При попадании жидкости или ее паров на слизистые, особенно в глаза, вызывает сильное раздражение. Пропеналь является высокореакционным соединением, и это объясняет его высокую токсичность.
Формальдегид
Подобно акролеину, формальдегид принадлежит к классу альдегидов и является альдегидом муравьиной кислоты. Также это соединение известно как метаналь. Это токсичный, бесцветный газ с резким запахом.
Азотсодержащие вещества
Чаще всего во время горения веществ, содержащих азот, выделяется чистый азот – N2. Этот газ и так содержится в атмосфере в большом количестве. Азот может быть примером продукта горения аминов. Но при термическом разложении, к примеру, солей аммония, а в некоторых случаях и при самом горении, в атмосферу выбрасываются и его оксиды, со степенью окисления азота в них плюс один, два, три, четыре, пять. Оксиды – газы, имеют бурый цвет и чрезвычайно токсичны.
Сернистый газ
Сернистый газ (SO2) – продукт горения серы и сернистых соединений. Бесцветный газ с характерным резким запахом. Относительная плотность сернистого газа равна 2,25. Плотность этого газа при Т = 0 °С и р = 760 мм Hg составляет 2,9 кг/м3, то есть он намного тяжелее воздуха. Сернистый газ хорошо растворяется в воде, например, при температуре Т = 0 °С в одном литре воды растворяется восемьдесят литров SO2, а при Т = 20 °С – сорок литров. Сернистый газ горение не поддерживает. Действует раздражающим образом на слизистые оболочки дыхательных путей, вследствие чего является очень токсичным.
Дым
При горении многих веществ, кроме рассмотренных выше продуктов сгорания выделяется дым – дисперсная система, состоящая из мельчайших твердых частиц, находящихся во взвешенном состоянии в каком-либо газе. Диаметр частиц дыма составляет от 10−4 до 10−6 см (от 1 до 0,01 мкм). Отметим, что 1 мкм (микрон) равен 10−6 м или 10−4 см. Более крупные твердые частицы, образующиеся при горении, быстро оседают в виде копоти и сажи. При горении органических веществ дым содержит твердые частицы сажи, взвешенные в CO2, CO, N2, SO2 и других газах. В зависимости от состава и условий горения вещества получаются различные по составу и по цвету дымы. При горении дерева, например, образуется серовато-черный дым, ткани – бурый дым, нефтепродуктов – черный дым, фосфора – белый дым, бумаги, соломы – беловато-желтый дым.
В составе дыма, образующегося на пожарах при горении органических веществ, кроме продуктов полного и неполного сгорания, содержатся продукты термоокислительного разложения горючих веществ. Образуются они при нагреве еще негорящих горючих веществ, находящихся в среде воздуха или дыма, содержащего кислород. Обычно это происходит перед факелом пламени или в верхних частях помещений, где находятся нагретые продукты сгорания.
Состав продуктов термоокислительного разложения зависит от природы горючих веществ, температуры и условий контакта с окислителем. Так, исследования показывают, что при термоокислительном разложении горючих веществ, в молекулах которых содержатся гидроксильные группы, всегда образуется вода. Если в составе горючих веществ находятся углерод, водород и кислород, продуктами термоокислительного разложения чаще всего являются углеводороды, спирты, альдегиды, кетоны и органические кислоты. Если в составе горючих веществ, кроме перечисленных элементов, есть хлор или азот, то в дыме находятся также хлористый и цианистый водород, оксиды азота и другие соединения. Так, в дыме при горении капрона содержится цианистый водород, при горении линолеума «Релин» – сероводород, диоксид серы, при горении органического стекла – оксиды азота. Продукты неполного сгорания и термоокислительного разложения в большинстве случаев являются токсичными веществами, поэтому тушение пожаров в помещениях производят только в кислородных изолирующих противогазах.
Пепел, зола, копоть, сажа, уголь
Копоть, или сажа – остатки углерода, который не вступил в реакцию, по разным причинам. Сажу называют также амфотерным углеродом. Зола, или пепел – мелкие частицы неорганических солей, не сгоревших или не разложившихся при температуре горения. При выгорании топлива эти микросоединения переходят во взвешенное состояние или скапливаются внизу. А уголь – это продукт неполного сгорания дерева, то есть не сгоревшие его остатки, но при этом еще способные гореть. Конечно, это далеко не все соединения, которые выделятся при сгорании тех или иных веществ. Перечислить их всех нереально, да и не нужно, потому что другие вещества выделяются в ничтожно малых количествах, и только при окислении определенных соединений.
42 Горение твёрдых веществ. Общие положения.
43 Горение пыли. Общие положения.
44 Свойства аэровзвесей, характеризующие их пожаро- и взрывоопасность
45 Горение аэровзвесей.
46 Пределы воспламенения аэровзвесей.
47 Диффузионное горение жидкостей
48 Горение жидкостей. Общие положения
49 Тепловой баланс процесса горения жидкости в резервуар
Дата добавления: 2021-07-19; просмотров: 529; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!
