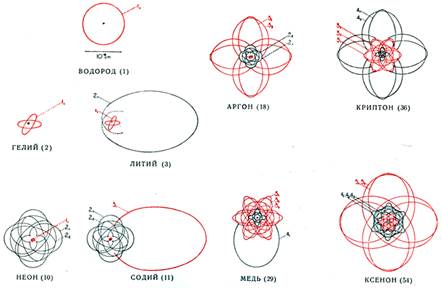
Результаты Н. Бора по атому водорода
●Были получены аналитические выражения: для энергий электронов на эллиптических орбитах, длин их больших полуосей, круговой частоты обращения.
●Был определён размер атома водорода в перманентом состоянии, соответствующий наинизшей орбите (1,1 10-8 см) и энергия связи электрона (13 эВ). Размер атома совпал с газокинетическим радиусом атома, а величина энергии связи[26] оказалась на 2 эВ больше экспериментального значения, определённого Дж. Томсоном в 1912 г. [27 , p . 488].
●Для формулы Ридберга, ν = R´(1/n2 – 1/m2) Бор вычислил постоянную Ридберга (R = 3,10´1015 Гц, против, экспериментального значения 3,29´1015 Гц). Тем самым, были подтверждены экспериментально отрытые серии Бальмера и Пашена, предсказаны серии в ультрафиолетовой и инфракрасной областях.
Модель, атома водорода, предложенная Бором смогла ответить на ряд вопросов:
●Почему в спектре звёзд наблюдается до 33 линий серии Бальмера, а в газоразрядных трубках лишь 12? – При n = 12 размер атома водорода около 1,6 10-6 см, такое среднее расстояние между атомами соответствует давлению около 7 мм рт. ст., при n = 33 размер атома 1,2 10-5 см, а давление – 0,02 мм рт. ст. “В соответствии с теорией необходимым условием появления большого числа линий, следовательно, является очень маленькая плотность газа…” [27 , p . 9]
●Почему в спектре некоторых звёзд спектральная серия «водорода» (серия Пиккеринга) может быть рассчитана с помощью формулы Ридберга (ν = R´(1/2,52 – 1/m2)? – Бор показал, что эти линии, а также линии, открытые Фаулером в 1912 г. для смеси водорода и гелия в газоразрядной трубке, принадлежат однозарядному иону гелия, а не атому водорода.
|
|
|
●Почему в водороде для серии Бальмера при нормальных условиях нет линий поглощения соответствующих линиям испускания, линии поглощения наблюдаются только в светящемся водородном газе, в то же время у паров натрия совпадение линий наблюдается? – Согласно теории Бора, излучение серии Бальмера возникает при переходе с n = 2, но обычному состоянию водорода отвечает n =1, кроме того, при обычных условиях водород находится в молекулярном состоянии, а в молекулах иные частоты электронов, чем в атоме. А если, “например, пары натрия поглощают излучение, соответствующее линиям линейчатого спектра вещества, мы можем заключить, с другой стороны, что упомянутые линии испускаются во время перехода системы между двумя состояниями, одно из которых является перманентным” [27 , p . 16].
В своей первой работе, как и последующих Н. Бор затронул и теорию вопроса многоэлектронных атомов, а также строения молекул. Применив к многоэлектронному атому свою модель, говоря современным языком водородоподобного атома, Н. Бор дал объяснение, например, возникновению К-серии рентгеновского излучения исходной посылкой к которому была гипотеза Дж.Дж. Томсона. Бор показал, что энергия связи электрона с ядром водородоподобного атома примерно равна энергии электрона в катодном луче, порождающем характеристическое рентгеновское излучение [27 , p . 498-499].
|
|
|
▼Приведённые примеры результатов, полученных Н. Бором, вполне соответствуют той последовательности научной работы, которую описал А. Пуанкаре. Из своих предположений Н. Бор получил непосредственные следствия, в ряде случаев уточнил их (в последующих статьях он учёл, например, массу электрона, которой пренебрёг в первой статье); а проверкой предположений в физике является эксперимент, поэтому открытие буквально в течение следующего 1914 г. серии Лаймана, постановка опытов Франка и Герца, объяснение эффекта Штарка – всё это стало проверкой теории Бора и его атомной модели.
Заключение
Модель атома по Бору продолжала развиваться и усложняться; для описания атома было введено уже не одно, как было первоначально, а четыре квантовых числа; предпринималась попытка дать им механическое толкование, построить механическую модель.
|
|
|
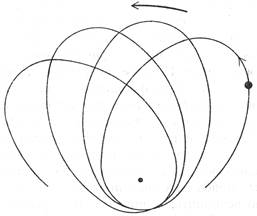
Электронные орбиты по согласно теории Бора-Зоммерфельда [29]
| Модель атома водорода | Движение электрона в атоме водорода | |

|
| |
| Орбиты задаются двумя квантовыми числами |
| |
| Схема структуры атомов некоторых элементов | ||
|
| 
| |
А. Зоммерфельд предположил, что одному значению главного квантового числа может соответствовать движение электронов по эллиптическим орбитам разной вытянутости, характеризуемой орбитальным квантовым числом (энергии этих движений так же несколько различаются). Плоскость орбиты при движении электрона может вращаться, а электрон описывает при этом сложную траекторию; ещё одним квантовым числом стали характеризовать возможный наклон плоскости орбиты [29], спин электрона должен был характеризовать его вращение. Хотя сам Н. Бор уже в самой первой работе подчёркивал определённую условность описания атома в рамках механики (“Динамическое равновесие систем в стационарных состояниях может обсуждаться при помощи обычной механики” - это отнюдь не признание самого «механического» характера атома), ко второй половине 1920-х гг. возникла законченная[27] «квази-механическая» планетарная модель атома[28]. Как показало дальнейшее развитие физики, с одной стороны, модель оказалась не способной в полной мере объяснить всю совокупность атомных явлений (наука выявила более глубокое понимание квантово-механических основ природы), а с другой, она и сегодня используется в средней школе на уроках физики и химии при объяснении устройства атома. Воспользуемся предисловием Н.А. Умова к книге А. Пуанкаре “Наука и гипотеза” (1903), чтобы понять, что вкладывали учёные-физики в конце XIX - нач. ХХ вв. в понятие модель, и какие два типа моделей они выделяли:
|
|
|
“…мы можем только строить образы или же воспроизводить определённые модели соотношений явлений между явлениями природы. Эти модели представляют собой или счастливое сочетание фигур и движений, нисходя даже до употребления растяжимых или нерастяжимых нитей, волчков, и т.д., говорящих чувствам и воображению, не имеющих претензии представлять отражение реальных явлений[29], а только имитацию открытых в них соотношений. Или же эти модели представляют собой ряд условных символов, связанных математическими соотношениями, ничего не говорящих нашему чувству и воображению, но дающих возможность путём математического развития прийти к новым соотношениями между символами, соответствующими реальным вещам. К первой группе относятся модели английских физиков Кельвина и Максвелла <…> ко второй группе методы Гельмгольца, Герца и др. <…> У. Томсон (лорд Кельвин) говорит: “Мне кажется, что истинный смысл вопроса: понимаем мы или не понимаем мы физическое явление? – сводится к следующему: можем мы построить соответствующую механическую модель? Я остаюсь неудовлетворённым, пока не построю такой модели, если я смогу её сделать, я пойму, в противном случае я не понимаю”. Из слов Гельмгольца <…> “Английские физики – лорд Кельвин, формулируя свою теорию вихревых атомов, и Максвелл, создавая систему клеток, содержимое, которых охвачено вихревым движением, – ту гипотезу, которая служит основанием его попытки механического объяснения электромагнетизма, – очевидно, находили в подобного рода объяснениях гораздо больше удовлетворения, чем в изображении явлений системой дифференциальных уравнений физики, что касается меня, я должен сознаться, что предпочитаю последний способ изображения, в нём я более уверен, чем во всяком другом; но я не могу выставить никакого принципиального возражения против методы, которой придерживаются такие великие физики” [30, С. 247-248].
Отвлекаясь от двух типов научного мышления, которые представляют Кельвин и Гельмгольц, укажем, что в рамках обучения в средней школе мы весьма ограничены в использовании моделей в виде математических уравнений, в силу как математической подготовки, так и уровня развития абстрактного мышления школьников. Поэтому планетарная модель Резерфорда-Бора-Зоммерфельда используется и, видимо, будет использоваться, в процессе обучения в школе, во-первых, как отвечающая принципу наглядности; во-вторых, как иллюстрирующая основные положения физики атома, изучаемые в школе (включая понятие о волне де Бройля), в-третьих, и мы старались это показать в рамках настоящей статьи, как пример, на котором возможно показать старшеклассникам становление и развитие физической теории (включая принципы соответствия и дополнительности, развитые Н. Бором). При этом, однако, необходимо подчеркнуть два момента (а этого, увы, часто не происходит): ●нельзя отождествлять механическую планетарную модель атома с реальной современной физической картиной строения атома вещества, ●механические модели не являются единственно возможным типом моделей в физике. Нужно суметь выдержать очень тонкую линию преподавания: не следует, на наш взгляд, спешить с уравнением Шрёдингера в курсе школьной физики, а к модели Бора нужно подвести учеников как к определённой вершине человеческой мысли, подчёркивая при этом, что наука значительно продвинулась вперёд за прошедшие сто лет, а мы должны быть признательны, учёным-физикам, которые в условиях мирового кризиса и разъединения государств, разразившихся сто лет назад, совместно совершали открытия в науке, которые занимают наши умы и сегодня, и среди этих учёных, безусловно, имя датского физика и философа Н. Бора в первых рядах.
Некоторые работы Н. Бора в журналах, доступных на сайте http://archive.org,
1. Bohr N. E. On the Theory of the Decrease of Velocity of Moving Electrified Particles on passing through Matter // Philosophical Magazine V. 25. pp. 10-31. 1913
2. Bohr N. E. On the Constitution of the Atom and Molecules. The blinding of electrons by positive nuclei // Philosophical Magazine V. 26. pp. 1-25. 1913.
3. Bohr N. E. On the Constitution of the Atom and Molecules. Systems containing only a single nucleus // Philosophical Magazine V. 26. pp. 476-502. 1913.
4. Bohr N. E. On the Constitution of the Atom and Molecules. Systems containing several nuclei // Philosophical Magazine V. 26. pp. 857-875. 1913.
5. Bohr N. E. Hydrogen and Helium spectra // Nature V. 92. pp. 231-232. 1913.
6. Bohr N. E. Atoms models and X-ray spectra // Nature V. 92. pp. 553-554. 1914.
7. Bohr N. E. On the Effect of Electric and Magnetic Fields on Spectral lines // Philosophical Magazine V. 27. pp. 506-524. 1914.
8. Bohr N. E. Hydrogen and Helium spectra // Nature V. 95. pp. 6-7. 1913.
9. Bohr N. E. Onthe Series spectrum of Hydrogen and Atomic spectrum. // Philosophical Magazine V. 29. pp. 332-335. 1915.
10. Bohr N. E. Quantum theory of radiation and atomic structure. // Philosophical Magazine V. 30. pp. 394-415. 1915.
Литература.
1. Содди Ф. Радий. 11 общедоступных лекций. М.: Космос. 1910. 168 С.
2. Перрен Ж. Предисловие к русскому изданию кн. Ж. Перрен “Атомы” /серия “Современные проблемы естествознания” кн. 20. М. ГосИздат. 1924. XVI + 254 С.
3. Хвольсон О.Д. Курс физики. т. Дополнительный. Ч. II. Физика 1914 – 1926 гг. М-Л. ГосИздат 1926. 275 С.
4. Хвольсон О.Д. Характеристика развития физики последние 50 лет. Л.: ГосИздат. 1924. 218 С.
5. Райс Ф., Долджин К. Психология подросткового и юношеского возраста. 12-е изд. С.-Пб.: Питер. 2012. 816 С.
6. Мякишев Г.Я. Буховцев Б.Б. Физика-11. 11-е изд. М. Просвещение. 2003. 336 С.
7. Behrens C.E. Atomic Theory from 1904 to 1913 // American Journal of Physics. V. 11. No 1 pp.60-66. 1943.
8. Томсон-Кельвин В. О вихревых атомах. / в кн. Дж.Дж. Томсон Электричество и материя. Москва-Ижевск: НИЦ «Регулярная и хаотичная динамика». 2004 С. 184 – 198.
9. Джеммер М. Эволюция понятий квантовой механики. М. Наука. 1985. 380 С.
10. Lord Kelvin. Aepinus Atomized. // Philosophical Magazine V.3 pp. 257 – 283. 1902.
11. Thomson J. J. On the Structure of the Atom...// Philosophical Magazine V.7 pp. 237 – 265. 1904.
12 Томсон Дж .Дж. Электричество и материя. / в кн. Дж.Дж. Томсон Электричество и материя. Москва-Ижевск: НИЦ «Регулярная и хаотичная динамика». 2004 С. 9 – 97.
13. Ландсберг Г.С. Теория атома. / в сб. Наука ХХ века. Физика. Т. II. М.-Л. ГосИздат 1929 г. С. 131 – 187.
14. Хвольсон О.Д. Курс физики. т. Дополнительный. Ч. I. Физика 1914 – 1926 гг. М-Л. ГосИздат 1926. 308 С.
15. Шишковский Б.А. Применение теории строения атомов и молекул Дж.Дж. Томсона к химии // ЖРФО № 8 1915.
16. Thomson J.J. On the Structure of the Atom. // Philosophical Magazine V. 26. pp. 792-799. 1913.
17. Nagaoka H. Kinetic of a System of Particles illustrating the Lines and the Band Spectrum and the Phenomena of radioactivity. // Philosophical Magazine V. 7. pp.445-455. 1904.
18. Rutherford E. The Scattering of α and β Particles by Matter and the Structure of the Atom. // Philosophical Magazine V. 21. pp. 669-688. 1911.
19. Nicholson J. W. A Structural Theory of the Chemical Elements // Philosophical Magazine V. 22. pp. 864-889. 1911.
20. McCormmach R. The Atomic Theory of John William Nicholson // Archive for History of Exact Sciences V. 3 issue 2, pp. 160-184
21. Behrens C.E. Bohr’s Early Atomic Theory // American Journal of Physics. V. 11. No 5. pp.272-281. 1943.
22. Бор Н. Избранные научные труды в двух томах. Ред. И.Е. Тамм, В.А. Фок, В.Г. Кузнецов. Т.1 М. Наука 1970. 585 С.
23. Bohr N. E. On the Theory of the Decrease of Velocity of Moving Electrified Particles on passing through Matter // Philosophical Magazine V. 25. pp. 10-31. 1913.
24. Пуанкаре А. Математическое творчество. Психологический этюд. М. Типография Эл. Бергмана. 1909. 24 С.
25. Нестурх К.Ф Строение атома по Бору. // Ж.Р.Ф.-Х.О. Отдел II “Вопросы физики”. Т. 45. вып. 8-9. С. 277 – 289. 1913.
26. Ельяшевич М.А. Важнейший этап развития квантовой теории (к выходу первого тома избранных научных трудов Нильса Бора). //УФН Т. 103 вып. 2. С. 381 – 386. 1971.
27. Bohr N. E. On the Constitution of the Atom and Molecules // Philosophical Magazine V. 26. pp. 1-25, 476-502, 857-875. 1913.
28. Касьянов В.А.. Физика-11. М.: Дрофа. 2003.
29. Крамер Г.А., Гольст Х. Строение атома и теория Бора. М.-Л.: ГосИздат. 1926. 155 С.
30. Умов Н.А. Предисловие к книге Пуанкаре “Наука и гипотеза” (1903) /в Н.А. Умов Собрание сочинений, т. III. ред. А.И. Бачинский. М. Императорское общество испытателей природы. 1916. С. 247 – 249.
[1] “Доживём до понедельника” реж. С. Ростоцкий
[2] Выделено мной М.Б.
[3]О.Д. Хвольсон (1852 – 1934) чл.-корр. Петербургской Академии наук, почётный академик АН СССР, его основные научные работы относятся к концу XIX века, он также автор знаменитого курса физики (5 томов плюс два дополнительных), в 1920-е гг. Хвольсон написал небольшую работу, в которой в рамках теории относительности А. Эйнштейна предсказал эффект гравитационного линзирования света.
[4] Здесь и далее в приведённых фрагментах курсив О.Д. Хвольсона.
[5] Речь идёт не об уроке «в стихах», театральных сценках и т.п., имеется в виду, что ученики на уроке должны прочувствовать то высокое напряжение мысли и эмоций, которым сопровождалось рождение принципиально новой теории в физике.
[6] Полное овладение наблюдается к возрасту 20 – 21 года.
[7] Bohr found the ground for his fundamental assumptions pretty well prepared.
[8] Многие публикации фундаментальных работ по теории атома: В. Кельвина, Дж. Дж. Томсона, Э. Резерфорда, Н. Бора были сделаны в крупнейшем английском научном журнале Philosophical Magazine и в журнале Nature. Номера этих журналов конца XIX начала ХХ века – доступны на сайте http://archive.org/, полезно познакомить учащихся с некоторыми формулировками оригинальных работ и указать, что при желании ученики могут сами попытаться прочесть эти работы, при некотором знании английского языка, конечно.
[9] Чтобы получить отклонение a-частиц на большие углы согласно модели Томсона необходимо было предположить их многократное рассеяние на атомах мишени, при этом число частиц, отклонённых на угол q убывало экспоненциально с ростом угла, в то время как эксперимент подтвердил вывод Э. Резерфорда об убыли пропорционально sin4(q/2), чтобы наглядно показать различие, укажем. что согласно Томсону при q = 300 должна наблюдаться 1 частица из 1013; в эксперименте Э. Марсденом наблюдалась 1 частица из 8000 [7 , p.62]
[10]Электрон в модели Нагаоки по оценке Шотта успевал сделать максимум десяток оборотов за время существования атома
[11] Важно показать ученикам, что модель Резерфорда могла объяснять и то, что не укладывалась в модель Томсона, и то, что та объясняла удовлетворительно.
[12] Лишь в 1927 г. было показано, что линии соответствуют спектру ионизированных атомов кислорода и азота.
[13]“angular moment”, в ряде переводов сохраняется дословная трактовка этого термина “угловой момент”, в других – “момент количества движения”, в современной терминологии – момент импульса, мы сохранили терминологию переводов начала ХХ века.
[14]Behrens видит в этом фрагменте истоки формирования принципа соответствия, сформулированного Н. Бором.
[15] “He was insistent on the point that the atomicity of the quantum theory was rooted in the mechanical system and not in the radiation field” [20 , p. 171].
[16] “On the Theory of the Decrease of Velocity of Moving Electrified Particles on passing through Matter”; в русском переводе статья называется “Теория торможения заряженных частиц веществом” [22]
[17]А. Пуанкаре написал небольшой этюд, выделив в нём характерные моменты личного научного творчества учёного: ●предварительная сознательная работа; ●бессознательная работа (невидимая, скрытая); ●озарение; ●второй период сознательной работы “...проблески внезапного озарения <…> являются признаками долгой предшествующей работы. <…> Нередко, работая над трудным вопросом, на первый раз только и делаешь, что принимаешься за работу; <…> ...она /бессознательная работа – М.Б./ возможна и, во всяком случае, плодотворна только тогда, когда, с одной стороны, ей предшествует, а с другой, следует за ней период сознательной работы. <…> Необходимость второго периода сознательной работы после вдохновения ещё более понятна. Нужно воспользоваться результатами этого вдохновения, вывести из них непосредственные следствия, привести их в порядок, редактировать доказательства. Но главным образом нужно их проверить” [24 , С. 14-15]. Эти моменты могут охарактеризовать как работу самого Н. Бора над созданием теории атома, так и работу учёных начала ХХ века по исследованию строения атома.
[18] Курсив Хвольсона
[19] К.Ф. Нестурх (1913 г.) переводит этот термин как “прочное состояние” [25].
[20] Н. Бор адресовал эти предположения выводу энергии связи электрона с положительным ядром.
[21] В работах 1914 – 1915 гг. Бор дал варианты трактовок основных предположений теории, см. работы 7 и 10 списка в конце статьи.
[22] Курсив Н. Бора.
[23] Чтобы оценить те нюансы, которые вносит перевод на русский язык, достаточно сравнить оригинальный текст с переводами последних пяти предположений в [9 , с.88-89] и [22 , с147-148].
[24] Хотя в гуманитарном классе мог бы получиться интересный языковой проект по переводу оригинальных работ на русский язык, но это не тема урока.
[25] Так, например, В.А. Касьянов использует для формулировки постулата Бора понятие длины волны де Бройля, оговаривая, правда, что это понятие введено в науку позже [28].
[26]Современное значение 13,55 эВ, т.е. теория Н. Бора точнее предсказывала определённые параметры, чем это было экспериментально измерено на тот момент.
[27] Т.е. были «исчерпаны» все ресурсы объяснения устройства атома, сочетавшего механические принципы и квантовые постулаты Н. Бора.
[28]В книге Г.А. Крамерса [29], вышедшей через 10 лет после первых статей Бора в 1923 г. с предисловием Э. Резерфорда (переведёна на русский язык в 1926 г.), основные положения теории Бора сформулированы в виде двух гипотез или постулатов, первый из которых утверждает наличие стационарных состояний, в которых атом не излучает, а второй определяет квантованный характер излучения и энергию испущенного кванта; вместо понятие “перманентное” состояние атома, авторы используют термин “нормальное”; так по мере развития теории происходит не только её углубление и расширение, но и уточнение её основных исходных предположений и терминологии, ещё раз подчеркнём, что в том же 1926 г. в курсе Хвольсона мы встречаемся с тремя постулатами Бора.
[29] Выделено мной М.Б.
Дата добавления: 2021-03-18; просмотров: 123; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!