Для карбоновых кислот характерна изомерия углеродной цепи.
КАРБОНОВЫЕ КИСЛОТЫ
Ребята, о чем может рассказать эта формула (формула СН3СОН).
Что образуется при окислении альдегида (напишите уравнение реакции )

(карбоновая кислота)
В 1714 г. по указу Петра I в Петербурге был заложен аптекарский сад. Там выращивали лекарственные растения, снабжая ими аптеки или перерабатывая их на лекарства. Так вот, листья одного из таких растений, помещенные в молоко, предохраняют его от скисания. Свежее мясо и рыба, переложенные этим растением, дольше сохраняются. Из его корней можно получить желтый краситель. Листья – неистощимая основа для фантазии хозяйки по приготовлению здоровой и полезной пищи. Личный опыт общения с этим растением способен довести до слез. Это – …Назовите это растение! (Ответ: Крапива)
- На столе лежат яблоко, апельсин, аспирин, мыло.
- Как вы думаете, что объединяет все эти предметы? Правильно, в них есть кислоты – из класса органических карбоновых кислот.
Тема нашего урока - Карбоновые кислоты
А какие ассоциации возникают у вас при упоминании слова «кислота»? («кислые», «едкие», «жидкие», «опасные», «несъедобные»…). Сравним ваши ассоциации в конце урока, ответив на вопрос: Все ли кислоты опасные?
На данном уроке мы познакомимся с новым классом кислородосодержащих соединений – карбоновыми кислотами.
Я хочу, чтобы вы сами назвали задачи, которые стоят перед нами сегодня на уроке:
· сформулировать определение,
|
|
|
· вывести общую формулу,
· изучить классификацию,
· рассмотреть физические свойства,
· определить закономерности, вытекающие из электронного строения,
· оценить разнообразие
· и наряду со всем названным познать области применения веществ.
Эпиграф. «Жизнь учит только тех, кто её изучает”, и это не случайно. Вы ещё раз убедитесь, что те вещества, о которых будет идти речь в данной теме, очень важны в жизни, в необходимости изучения свойств этих веществ и действия их на организм.
- Изучение новой темы
Объяснение темы происходит с применением презентации через проектор.
Карбоновые кислоты – кислородсодержащие органические вещества,содержащие в молекуле одну или несколько карбоксильных групп СООН
Общая формула: R – COOH
Общая формула одноосновных кислот предельного ряда СnH2n+1COOН где n может быть равно нулю
Проблемный вопрос: почему данные кислоты имеют первое слово «карбоновые»?
«Карбо» - углерод Þ кислоты углерода.
Классификация карбоновых кислот
1) В зависимости от числа карбоксильных групп:
• одноосновные, например уксусная
• двухосновные, например щавелевая
• многоосновные, например лимонная
2) В зависимости от природы радикала:
|
|
|
• предельные, например пропионовая
• непредельные, например акриловая
• ароматические, например бензойная
Номенклатура (слайд ).
Для определения названия в соответствии с международной номенклатурой придерживаются порядка:
1) Нумеруют цепь, начиная с карбоксильной группы;
2) Называют номер атома углерода, при котором находится радикал;
3) Называют радикал;
4) Называют углеродную цепь;
5) Добавляют суффикс - овая кислота
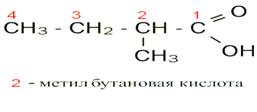
Задание. Дать название веществам и составить формулы карбоновых кислот.
- СН3 - СН2 - СН2 – СН – СН – СООН 2,2-диметилбутановая кислота
2. СН3 - СН – С – СООН 2,3 – диметилпентановая кислота
3. CH3 – CH – COOH 3-метилпентановая кислота
Многие кислоты имеют и исторически сложившиеся, или тривиальные названия, связанные, главным образом, с источником получения:
Сейчас я буду говорить вам, где содержится кислота, а вы постараетесь догадаться, как кислота называется.
В щавеле содержится…… (щавелевая кислота).
В корнях растения валерианы…… (валериановая кислота).
В яблоках……. (яблочная кислота).
В лимоне…… (лимонная кислота).
В молоке (прокисшем)……(молочная кислота).
В сливочном масле (прогорклом)…….(масляная кислота).
|
|
|
Таким образом, карбоновые кислоты не обязательно получать синтетически, их можно выделить из окружающих нас растений, они содержатся в продуктах.
Для карбоновых кислот характерна изомерия углеродной цепи.
Она начинается с бутановой кислоты (С3Н7СООН), которая существует в виде двух изомеров:
Бутановая кислота и 2-метилпропионовая кислота
Физические свойства.
НСООН … С9Н19СООН - жидкости
С10Н21СООН - твердые вещества, высшие к/к - без запаха.
Зависимость физических свойств карбоновых кислот от строения молекулы:
С увеличением относительной молекулярной массы в гомологическом ряду предельных одноосновных карбоновых кислот - увеличивается их плотность, температура кипения и плавления, уменьшается растворимость в воде.
Что влияет на физические свойства карбоновых кислот?
Электронное строение молекулы. Давайте рассмотрим электронное строение молекул карбоновых кислот. (На доске)
Рассмотрите строение молекулы карбоновой кислоты. Из каких двух самостоятельных групп состоит карбоксильная группа?
Карбонил: - С = О Гидроксил: - ОН
Какова особенность электронного строения карбонильной группы?
Связь С=О полярная, плотность смещена к атому кислорода. Электронная плотность в карбонильной группе (особенно σ-связи) смещена в сторону кислорода, как более электроотрицательного элемента. Вследствие этого карбонильный атом углерода приобретает частичный положительный заряд. Чтобы его компенсировать, он притягивает к себе электроны атома кислорода гидроксильной группы. Электронная плотность на атоме кислорода понижается и он смещает в свою сторону электронную плотность связи О – Н. Полярность связи в гидроксогруппе возрастает, водород становится подвижнее и легче отщепляется в виде протона, что обуславливает общие свойства карбоновых кислот.
|
|
|
Какие свойства придает спиртам наличие гидроксила?
За счет подвижности атома водорода спирты проявляют слабые кислотные свойства.
И вот две эти функциональные группы соединены между собой полярность связи – О — Н гидроксильного фрагмента, ион водорода легче отщепляется, кислотные свойства карбоновых кислот значительно сильнее по сравнению со спиртами
- Химические свойства карбоновых кислот (на опытах)
Прежде чем перейти к следующему разделу, ставлю проблему.
Проблема: некоторые лекарственные препараты нельзя запивать целым рядом напитков, в том числе кислые фрукты и соки, маринады, блюда с уксусом нельзя употреблять в пищу наряду с антибиотиками пенициллинового ряда и эритромицином. Как вы думаете, чем вызван данный запрет?
Кислоты, содержащиеся в указанных продуктах, могут вступать в химическое взаимодействие с названными антибиотиками, нейтрализуя их воздействие на организм.
ИТОГ: Действительно, все дело в химическом взаимодействии кислот с различными веществами.
Рассмотрим химические свойства:
Ребята, не забывайте, при работе с кислотами и щелочами необходимо быть предельно осторожными, соблюдать правила техники безопасности. При попадании веществ на кожу немедленно промыть водой.
2HCOOH + MgO = (HCOO)2Mg + H2O
HCOOH + NaOH = HCOONa + H2O
4. Реагируют с солями (видеоопыт)
2CH3COOH + CaCO3 = (CH3COO)2Ca + H2O + CO2
5. Реагируют со спиртами (видеоопыт)
CH3COOH+ C5H11OH = CH3COOC5H11+ H2O
6.Горение (видеоопыт)
СН3СООН+2О2=2СО2+2Н2О
Карбоновые кислоты обладают и некоторыми специфическими свойствами, обусловленными наличием в их молекулах радикалов. Так, например, уксусная кислота реагирует с хлором:
Cl – Cl + CH3COOH → Cl CH2COOH + HCl
монохлоруксусная
кислота
Муравьиная кислота по химическим свойствам несколько отличается от других карбоновых кислот.
1. Из одноосновных карбоновых кислот муравьиная кислота является самой сильной кислотой.
2. Муравьиная кислота подобно альдегидам легко окисляется (реакция «серебряного зеркала»)
НСООН + Ag2О → НОСООН + 2Ag↓
угольная кислота
Кейс-задание.
- В истории известен следующий интересный факт:
Римский историк Кай Плиний Старший (23 – 79 гг.н.э.) пересказал легенду о жемчужинах Клеопатры. Египетская царица устроила пир в честь римского полководца Марка Антония. А надо сказать, что среди сокровищ сказочно богатой Клеопатры больше всего славились серьги с огромными грушевидными жемчужинами, массу которых историки оценивали в 40,2г. Желая поразить римского гостя, Клеопатра растворила одну из жемчужин с уксусной кислотой и выпила за здоровье Антония. Какую реакцию осуществила Клеопатра. Какое соединение она принимала? Написать уравнение соответствующей реакции.
Жемчуг - это перламутр, который состоит из шестиугольных пластинок арагонита. Химическая формула его CaCO3 (карбонат кальция). А карбонат кальция легко взаимодействует даже с очень слабыми кислотами (к которым относится и уксусная).
Происходит реакция нейтрализации. Чем в свое время и воспользовалась знаменитая Клеопатра. СаСО3 + 2СН3СООН =(СН3СОО)2Са + Н2О + СО2↑
Дата добавления: 2021-01-21; просмотров: 57; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!
