Опыт 2. Получение, собирание и распознавание водорода.
Повторите основные способы получения, собирания и распознавания газов. Для этого внимательно изучите информацию из практического занятия.
Выполните только опыт №1 (просмотрите в приложении ВК видео).
При оформлении протокола укажите дату занятия, название и цель практического занятия, оборудование и реактивы (только те, которые используются в опыте №1)
В ходе практической работы напишите пошагово отчет о проделанной работе.
Ответьте на вопросы и выполните задания в конце опыта №1.
ПРАКТИЧЕСКОЕ ЗАНЯТИЕ №5
Получение, собирание и распознавание газов
Цель занятия: повторить способы получения, собирания газов, их физические и химические свойства, совершенствовать приемы работы с лабораторным оборудованием и химическими веществами.
Оборудование и реактивы: штатив с пробирками, лабораторный штатив, пробка с газоотводной трубкой, спиртовка, шпатель, вата, химические стаканы, кристаллизатор (сосуд для охлаждения водой), фарфоровая чашка, ложечка для сжигания веществ, стеклянная палочка, лучина, спички, оксид марганца (IV), перекись водорода, гранулы цинка, соляная кислота, мел, раствор соляной кислоты, известковая вода, твердый хлорид аммония, твердое вещество гидроксида кальция, вода, универсальная лакмусовая бумага, раствор фенолфталеина, раствор лакмуса.
Техника безопасности.
1. Вспомните общие правила техники безопасности в кабинете «Химия».
|
|
|
2. Осторожно использовать стеклянную посуду.
3. Осторожно использовать кислоты и щелочи. Всегда следует наливать кислоту в воду.
4. При получении водорода горящая спиртовка не должна находиться рядом с прибором для получения этого газа.
5. Пробирку с веществом прогревают сначала всю в верхней части пламени, а затем ту часть, где находится вещество. При нагревании жидкости отверстие пробирки следует направлять в сторону от себя и других людей. При нагревании объем вещества не должен превышать 1/3 объема пробирки.
Правила первой помощи.
При ранении стеклом удалить осколки из раны, смазать края раны раствором йода и перевязать бинтом. При необходимости обратиться к врачу.
При ожоге кислотой следует промыть место ожога проточной холодной водой, а затем нейтрализовать остатки кислоты мыльным раствором.
При ожоге щелочью следует промыть место ожога проточной холодной водой, а затем нейтрализовать остатки щелочи 3% раствором борной кислоты.
Ход практической работы.
Опыт 1. Получение, собирание (методом вытеснения воздуха) и распознавание кислорода
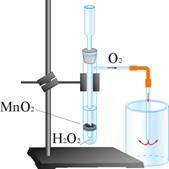
|
| Рис.2. Установка для получения и собирания кислорода из перекиси водорода |
1. Соберите прибор для получения газов и проверьте его на герметичность.
|
|
|
2. В пробирку положите одну ложечку для сжигания веществ оксида марганца (IV).
3. Прилейте в нее 2 мл перекиси водорода.
4. Закройте пробирку пробкой с газоотводной трубкой.
5. Наденьте на кончик трубки еще одну пробирку. В связи с тем, что кислород — газ тяжелее воздуха, для его собирания можно использовать метод вытеснения воздуха.
6. Подождите некоторое время, чтобы пробирка заполнилась выделяющимся газом.
7. Наличие кислорода проверьте, внося тлеющую лучинку в пробирку-приемник. Наблюдается яркая вспышка и горение лучинки.
8. Сделайте вывод согласно цели занятия.
Вопросы и задания.
А). Что происходит при взаимодействии перекиси водорода с оксидом марганца (IV)? Составьте молекулярное уравнение реакции.
Б). Опишите физические свойства кислорода, непосредственно наблюдаемые в опыте.
В). Опишите, как вы распознавали кислород.
Г). При оформлении протокола укажите дату занятия, название и цель практического занятия, оборудование и реактивы.
Д). Баллоны, предназначенные для хранения и транспортировки газов, окрашиваются эмалевой, масляной или алюминиевой краской и отличаются по цвету. Какие цвета используют при маркировке баллонов, заправленных кислородом?
|
|
|
Е). Какие последствия может вызвать аварийная разгерметизация кислородного баллона?
Ж). Предложите меры, которые необходимо предпринять для тушения веществ в атмосфере, обогащенной кислородом.
Опыт 2. Получение, собирание и распознавание водорода.
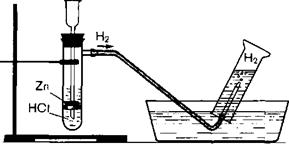
|
| Рис.3. Установка для получения и собирания водорода |
1. Соберите прибор для получения газов и проверьте его на герметичность.
2. В пробирку положите 1—2 гранулы цинка.
3. Прилейте в нее 1—2 мл соляной кислоты.
4. Закройте пробирку пробкой с газоотводной трубкой.
5. Наденьте на кончик трубки еще одну пробирку.
6. Подождите некоторое время, чтобы пробирка заполнилась выделяющимся газом.
7. Снимите пробирку с водородом и, не переворачивая ее, поднесите к горящей спиртовке. Если водород взрывается с глухим хлопком, то он чистый, а если с «лающим» звуком, значит, водород собран в смеси с воздухом («гремучий газ»).
Вопросы и задания.
1. Что происходит при взаимодействии цинка с соляной кислотой? Составьте уравнение реакции и дайте ее характеристику по всем изученным признакам классификации химических реакций.
2. Рассмотрите записанную реакцию с точки зрения процессов окисления-восстановления.
3. Опишите физические свойства водорода, непосредственно наблюдаемые при проведении опыта.
4. Опишите, как можно распознать водород.
Дата добавления: 2020-12-22; просмотров: 244; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!
