Арнольд Л.В., Михайловский Г.А., Селиверстов В.М. Техническая термодинамика и теплопередача, М, Высшая школа, 1979, - 446 с.
2. А.Ф. Гогин Судовые дизели, М. Транспорт, 1988.
Интернет-ресурсы:
1.Электронный ресурс «Измерительный инструмент» - Режим доступа: http://www.chelzavod.ru/.
2.Электронный ресурс «Мега Слесарь» - Режим доступа: http://www.megaslesar.ru/.
3.Электронный ресурс «Понятия о допусках и посадках основные термины» - Режим доступа: http://cxt.telesort.ru/vdovichenkovaucheb/Dopuski.htm.
4.Электронные ресурсы «Теоретические основы теплотехники», форма доступа: http://03-ts.r.
5.Электронный ресурс «Материаловедение» - Режим доступа: http://www.materialcince.ru.
Пример выполнения работы:
Задача №1. Сернистый газ (SO2) объемом V1=20 м3 сжимают при постоянной температуре Т=317 К от давления р1=3 кПа до давления р2=300 кПа.
Определить: а) параметры состояния в начале и конце процесса;
б) работу, затраченную на сжатие;
в) количество тепла в процессе;
г) изменение внутренней энергии.
Построить процесс в pV-диаграмме.
Решение:
1) Конечный объем газа находим из соотношения между параметрами в изотермическом процессе (T=const)
 м3.
м3.
2) Газовая постоянная SO2
 Дж/(кг·К).
Дж/(кг·К).
3) Масса газа
 кг.
кг.
4) Работа, затраченная на сжатие
 Дж.
Дж.
5) Количество тепла в процессе
Т.к. процесс изотермический, изменение внутренней энергии ΔU=0, и по первому з-ну термодинамики Q=L=-277077.4 Дж.
6) по известным значениям р1, р2, V1 и V2 строим в масштабе процесс в pV-диаграмме.
Задача №2. В баллоне объемом V=0,5 м3 находится кислород (О2) под давлением р1=10 кПа и температуре t1=17 °С. Газ нагревают при постоянном объеме до давления р2=20 кПа.
|
|
|
Определить: 1) сколько тепла сообщено газу;
2) до какой температуры нагрелся кислород;
3) работу, совершенную газом;
4) изменение внутренней энергии.
Построить процесс в pV-диаграмме.
Решение:
1) Конечная температура газа в изохорном процессе определяется из соотношения параметров

2) Газовая постоянная кислорода
 Дж/(кг·К).
Дж/(кг·К).
3) Масса кислорода
 кг.
кг.
4) Массовая изохорная теплоемкость кислорода определяется по таблицам теплоемкостей при средней температуре процесса tср=(t1+t2)/2=(17+307)/2=162 °С.
 =0,6915 кДж/(кг·К).
=0,6915 кДж/(кг·К).
5) Количество тепла в процессе
 кДж.
кДж.
6) В изохорном процессе работа сжатия L=0, т.к. объем постоянный. Отсюда по 1-му з-ну термодинамики  кДж.
кДж.
7) по известным значениям р1, р2, V строим в масштабе процесс в pV-диаграмме.
Задача №3. В цилиндре с поршнем, под постоянным давлением 4 бар, находится воздух при температуре t1=500 °C. От воздуха отводится тепло таким образом, что в конце процесса устанавливается температура t2=100 °C. Объем цилиндра, в котором находится воздух, 200 л.
Определить количество отнятого тепла, конечный объем, изменение внутренней энергии и совершенную над газом работу сжатия.
|
|
|
Решение:
1) выполняем перевод внесистемных единиц измерения в единицы системы СИ: р=4 бар=4·105 Па; V1=200 л=0,2 м3.
2) Конечный объем в изобарном процессе определяем по з-ну Гей-Люссака:
 м3.
м3.
3) Газовая постоянная воздуха
 Дж/(кг·К).
Дж/(кг·К).
4) Масса воздуха
 кг.
кг.
5) Массовая изобарная теплоемкость воздуха определяется по таблицам теплоемкостей при средней температуре процесса tср=(t1+t2)/2=(100+500)/2=300 °С.
 =1,0191 кДж/(кг·К).
=1,0191 кДж/(кг·К).
6) Количество тепла в процессе
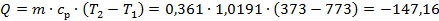 кДж.
кДж.
7) Работа сжатия

8) Изменение внутренней энергии определим из 1-го з-на термодинамики
 кДж.
кДж.
Задача №4. m=10 кг азота, параметры которого р1=1,2 бар, t1=30 °С, сжимаются, причем объем уменьшается в 2.5 раза.
Найти начальные и конечные параметры, количество тепла в процессе, работу и изменение внутренней энергии, если сжатие происходит: а) по адиабате с показателем адиабаты k=1.4; б) по политропе с показателем политропы m=1.2.
Построить процессы сжатия в pV-диаграмме.
Решение:
I. Расчет адиабатного процесса.
1) Выполняем перевод внесистемных единиц измерения в единицы системы СИ: р=1.2 бар=1,2·105 Па; Т1=30+273=303 К.
2) Газовая постоянная азота
 Дж/(кг·К).
Дж/(кг·К).
3) Начальный объем определяем по уравнению состояния
|
|
|
 м3.
м3.
4) Конечный объем
 м3
м3
5) Конечное давление
 Па.
Па.
6) Конечная температура определяется из уравнения состояния для точки 2 окончания процесса
 .
.
7) Количество тепла в процессе Q=0, т.к. процесс адиабатный.
8) Работа сжатия
 Дж.
Дж.
9) Изменение внутренней энергии по 1-му з-ну термодинамики
 Дж.
Дж.
II. Расчет политропного процесса.
Пп.1 – 4 такие же, как и в адиабатном процессе.
5) Конечное давление
 Па.
Па.
6)Конечная температура определяется из уравнения состояния для точки 2 окончания процесса
 .
.
7)Работа сжатия
 Дж.
Дж.
8)массовая изохорная теплоемкость азота определяется по таблице при средней температуре процесса tср=(t1+t2)/2=(30+91)/2=61.5 °C.
 кДж/(кг·К).
кДж/(кг·К).
9)Изменение внутренней энергии
 кДж.
кДж.
10) Количество тепла определим по 1-му з-ну термодинамики
 кДж.
кДж.
11) По рассчитанным значениям параметров состояния строятся процессы в pV-диаграмме.
Дата добавления: 2020-04-25; просмотров: 379; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!
