Буферные системы плазмы крови, их относительный вклад в поддержании кислотно-основного гомеостаза.
В плазме крови человека поддерживается приблизительно постоянное значение рН, равное ~7,4 за счет действия карбонатной, фосфатной, белковой, гемоглобин-оксигемоглобиновой буферных систем.
Карбонатная буферная система способна поддерживать значение рН≈7,4,физиологического буферного раствора. Ее буферная емкость вплазме крови по кислоте равно ~ 40ммоль, по щелочи – около 1-2ммоль.
Фосфатная буферная система способна поддерживать постоянное значение рН в биологических жидкостях в интервале значение рН=6,2-8,2. Ее буферная емкость в плазме крови составляет около 1-2ммоль по кислоте, по щелочи – около 0,5 ммоль.
Белковая буферная система в плазме крови содержит при рН≈7,4. Ее буферная емкость по кислоте составляет около 3-10 ммоль.
Буферные системы плазмы крови - гидрокарбонат=35%, белковая=7%, фосфатная=1%, всего =43%
РН внутренней среды эритроцитов. Буферные системы эритроцитов.
Во внутренней среде эритроцитов в норме поддерживается постоянное рН, равное 7,25 за счет действия карбонатной, фосфатной, белковой, гемоглобин-оксигемоглобиновой систем. Последняя система одновременно играет роль буферной окислительно-восстановительной системы, участвуя в процессах переноса кислорода и удаления диоксида углерода.
Гемоглобин,оксигемоглобиновая =35%, гидрокарбонатная=18%, фосфатная=4%,всего= 57%
Механизм действия гидрокарбонатного буфера в условиях организма. Уравнение Гендерсона-Гассельбаха.
|
|
|
Наибольшее значение для поддержания рН межклеточной жидкости и плазмы крови имеет бикарбонатная буферная система. Угольная кислота в плазме и межклеточной жидкости присутствует в четырех формах: физически растворенного углекислого газа (СО2), угольной кислоты (Н2СО,), аниона карбоната (СО32-) и аниона бикарбоната (НСО3). В условиях физиологического диапазона рН больше всего содержание бикарбоната, примерно в 20 раз меньше содержание растворенного углекислого газа и угольной кислоты, а ион карбоната практически отсутствует. Бикарбонат представлен в виде натриевых и калиевых солей. Как уже указывалось выше, константа диссоциации (К) есть отношение:

| а для бикарбоната | 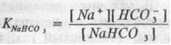
|
Анион НСО3 является общим как для кислоты, так и для соли, а соль диссоциирует сильнее, поэтому этот анион, образуясь из бикарбоната, будет подавлять диссоциацию угольной кислоты, т.е. практически все количество аниона НСО3 в бикарбонатном буфере происходит из NaHCO3. Следовательно:
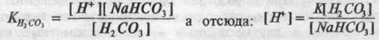
(формула Гендерсона, где К — константа диссоциации угольной кислоты). В связи с использованием отрицательного логарифма концентрации, формула, названная уравнением Гендерсона-Гассгльбаха, для бикарбонатного буфера приняла выражение:
|
|
|
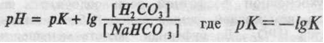
При физиологических значениях рН отношение концентрации углекислоты к бикарбонату составляет 1/20
В условиях взаимодействия бикарбонатного буфера с кислотами происходит их нейтрализация с образованием слабой угольной кислоты. Углекислый газ, появляющийся при ее разложении с помощью карбоангибразы, удаляется через легкие. Избыток оснований, взаимодействуя с бикарбонатным буфером, связывается с угольной кислотой и приводит в конченом счете к образованию бикарбоната, излишки которого удаляются, в свою очередь, из крови через почки.
?16. Значение гидрокарбонатного буфера для различных сред организма. Соотношение компонентов буфера в плазме крови и в эритроцитах. Сравнительная емкость по кислоте и по щелочи.
Главное назначение гидрокарбонатного буфера заключается в нейтрализации кислот. Он является системой быстрого и эффективного реагирования, так как продукт его взаимодействия с кислотами - углекислый газ - быстро выводится через легкие.
Относительный вклад в плазме 35%,в эритроцитах 18%.
При физиологических значениях рН отношение концентрации углекислоты к бикарбонату составляет 1/20. Т. к. рН внутри эритроцитов 7,25, то соотношение концентраций соли (НСО3-) и кислоты (Н2СО3) здесь несколько меньше, чем в плазме крови.
Ее буферная емкость в плазме крови составляет около 1-2ммоль по кислоте, по щелочи – около 0,5 ммоль. В эритроцитах????
|
|
|
?17. Роль дыхания в поддержании кислотно-основного гомеостаза.
Система дыхания играет значительную роль в поддержании кислотно-щелочного баланса организма, однако для нивелирования сдвига рН крови им требуется 1–3 минуты. Роль легких сводится к поддержанию нормальной концентрации углекислоты, и основным показателем функционального состояния легких является парциальное напряжение углекислого газа в крови. Легочные механизмы обеспечивают временную компенсацию, так как при этом происходит смещение кривой диссоциации оксигемоглобина влево и уменьшается кислородная емкость артериальной крови.
При устойчивом состоянии газообмена легкие выводят углекислого газа около 850 г в сутки. Если напряжение углекислого газа в крови повышается сверх нормы на 10 мм рт. ст., вентиляция увеличивается в 4 раза.
?18. Механизм действия гемоглобин-оксигемоглобинового буфера.
Гемоглобиновый буфер является самой емкой буферной системой. На ее долю приходится до 75 % всей буферной емкости крови. Свойства буферной системы гемоглобину придает главным образом его способность постоянно находиться в виде двух форм – восстановленного (редуцированного) гемоглобина ННb и окисленного (оксигемоглобина) НbО2.
|
|
|
Гемоглобиновый буфер, в отличие от бикарбонатного, в состоянии нейтрализовать как нелетучие, так и летучие кислоты. Окисленный гемоглобин ведёт себя как кислота, увеличивая концентрацию ионов водорода, а восстановленный (дезоксигенированный) – как основание, нейтрализуя H+.
Гемоглобин является классическим примером белкового буфера и эффективность его достаточно высока. Гемоглобин в шесть раз более эффективен как буфер, чем плазменные протеины.
Переход окисленной формы гемоглобина в восстановленную форму предупреждает сдвиг рН в кислую сторону во время контакта крови с тканями, а образование оксигемоглобина в легочных капиллярах предотвращает сдвиг рН в щелочную сторону за счет выхода из эритроцитов СО2 и иона хлора и образования в них бикарбоната.
Дата добавления: 2020-04-25; просмотров: 1743; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!
