Интенсификация процессов, основанных на необратимых реакциях
Строго говоря, все реакции являются обратимыми. К практически необратимым реакциям можно отнести те, которые характеризуются большой величиной константы равновесия. Можно принять, что они протекают только в прямом направлении. При разработке технологии проведения процесса, основанного на необратимых реакциях, преследуют две основные цели: повышение скорости реакции и выхода целевого продукта. Ускорить необратимую реакцию возможно за счет увеличения начальных концентраций реагентов и путем повышения температуры процесса. Но главным способом ускорения необратимой реакии является правильный подбор катализатора процесса. Выход продукта в таких процессах пропорционален степени превращения сырья.
При разработке технологии проведения сложной необратимой реакции большое внимание уделяют повышению селективности процесса. Эта цель достигается подбором оптимальных концентраций реагентов и температур, а также подбором наиболее селективных катализаторов.
Селективность S реакции можно оценить соотношением скоростей основной и побочной реакций:
S = V1 / V2 =k1CAa / k2CAb = k CAa – b ,
где k = k1 / k2 .
На основе данного уравнения можно сделать выводы о влиянии концентрации на селективность:
– при a > b (порядок целевой реакции выше побочной) селективность пропорциональна максимальному значению концентрации;
– при a < b селективность пропорциональна минимальным значениям концентрации;
– при a = b концентрация не влияет на селективность: S = kCA0 = k.
Катализ – наиболее сильное воздействие на селективность реакции. Катализ – сложная система реакций, при которых снижаются многие затруднения в протекании реакции по сравнению с некатализируемым процессом. Этот эффект связан с понижением энергии активации и/или увеличением предэкспоненциального множителя в кинетическом уравнении реакции.
Интенсификация процессов, основанных на обратимых реакциях
К обратимым относят реакции, протекающие одновременно в прямом и обратном направлениях.
В обратимой реакции aA + bB = dD в соответствии с законом действующих масс, скорости прямой и обратной реакций будут следующие:
Vпр = k/ CAa CBb ;
Vоб = k// CDd,
где С – концентрация;
k / , k// – константы скорости прямой и обратной реакций;
a , b, d – стехиометрические коэффициенты (порядки реакции) при участниках процесса A, B, D.
Суммарная скорость обратимой реакции равна разности скоростей прямой и обратной реакций: V = Vпр – Vобр. В момент равновесия Vпр = Vобр и
CDd / CAa CBb = k/ / k// = K р ,
где КР – константа равновесия.
Степень превращения, при которой устанавливается равновесие, называют равновесной. В производственных условиях систему не доводят до состояния равновесия, т.к. в этом состоянии производительность реактора равна нулю. Реактор работает в режиме, удаленном в большей или меньшей степени от состояния равновесия.
Существуют реакции с легко смещаемым равновесием и с неблагоприятным положением равновесия, для которых приемлемая конверсия может составлять 30 % и даже меньше.
Смещение равновесия при изменении давления, температуры, концентрации подчиняется принципу Ле-Шателье:
внешнее воздействие на систему с установившимся равновесием смещает его в сторону уменьшения этого воздействия.
В качестве примера действия принципа Ле-Шателье рассмотрим реакцию синтеза аммиака: 3Н2 + N2 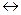 2NH3. Эта реакция – простая обратимая, экзотермическая, протекающая с уменьшением объема. Увеличение концентрации одного из реагентов приведет к возрастанию скорости прямой реакции, т.е. в сторону образования целевого продукта. В этом случае движущей силой процесса является величина внешнего воздействия.
2NH3. Эта реакция – простая обратимая, экзотермическая, протекающая с уменьшением объема. Увеличение концентрации одного из реагентов приведет к возрастанию скорости прямой реакции, т.е. в сторону образования целевого продукта. В этом случае движущей силой процесса является величина внешнего воздействия.
Такой же эффект можно получить при увеличении давления в системе. Действительно, повышая давление, мы увеличиваем концентрацию всех участников процесса, но увеличение концентрации реагентов будет более значительным, т.к. число молей исходных веществ больше, чем продуктов реакции. Движущей силой этого процесса является разность объемов конечных и исходных продуктов. Поэтому, в случае равенства объемов конечных и исходных продуктов, сместить равновесие путем изменения давления в системе невозможно.
Влияние изменения температуры на смещение равновесия в данной реакции таково. Поскольку реакция экзотермическая, то сместить равновесие в направлении образования аммиака возможно путем понижения температуры процесса. Движущей силой в этом случае является абсолютная величина такого изменения температуры.
Принцип Ле-Шателье позволяет качественно оценить влияние основных параметров процесса на направление протекания обратимой химической реакции. Количественную оценку на смещение равновесия при изменении температуры или саму возможность протекания данной реакции при посто-янном давлении (а именно при постоянном давлении в промышленных химико-технологических процессах, как правило, ведут химические реакции) можно, если известны знак и величина изменения в этом процессе свободной энергии Гиббса:
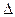 G = ∑Gкон. – ∑ Gнач.,
G = ∑Gкон. – ∑ Gнач.,
где ΔGнач. иΔGкон. – значения свободной энергии Гиббса реагентов и продуктов процесса соответственно.
Отрицательное значение этой разности означает принципиальную возможность протекания реакции в прямом направлении. Чем больше абсолютная величина этой разности, тем больше движущая сила процесса.
Как известно
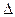 G =
G = 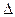 H – T
H – T 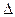 S,
S,
где 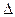 H = Hкон. – Hнач. – изменение энтальпии;
H = Hкон. – Hнач. – изменение энтальпии;
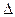 S = Sкон. – Sнач. – изменение энтропии;
S = Sкон. – Sнач. – изменение энтропии;
Ннач . , Нкон., Sнач., Sкон. – состояния системы, отвечающие начальным и конечным значениям энтальпии и энтропии соответственно.
В соответствии с этим уравнением значение и знак 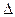 G определяется значениями
G определяется значениями 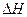 ,
, 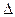 S, и T.
S, и T.
Согласно первому закону термодинамики:
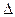 Н =
Н = 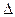 U – P
U – P 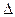 V,
V,
где 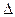 U – изменение внутренней энергии;
U – изменение внутренней энергии;
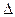 V – изменение объема при Р = соnst.
V – изменение объема при Р = соnst.
В рассматриваемых условиях 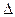 Н равна по абсолютной величине, но противоположна по знаку тепловому эффекту реакции Q (Q = –
Н равна по абсолютной величине, но противоположна по знаку тепловому эффекту реакции Q (Q = –  H).
H).
Изменение энтропии в первом приближении можно оценить, если учесть, что ее можно рассматривать как меру беспорядка системы. Процессы, протекающие с его возрастанием (расширение газа, растворение, испарение, плавление, реакции разложения), т.е. с увеличением объема, характеризуются возрастанием энтропии. Процессам, протекающим с уменьшением беспорядка (конденсация, кристаллизация, реакции присоединения, комплексообразования), соответствует уменьшение энтропии.
При выборе оптимальных параметров ведения технологического процесса в случае обратимых реакций, кроме термодинамических закономерностей следует учитывать и особенности процессов, связанных с их кинетикой. Характер влияния температуры на скорость и положение равновесия для обратимых экзо- и эндотермических реакций различен.
Для обратимой экзотермической реакции при малых степенях превращения, когда концентрация исходных продуктов в реакционной массе достаточно велика, а концентрация продуктов реакции мала, обратимая реакция протекает, как необратимая. Поэтому с повышением температуры ее скорость возрастает. По мере увеличения концентрации конечных продуктов и снижения концентрации исходных продуктов, разность скоростей между прямой и обратной реакциями сокращается, и в момент, когда скорости сравняются, наступает равновесие. При этом технологический процесс прекращается. Чтобы этого не происходило, в непрерывных химико-технологических процессах при стационарном режиме осуществляется непрерывная подача свежего сырья и непрерывный вывод продуктов процесса.
В обратимой эндотермической реакции с увеличением температуры скорость прямой реакции возрастает быстрее чем обратной. При этом возрастает и разность скоростей между прямой и обратной реакциями. На основе изложенного можно обосновать выбор температурного режима химико-технологического процесса для обратимых реакций.
1. Поскольку в случае обратимой эндотермической реакции повышение температуры положительно влияет на оба критерия оптимизации (на скорость и смещение равновесия), такую реакцию лучше проводить при постоянной повышенной температуре.
2. Неоднозначное влияние температуры на критерии оптимизации обратимой экзотермической реакции требует использования режима понижающейся температуры: начинают процесс при более высокой температуре, а затем ее снижают по линии оптимальных температур. Такой прием применим для периодических процессов. В непрерывных процессах поддерживают постоянную температуру, т.к. нет явления накопления конечных продуктов и невозобновляемого расхода исходного сырья.
Дата добавления: 2019-11-25; просмотров: 563; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!
