Расчёт температуры горения с использованием средних значений теплоёмкостей
Пример 1. Рассчитать действительную температуру горения вещества сложного состава, состоящего из 40 % углерода, 20 % водорода, 30 % азота, 10 % влаги. Горение протекает при коэффициенте избытка воздуха, равном 1,2, а потери тепла на излучение составляют 30 %.
Решение:
1. Рассчитаем низшую теплоту сгорания горючего вещества, используя формулу Д.И. Менделеева (см. формулу 27).
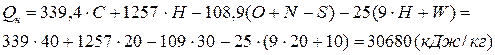
2. Рассчитаем объёмы продуктов горения при полном сгорании 1 кг горючего вещества сложного состава (см. формулы) (29-31).
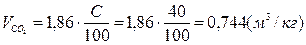 ;
;
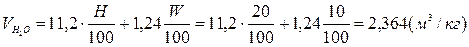 ;
;
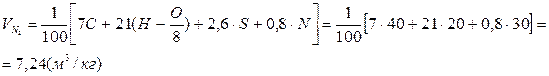
В связи с тем, что горение происходит при избытке воздуха, то в продуктах горения будет присутствовать избыточный воздух, который не участвовал в горении.
2. Рассчитаем избыточный объём воздуха при полном сгорании 1 кг горючего вещества (см. формулу 9).
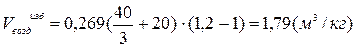
3. Рассчитаем температуру горения и, т.к. в условии задачи ничего не сказано о начальной температуре горения, будем считать, что горение протекает при нормальных условиях (см. формулу 33 и табл. 17):
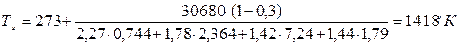
Ответ: действительная температура горения вещества сложного состава составила 1418 К.
Расчёт температуры горения методом последовательных приближений
Для более точных расчётов используют метод последовательных приближений по известной зависимости теплосодержания (энтальпии) продуктов горения от температуры.
Если теплосодержание продуктов горения при Т=273 К принять равным нулю, то полное теплосодержание продуктов горения при Тг будет равно количеству теплоты, выделившейся в результате химической реакции.
С учётом теплопотерь:
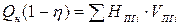 (34)
(34)
где 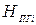 - теплосодержание (энтальпия) i-го продукта горения.
- теплосодержание (энтальпия) i-го продукта горения.
Задача состоит в том, чтобы найти температуру, при которой будет справедливо это равенство.
Пример 2. Найти адиабатную температуру горения этилового спирта в воздухе, если теплота его образования равна - 278,2 кДж/моль.
Решение. Адиабатную температуру горения вещества находят при условии отсутствия теплопотерь (h = 0), для стехиометрической смеси горючего с воздухом, т.е. при a = 1.
1. Для определение состава и объёма продуктов горения запишем уравнение химической реакции горения этилового спирта:
С2Н6О + 3(О2 + 3,76 N2) = 2 CО2 + 3 Н2О + 3 ×3,76 N2
2. Объём продуктов горения составляет: 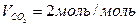 ;
; 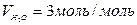 ;
; 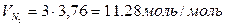 ; объём продуктов горения
; объём продуктов горения 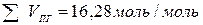 .
.
3. Рассчитаем низшую теплоту сгорания этилового спирта по следствию из закона Гесса:
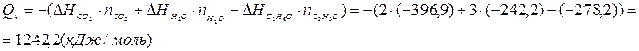
4. Так как теплопотери отсутствуют, то всё выделившееся тепло идёт на нагрев продуктов горения. Среднее теплосодержание 1 моля продуктов горения будет составлять:
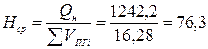 (кДж/моль)
(кДж/моль)
5. Воспользовавшись зависимостью теплосодержания газов от температуры (табл. VII приложения) , можно установить какой температуре соответствует такое теплосодержание. Лучше всего это сделать, ориентируясь на азот, так как его больше всего в продуктах горения. Из табл. VII видно, что при температуре 2200°С теплосодержание азота 74,1 кДж/моль. Уточним, сколько потребовалось бы тепла, чтобы нагреть продукты горения до такой температуры. При Т1 = 2200 °С
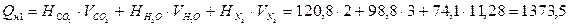
(кДж/моль)
Но это больше, чем выделилось тепла в результате реакции горения 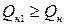 , поэтому можно сказать, что температура горения меньше, чем 2200 °С. Определим, сколько потребуется тепла для нагревания продуктов горения до 2100 °С.
, поэтому можно сказать, что температура горения меньше, чем 2200 °С. Определим, сколько потребуется тепла для нагревания продуктов горения до 2100 °С.
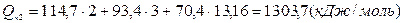
Но и 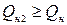 , значит Тг < 2100°С
, значит Тг < 2100°С
При температуре 2000°С
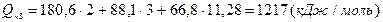
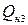 уже меньше, чем
уже меньше, чем 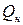 , из этого можно сделать вывод, что температура горения этанола имеет значение между 2000 и 2100°С. Уточним эту температуру линейной интерполяцией между двумя этими ближайшими значениями:
, из этого можно сделать вывод, что температура горения этанола имеет значение между 2000 и 2100°С. Уточним эту температуру линейной интерполяцией между двумя этими ближайшими значениями:
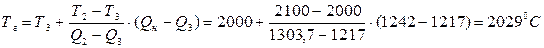
или 2302 К
Ответ: адиабатическая температура горения этанола составила 2302 К
Дата добавления: 2019-09-08; просмотров: 922; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!
