Современная классификация ферментов и их номенклатура
Согласно классификации, разработанной Международной комиссией по ферментам (1961г.) все ферменты делят на шесть классов. Классы делятся на подклассы, а последние – на подподклассы, внутри которых ферменту присваивается свой порядковый номер. Например, ЛДГ имеет шифр. 1.1.1.27. 1- название класса – оксидоредуктазы – указывает тип ферментной реакции; 2-я цифра показывает номер подкласса; подкласс уточняет действие фермента, так как указывает в общих чертах на природу химической группы S. Подподкласс – уточняет природу атакуемой химической связи S или природу акцептора. № 27 – порядковый № ЛДГ в подподклассе.
1) Оксидоредуктазы – катализируют реакции окисления-восстановления – содержат 17 подклассов и ~ 480 Е. Например: ЛДГ.
2) Трансферазы – катализируют реакции переноса различных групп от одного S (донор) к другому (акцептор). 8 подклассов в зависимости от вида переносимых групп и ~ 500 Е. Например: фермент холинацетилтрансфераза – катализирует перенос остатка уксусной кислоты на холин ® ацетилхолин.
3) Гидролазы – катализируют разрыв связей в S с присоединением воды. Содержат 11 подклассов и ~ 460 Е. К гидролазам относятся пищеварительные ферменты, а также ферменты, входящие в состав лизосом и других органоидов клетки, где они способствуют распаду крупных молекул на более мелкие.
4) Лиазы – катализируют реакции разрыва связей в S без присоединения воды или окисления. Содержат 4 подкласса и ~ 230 Е – участвуют в промежуточных реакциях синтеза (синтазы) или распада (дегидратазы).
|
|
|
5) Изомеразы – катализируют превращение изомеров друг в друга. От типа реакции изомеризации – различают мутазы (рацемазы). Содержат 5 подклассов и ~ 80 Е.
6) Лигазы (синтетазы) – катализируют реакции соединения двух молекул S с использованием Е фосфатных связей. Источником ферментов является АТФ и др. Содержат 5 подклассов, ~ 80 Е (например, гексокиназа, фосфофруктокиназа).
Номенклатура ферментов.
Существует два типа названий ферментов:
1) рабочее, или тривиальное;
2) систематическое.
Рабочее название – название S + тип реакции + окончание аза. Лактат + реакция дегидрогенизации + аза ®ЛДГ.
Для некоторых ферментов оставлены их рабочие названия: пепсин, трипсин и т.д.
Систематическое название – название обоих S + тип реакции + аза.
a-Лактат (S1): НАД+ (S2) – оксидоредуктаза.
Систематическое название дается только тем ферментам, структура которых полностью изучена. В одной клетке находится ~ 104 молекул ферментов, катализируется ~ 2000 разных реакций. В настоящее время известно около 1800 ферментов, в кристаллическом виде получено ~ 150 ферментов.
Общие представления о катализе
|
|
|
Вероятность протекания химической реакции определяется разницей между свободной Е исходных веществ и свободной Е продуктов реакции. Ферменты ускоряют химические реакции за счет энергии активации – Еа.
Еа – это дополнительная энергия, необходимая для перевода всех молекул одного вещества в активное состояние при данной температуре. (Аррениус – понятие об Еа).
Таким образом, Vфр зависит от энергетического барьера, который необходимо преодолеть реагирующим веществам, причем высота этого барьера неодинакова для различных реакций.
Чем выше энергия активации, тем медленнее протекает реакция. Ea не виляет на изменение свободных ферментов исходных веществ и продуктов реакции, то есть ∆G, то есть энергетическая возможность реакции не зависит от фермента.
Фермент понижает Ea (пик 2), то есть снижает высоту барьера в результате чего возрастает доля реакционноспособных молекул, а, следовательно, увеличивается Vфр. Чем больше снижается Ea, тем эффективнее действует катализатор и тем больше ускоряется реакция.
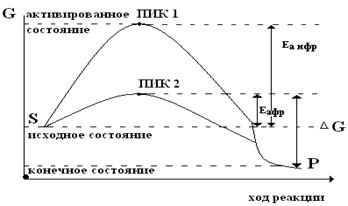
| S - исходный субстрат P – конечный продукт ΔG – стандартное изменение свободной энергии Еа нфр – энергия активации неферментативной реакции Еа фр – энергия активации ферментативной реакции |
Механизм действия ферментов
|
|
|
Большую роль в развитии представлений о механизме действия ферментов сыграли классические работы Михаэлиса и Ментен, которые развили положения о Е-S-х комплексах. Согласно их представлениям (1915г.), ферменты обратимо соединяются со своим S, образуя нестойкий промежуточный продукт – Е-S-комплекс, 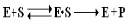 который в конце реакции распадается на ферменты и продукты реакции (Р). Фактически в природе идет ступенчатое превращение S через целый ряд промежуточных реакций: ES1→ ES2→ ES3 … → E + P. Схематически преобразование S в Р можно представить таким образом:
который в конце реакции распадается на ферменты и продукты реакции (Р). Фактически в природе идет ступенчатое превращение S через целый ряд промежуточных реакций: ES1→ ES2→ ES3 … → E + P. Схематически преобразование S в Р можно представить таким образом:
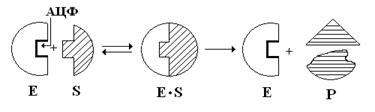
АЦФ, как правило, располагается в глубине молекулы Е.
Математическая обработка реакции образование ЕS-комплекса позволила вывести уравнение, которое называется уравнением Михаэлиса-Ментен:
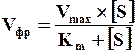
где Vфр – наблюдаемая скорость фр;
Vmax – максимальная скорость фр при неполном насыщении фермента S-том;
[S] – концентрация S;
Км – константа Михаэлиса-Ментен.
Графически уравнение Михаэлиса-Ментен имеет следующий вид:
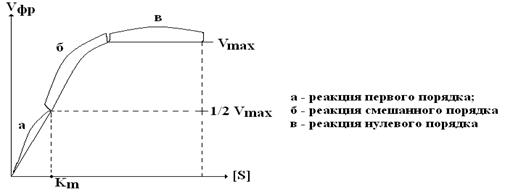
При низкой [S] Vфр прямо пропорциональна [S] в каждый данный момент времени (реакция 1-го порядка).
|
|
|
Из уравнения Михаэлиса-Ментен также следует, что при низком значении Км и высоком значении [S] Vфр является максимальной (в) и не зависит от [S] – это реакция нулевого порядка. Реакция нулевого порядка соответствует явлению, которое называется полным насыщением фермента субстратом.
Гипербола, выражающая зависимость Vфр от [S], называется кривой Михаэлиса. Чтобы правильно определить активность ферментов, нужно добиться реакции нулевого порядка, то есть определять Vфр при насыщающих концентрациях S.
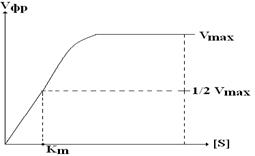
| Км численно равна [S] (моль(л)), при которой V реакции равна половине от максимальной. Для определения численного значения Км находят ту [S], при которой Vфр составляет от ½ от Vmax. Таким образом, определение Км играет важную роль для выяснения МД модификаторов на активность фермента. |
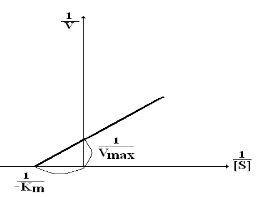
| Иногда график строят методом двойных обратных величин – метод Лайнуивера-Бэрка: Значение как Vmax, так и Км более точно определяется методом двойных обратных величин. |
ЛЕКЦИЯ 7
Дата добавления: 2019-07-15; просмотров: 208; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!
