Образование комплексов с переходными металлами
Высокое сродство молекул C60 и C70 к электрону проявляется в склонности к образованию комплексов с пеходными металлами. Изучение кристаллической структуры получающихся соединений привело к выводу, что процесс комплексообразования переходных металлов с фуллереновым ядром по сути такой же, как и хорошо известная реакция комплексообразования с электронодифицитными алкенами.
 |
Так, при взаимодействии ди(трифенилфосфин)платины с этиленом (представляющим собой плоскую молекулу) образуется комплекс, сокращенно обозначаемом (Ph3P)2Pt(h2-C2H4), в котором атомы водорода в молекуле этилена более не лежат в плоскости, а отклонены на угол q , что является мерой прочности донорно-акцепторных связей. Такое изменение конфигурации заместителей усиливается при наличии в молекуле этилена более электроноакцепторных заместителей, чем водород. С раствором фуллерена-60 в толуоле (Ph3P)2Pt(h2-C2H4) образует окрашенный в изумрудно-зеленый цвет комплекс (Ph3P)2Pt(h2-C60).
 |
Интересно, что образование комплекса, включающего шесть атомов платины, и соответственно имеющего на 6 двойных связей меньше, чем исходный фуллерен, увеличивает степень делокализации электронов в оставшихся бензольных кольцах. Иными словами, образовавшаяся структура имеет более ароматический характер, чем сам фуллерен-60. Проявлением этого является уравнивание длин углерод-углеродных связей в восьми шестиугольниках:
|
|
|
 |
Нуклеофильное присоединение
Проявление молекулой C60 окислительный свойств по отношению к щелочным металлам, как было показано ниже, указывает на то, что фуллерен является электронодифицитной молекулой. Рассмотрение же химического строения молекулы представляет фуллерен скорее как сопряженный полиен, в составе могут быть выделены фрагменты структуры искаженного [5]-радиалена и циклогексатриена, чем как “сверхароматическое” соединение. Характерной реакцией такого полиена оказывается нуклеофильное присоединение. Уникальность фуллерена в этом случае заключается в исключительном разнообразии образующихся продуктов, что создает большие трудности для выделения их в чистом виде.
 |
Фуллерен-60 легко взаимодействует с литийорганическими соединениями и реактивами Гриньяра, образуя в качестве первичных интермедиатов анионы RC60-. Процесс проходит очень быстро; например, в толуоле осадок солей выпадает практически мгновенно:
Дальнейшая обработка, например, раствором хлороводорода в метаноле позволяет получить производные гидрофуллеренов, а йодистым метилом - метилфуллеренов:
 |
Сродство фуллерена к С-нуклеофилам может проявляться в возможности получения полимеров C60. Такие фуллерены (Рисунок 4) представляют интерес по следующим соображениям: 1) свойства полимера сочетаются со свойствами фуллерена, 2) при соответствующем подборе мономеров они могут образовывать плотные мономолекулярные пленки, проявлять устойчивость к растворителям и быть неплавкими, а также 3) обладать необычными электрическими, оптическими и каталитическими свойствами.
|
|
|
Рисунок 4. Четыре прототипа полимеров, включающие структурную единицу C60: а) прикрепленные к цепи, б) прикрепленные к поверхности (привитые), в) дендритные (ветвящиеся), г) цепочечные.
 |
Одним из способов получения, например, привитых полимеров, может служить следующая схема (в качестве основы использована полиэтиленовая пленка с поверхностными дифенилметильными группами):
Стабилизация активных интермедиатов RC60- может быть осуществлена путем внутримолекулярного нуклеофильного замещения (SNi), если R представляет собой уходящую группу. Как показал Бингель, при взаимодействии с a -галогенэфирами и a -галогенкетонами осуществляется гладкое циклопропанирование фуллерена, например, реакция с броммалоновым эфиром (диэтилброммалонатом) с участием гидрида натрия в толуоле осуществляется при комнатной температуре, причем моноаддукт может быть
 |
выделен хроматографией на колонке:
|
|
|
 |
В тех же условиях возможно образование бис-аддукта, то есть вещества, в составе которого содержатся два циклопропановых кольца. Для фуллерена-60 изомеров такого вида будет восемь, из которых преобладает следующий:

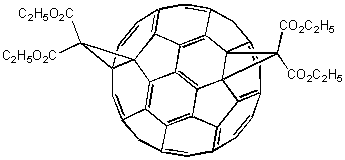 |
Интересно, что C70 в этих условиях взаимодействует быстрее, чем C60, что позволяет судить о ходе реакции по окраске раствора: раствор C60 окрашен в красно-фиолетовый цвет, а C70 - в винно-красный.
 |  | ||
Реакции присоединения
Реакции циклоприсоединения
При реакциях циклоприсоединения активную роль всегда играют двойные связи шестичленного кольца, выступая как в качестве диенов, так и диенофилов. Огромное количество циклоаддуктов, которые при этом можно получить, сильно способствовало повышению интереса исследователей к химии фуллеренов. Эта реакция оказалась мощным инструментом, позволяющим вводить в C60 практически любые функциональные группы, получая вещества, многие из которых выдерживают нагревание до 400 ° С без разложения.
 Наиболее типичными являются реакции Дильса-Альдера ([4+2]циклоприсоединение), в которых фуллерен выступает в качестве диенофила. В случае активных диенов характер устанавливающегося равновесия таков, что выход аддуктов весьма высок, а их очистка возможна методами жидкостной хроматографии с использованием толуола в качестве элюента:
Наиболее типичными являются реакции Дильса-Альдера ([4+2]циклоприсоединение), в которых фуллерен выступает в качестве диенофила. В случае активных диенов характер устанавливающегося равновесия таков, что выход аддуктов весьма высок, а их очистка возможна методами жидкостной хроматографии с использованием толуола в качестве элюента:
|
|
|
 |
Синтезированный по сходной схеме аддукт содержит электроноизбыточную диметоксифельную группу и электронодифицитный C60 в составе одной молекулы, что обусловливает внутримолекулярное донорно-акцепторное взаимодействие:
 |
Растворимость другого аддукта, полученного с использованием эфира бензо[18]краун-6, в полярных протонных растворителях, сильно зависит от концентрации ионов K+; это приводит к выводу, что эфирная группировка практически не взаимодействует с фуллереновой частью молекулы:
 Другим важным типом реакций циклоприсоединения является реакция с диазометаном ([3+2]циклоприсоединение), в ходе которого фуллерен ведет себя как 1,3-диполярофил. При обработке раствора C60 в толуоле диазометаном интермедиат (пиразолин) оказывается относительно устойчивым, как показал Вудль, и разлагается на смесь изомеров только под действием света:
Другим важным типом реакций циклоприсоединения является реакция с диазометаном ([3+2]циклоприсоединение), в ходе которого фуллерен ведет себя как 1,3-диполярофил. При обработке раствора C60 в толуоле диазометаном интермедиат (пиразолин) оказывается относительно устойчивым, как показал Вудль, и разлагается на смесь изомеров только под действием света:
 |
Выходы изомеров заметно отличаются; этот и другие подобные факты, а также теоретические расчеты, позволили придти к заключению, что для фуллерена C60, а также для его производных оказывается энергетически невыгодным образовывать двойные связи в месте соединения пяти- и шестичленных колец или уменьшать максимально возможное число [5]радиаленовых колец. Напомним, что в составеC60 имеется 12 [5]радиаленовых колец:
Реакции циклоприсоединения с замещенными фенилдиазометанами открывают широкие возможности для введения различных функциональных групп. При наличии нескольких диазогрупп (такие соединения легко могут быть синтезированы из кетонов через их гидразоны), избирательно реагирующих с фуллереном, могут быть получены соединения, образно названные “нитью жемчуга”:

Другим примером синтеза соединения с дифенилметановым мостиком является диметиловый эфир дифенола, получаемый с выходом 94% при комнатной температуре:
Дифенол, получаемый в результате гидролиза его простого эфира, оказался исключительно интересным исходным веществом для широкого круга синтезов, например, для получения полиуретана при взаимодействии с гексаметилендиизоцианатом:

а также для синтеза растворимого во многих органических растворителях светло-коричневого стеклообразного полимера, обладающего дендритной структурой:

Исключительно важными, наконец, являются реакции [2+2]циклоприсоединения; например, бензина к C60. Напомним, что термин “бензин” относится к открытому Дж.Робертсом в 1953 г интермедиату многих реакций ароматических соединений, формально содержащему тройную связь. Так, бензин, образовавшийся in situ путем диазотирования антраниловой кислоты, может присоединиться к C60 по связи между C-1 и C-2:
 |
Еще один интересный пример циклоприсоединения того же типа представляет фотохимическая полимеризация фуллерена, которая обратимо осуществляются при освещении видимым или ультрафиолетовым светом тонких (мономолекулярных) пленок C60, получающихся, к примеру, при выливании капли толуольного раствора на поверхность воды и последующем испарении растворителя:
|
 |
Наряду с димерами образуются и другие олигомеры, включая (C60)20. Интересно, что “межфуллереновые” углерод-углеродные связи имеют исключительную длину - более 2-х Е, а сферы оказываются слегка вытянутыми по отношению друг к другу (Рисунок 5).
 В заключение следует упомянуть еще об одном примере, [2+1]циклоприсоединении. Речь идет о реакции с фуллереном карбеновых частиц, генерируемых из производных диазирина. В приведенном ниже примере рассматривается образование в толуоле моноаддуктов с моносахаридом, гидроксильные группы которого защищены бензильными остатками:
В заключение следует упомянуть еще об одном примере, [2+1]циклоприсоединении. Речь идет о реакции с фуллереном карбеновых частиц, генерируемых из производных диазирина. В приведенном ниже примере рассматривается образование в толуоле моноаддуктов с моносахаридом, гидроксильные группы которого защищены бензильными остатками:
Конфигурация заместителей в аддукте сохраняется такой же, какой она была в исходной молекуле сахара; важно, что в реакции образуется только один энантиомер, а не смесь оптических изомеров.
Гидрирование
|
 |
С самого начала “эры фуллеренов” химиков, державших в руках молекулы содержащего двойные связи фуллерена, привлекала потенциальная возможность его гидрирования с образованием “фуллерана”. Однако задача оказалась значительно труднее, чем представлялось ранее, настолько, что полностью восстановленного фуллерена C60H60 не получено до сих пор. Исключительной нестойкостью обладают также не полностью восстановленные фуллерены, например, C60H36, что связано со значительной деформацией сферической формы молекулы. Как было показано в серии блестящих теоретических исследований, в молекуле “фуллерана” C60H60 часть атомов водорода должна оказаться внутри фуллереновой сферы, так как шестичленные кольца, подобно молекулам циклогексана, должны принять конформации “кресла” или “ванны”; именно невозможность сохранения сферы, пусть даже искаженной, обусловливает неуспех полного гидрирования и ту исключительную легкость, с которой образовавшиеся гидриды теряют водород.

Приводимая ниже таблица позволяет получить представление о различиях в энергиях молекулы, связанных в искажением валентных углов в молекуле C60H60, а также с другими факторами. Следует иметь в виду, что возможен только один “полностью экзо-” изомер и множество изомеров, содержащих часть атомов водорода внутри сферы. Расчеты выполнены с помощью программы Chem 3D Pro v.3.5 (Cambridge Soft).
| Изомер а | изомер б | |
| Заслонение соседних атомов водорода, кДж/моль | 483.8 | 905.8 |
| Искажение валентных углов, кДж/моль | 630.3 | 827.9 |
| Отталкивание 1,4-заместителей в циклогексановых кольцах, кДж/моль | 374.6 | 1027.7 |
| Общий запас энергии | 1556.5 | 2580.9 |
Вместе с тем гидриды с небольшим числом водородных атомов, такие как C60H2, C60H4, C70H2, получены и охарактеризованы.
 |
Прямое восстановление фуллерена водородом на активированном угле с рутением в качестве катализатора возможно только в жестких условиях (высокое давление и температура) по схеме:
Наибольшая достигнутая степень гидрирования соответствует C60H50 и C70H36, являющихся энергичными восстановителями.
Для получения ди- и тетрагидридов наиболее подходящими оказались методы гидроборирования (взаимодействие с бораном) и гидроцирконирования (восстановление дициклопентадиенилцирконийгидрохлоридом, имеющим сэндвич-структуру):

В случае фуллерена-60 получается единственный изомер, выделение которого методом жидкостной хроматографии высокого давления не представляет серьезных трудностей; в случае C70 образуется смесь двух изомеров. Дальнейшее восстановление C60H2 может быть осуществлено только с весьма низким выходом: 15% для C60H4.
Исключительно интересным способом восстановления оказался метод, предложенный в свое время Берчем и Хюккелем, который заключается в обработке литием в жидком аммиаке в присутствии трет-бутилового спирта. Темно-фиолетовая суспензия фуллерена при этом превращается в смесь продуктов гидрирования, окрашенную в светло-кремовый или вообще белый цвет. Исследование ее состава показало, что в ней преобладает C60H32, хотя количества других гидридов фуллерена значительны:
 |
Продукты гидрирования по Берчю-Хюккелю легко теряют водород и превращаются в C60, то есть гидрирование является полностью обратимым.
Дата добавления: 2019-07-15; просмотров: 277; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!
