Дослід штерна. Броунівський рух.
| Кількість годин: 1 год |
| ||
| Знання і навички, якими необхідно оволодіти: | |||
| Основні положення МКТ; дифузія, осмос, Броунівсткий рух, хаотичний рух. | |||
| Завдання до самостійної роботи: 1.Законспекутвати основні поняття. 2.Письмово навести приклади дифузії, осмосу, вакууму. | |||
| Форма контролю: | Перевірка самостійних конспектів. | ||
|
| |||
Молекулярно-кинетична теорія (МКТ) пояснює теплові явища в тілах (у речовині) та їх внутрішні властивості. Вона пов`язує закономірності поведінки окремих молекул з характеристиками властивостей тіл. Основні положення МКТ 1. Речовина складається з величезного числа дрібних частинок – молекул( атомів або іонів). 2. Ці частинки знаходяться у безперервному хаотичному русі. 3. Ці частинки (як правило) взаємодіють між собою. Атом – найдрібніша частинка хімічного елемента, що зберігає його хімічні властивості. Молекула – об єднання з кількох атомів – найдрібніша частинка речовини, що зберігає її хімічні властивості. Більшість речовин молекулярної будови (кисень, вода, аміак, метан), але є й атомарні речовини (грфіт, алмаз, гелій,і всі інертні гази), і навіть іонні речовини (всі мітали). Маючи на увазі існування атомарних та іонних речовин, усе ж умовно можна говорити узагальнено про молекулярну будову речовини. Підтвердження положень МКТ:
1)Броунівський рух.
2)Дифузія.
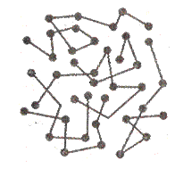
Ботанік Броун, розглядаючи під мікроскопом краплю рідини з урівноваженими в ній частинками (пилком), спостеріг їхній безладний рух. Частинки пилку рухаються під ударами невидимих у мікроскоп молекул.
|
|
|
Дифузія – це проникнення молекул деякої речовини в ділянки простору, в яких перебувають молекули іншої речовини, і навпаки (взаємна дифузія).
Маса і розміри молекул
Для кількісної оцінки речовини користуються поняттям моля – одиниці кількості речовини. Моль – це така кількість речовини, в якій міститься стільки молекул (атомів чи іонів), скільки міститься атомів в 0,012 кг вуглецю 12С. Число молів де т – маса речовини, М –маса моля (визначається За таблицею Менделєєва, наприклад, МN2 = 0,028 кг/моль). Авогадро встановив: 1.Число молекул у молі: NA = 6,02 . 1023 моль-1(стала Авогадро). 2.Об єм моля будь-якого газу при нормальних тиску і темперетурі:
VM0 = 22,4 л/моль = 0,0224 м3/моль.Маса однієї молекули: 
Число молекул у тілі: N = γNA = (m/M)NA . Для оцінки розміру деякої молекули можна розглядати її як маленьку кульку, тоді її об єм (з геометрії) дорівнює 4/3πr3. З формули густини речовини (ρ = m/V) маємо V = m/ρ. Для однієї молекули V 0 = т0/ρ = М/(ρNA) = 4/3 πr3. Звідси для молекули води: 
Молекули настільки малі, що за допомогою оптичних мікроскопів їх побачити не можна.
|
|
|
Дата добавления: 2019-03-09; просмотров: 400; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!
