Соединения металлов главной подгруппы II группы
ОКСИДЫ И ГИДРОКСИДЫ МЕТАЛЛОВ I – III ГРУПП
ГЛАВНЫХ ПОДГРУПП
Оксиды – это сложные вещества, состоящие из двух элементов, один из которых кислород.
Основания - сложные вещества, состоящие из атомов металла, соединенных с одной или несколькими гидроксогруппами.
• Свойства оксидов и гидроксидов в периоде изменяются от основных через амфотерные к кислотным, т.к. увеличивается положительная степень окисления элементов.

 Na
Na 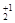 O, Mg+2 O , Al
O, Mg+2 O , Al 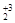 O3
O3
основные амфотерный
Na+1O Н , Mg+2O Н , Al+3(O Н )3
Щелочь Слабое Амфотерный
Основание гидроксид
• В главных подгруппах основные свойства оксидов и гидроксидов возрастают сверху вниз.
Соединения металлов I А группы
Оксиды щелочных металлов
• Общая формула Ме2О
• Физические свойства: Твердые, кристаллические вещества, хорошо растворимые в воде.
Li2O, Na2O – бесцветные, К2О, Rb2O – желтые, Cs2О – оранжевый.
• Способы получения:
1. Окислением металла получается только оксид лития
4Li + O2 → 2Li2O
(в остальных случаях получаются пероксиды или надпероксиды).
2. Все оксиды (кроме Li2O) получают при нагревании смеси пероксида (или надпероксида) с избытком металла:
Na2O2 + 2Na → 2Na2O
KO2 + 3K → 2K2O
|
|
|
· Химические свойства
Типичные основные оксиды:
1. Взаимодействуют с водой, образуя щелочи: Na2О + H2O →
2. Взаимодействуют с кислотами, образуя соль и воду: Na2О + НCl →
3. Взаимодействуют с кислотными оксидами, образуя соли: Na2О + SO3 →
4. Взаимодействуют с амфотерными оксидами образуя соли: Na2О + ZnO → Na2 ZnO2
Гидроксиды щелочных металлов
• Общая формула – МеОН
• Физические свойства: Белые кристаллические вещества, гигроскопичны, хорошо растворимы в воде (с выделением тепла). Растворы мылкие на ощупь, очень едкие.
NaOH – едкий натр
КОН – едкое кали
· Сильные основания - Щелочи. Основные свойства усиливаются в ряду:
LiOH → NaOH → KOH → RbOH → CsOH
- Способы получения:
1. Электролиз растворов хлоридов:
2NaCl + 2H2O → 2NaOH + H2+ Cl2
2. Обменные реакции между солью и основанием:
K2CO3 + Ca(OH)2 → CaCO3 + 2KOH
3. Взаимодействие металлов или их основных оксидов (или пероксидов и надпероксидов) с водой:
2Li + 2H2O → 2LiOH + H2
Li2O + H2O → 2LiOH
Na2O2 + 2H2O → 2NaOH + H2O2
· Химические свойства
1. Изменяют цвет индикаторов:
Лакмус – на синий
Фенолфталеин – на малиновый
Метил-оранж – на желтый
|
|
|
2. Взаимодействуют со всеми кислотами.
NaOH + HCl → NaCl + H2O
3. Взаимодействуют с кислотными оксидами.
2NaOH + SO3 → Na2SO4 + H2O
4. Взаимодействуют с растворами солей, если образуется газ или осадок.
2 NaOH + CuSO4 → Cu(OH)2↓ + Na2SO4
5. Взаимодействуют с некоторыми неметаллами (серой, кремнием, фосфором)
2 NaOH +Si + H2O → Na2SiO3 + 2H2↑
6. Взаимодействуют с амфотерными оксидами и гидроксидами
2 NaOH + ZnО + H2O → Na2[Zn(OH)4]
2 NaOH + Zn(ОН)2 → Na2[Zn(OH)4]
7. При нагревании не разлагаются, кроме LiOH.
Соединения металлов главной подгруппы II группы
Оксиды металлов II А группы
• Общая формула МеО
• Физические свойства: Твердые, кристаллические вещества белого цвета, малорастворимые в воде.
• Способы получения:
1) Окисление металлов (кроме Ba, который образует пероксид)
2Са + О2 → 2СаО
2) Термическое разложение нитратов или карбонатов
CaCO3  CaO + CO2
CaO + CO2
2Mg(NO3)2  2MgO + 4NO2 + O2
2MgO + 4NO2 + O2
· Химические свойства
ВеО – амфотерный оксид
Оксиды Mg, Ca, Sr, Ba – основные оксиды
1. Взаимодействуют с водой(кроме ВеО), образуя щелочи(MgO – слабое основание):
СаО + H2O →
2. Взаимодействуют с кислотами, образуя соль и воду: СаО + НCl →
3. Взаимодействуют с кислотными оксидами, образуя соли: СаО + SO3 →
|
|
|
4. ВеО взаимодействует со щелочами: ВеО + 2NaOH + H2O → Na2[Ве(OH)4]
Дата добавления: 2019-02-22; просмотров: 1294; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!
