При выполнении лабораторной работы необходимо строго соблюдать правила техники безопасности работы в химической лаборатории.
Каждый студент анализирует один из предложенных лекарственных препаратов.
УИРС:
По указанию преподавателя определяют концентрацию одного из лекарственных препаратов нефармакопейными методами. Сравнить результаты определений.
Примечание: список лекарственных форм и лекарственных веществ прилагается.
ЗАНЯТИЕ № 4
ТЕМА: Анализ качества лекарственных и парфюмерно-косметических средств, производных пиримидина: барбитал, барбитал–натрий, барбамил, фенобарбитал, гексенал и др.
Барбитуровая кислота представляет собой циклический уреид – продукт конденсации мочевины с двухосновной малоновой кислотой.
Барбитуровая кислота может существовать в двух таутомерных формах: кето-енольной (за счет протонов водорода метиленовой группы) и имидо-имидольной (за счет протонов водорода имидных групп):
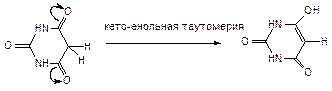
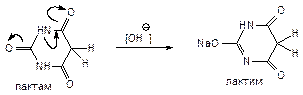
Енольная форма барбитуровой кислоты и её производных обуславливает их кислотный характер.
Подвижность протона в 5-ом положении позволила ученым путём его замены на соответствующие радикалы получить ЛС под общим названием барбитураты. Причем фармакологическое действие проявляют только производные, у которых оба атома водорода заменены на соответствующие радикалы.
Барбитураты существуют в двух формах – это лекарственные средства в кислотной лактамной форме (барбитал, фенобарбитал, бензонал) и солевой лактимной форме (барбитал-натрий, этаминал-натрий, гексенал, тиопентал).
Химические свойства
1) Вследствие лактим-лактамной таутомерии – все барбитураты являются слабыми кислотами или их солями. Барбитураты в кислотной форме растворяются в растворах щелочей и карбонатов щелочных металлов (NaOH, NH4OH, Na2CO3), образуя соли (монозамещенные при рН=10); дизамещенные (рН =13 и более). В медицине применяются только монозамещенные соли.
2) Как соединения, обладающие кислотными свойствами, все барбитураты вступают в реакции комплексообразования с солями тяжелых металлов - кобальта, меди, серебра. Для проведения этих реакций требуется соблюдение следующих условий:
а) в реакции комплексообразования барбитураты должны вступать только в ионном виде
б) реакция среды должна быть примерно нейтральной или слабощелочной.
Для барбитуратов эти условия имеют очень важное значение, т.к. это очень слабые кислоты и их соли легко подвергаются гидролизу, чтобы не допустить гидролиз используется спирт:
А) Фармакопейной реакцией является реакция с солями кобальта. Для этого навеска субстанции растворяется в спирте, добавляется раствор CаCl2 (повышение устойчивости комплекса), растворы Co(NO3)3 или CoCl3, раствор NaOH (для кислотных форм). Для солевых форм NaOH не добавляется. В этих условиях все барбитураты образуют комплексную соль сине-фиолетового цвета, растворимую в воде (т.е. сине-фиолетовый раствор) - общегрупповая реакция.
Для ионизации рекомендуется добавлять раствор аммиака.
Исключение: барбитал-натрий - в виде кислотной формы осаждается из водного раствора добавлением HCl, осадок кислотной формы извлекается в эфир, высушивается, затем проводится реакция как для барбитала.
Б) В реакции с раствором меди сульфата для сохранения необходимой реакции среды используется карбонатный буфер (КНСО3 и К2СО3). Препараты растворяются в воде (солевая форма) прибавляют карбонатный буфер, раствор CuSO4. Для кислотной формы - дополнительно прибавляют раствор 1% NaOH.
Цвет осадка будет характерен для каждого барбитурата, что позволяет использовать эту реакцию для идентификации.
В) Реакция с солями серебра протекает с образованием моно- и дизамещенной соли в присутствии карбоната натрия. Кислотные формы барбитуратов растворяют в растворе карбоната натрия, образуется натриевая соль в лактимной форме (помутнение раствора):
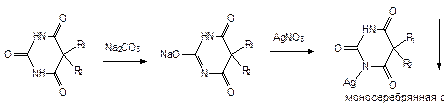
Солевые формы просто растворяются в воде (карбонат натрия не добавляют).
В избытке реактива моносеребрянная соль растворяется, т.к. образуется натриево-серебрянная соль:
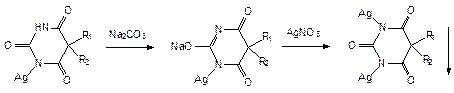
Гексенал, бензонал, которые имеют заместителей в первом положении, образуют монозамещенную серебряную соль, не растворимую в воде:
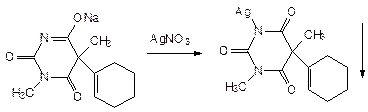
Эту реакцию можно использовать для идентификации, но она не является фармакопейной (используется иногда во внутриаптечном контроле). Или можно использовать нитрат серебра в методе Мора до появления неисчезающего осадка (до появления дизамещенной соли).
Дата добавления: 2019-02-12; просмотров: 201; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!
