Волновые функции и квантовые числа
КВАНТОВАЯ 3
Лекция 9
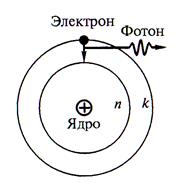
Ядерная модель атома
Резерфорд на основании результатов эксперимента по рассеянию
α-частиц на атомах металлической фольги обосновал планетарную модель строения атома.
Согласно этой модели, атом состоит из тяжёлого положительно заряженного ядра очень малых размеров (~ 10-15 м ), вокруг которого по некоторым орбитам движутся электроны. Радиусы этих орбит имеют размеры ~ 10-10 м.
Наличие у электрона заряда делает планетарную модель противоречивой с точки зрения классической физики, т.к. вращающийся вокруг ядра электрон, как и любая ускоренно движущаяся заряженная частица должен излучать электромагнитные волны. Спектр такого излучения должен быть непрерывным. В опытах наблюдается линейчатый спектр излучения атомов. Кроме того, непрерывное излучение уменьшает энергию электрона, и он из-за уменьшения орбиты обязан был бы упасть на ядро.
Постулаты Нильса Бора
1. Электрон в атоме может двигаться только по определённым стационарным орбитам с определённым номером п = 1; 2; 3; … Движущийся по стационарной замкнутой орбите электрон обладает неизменной полной энергией Еп .
2. Разрешёнными стационарными орбитами являются только те, для которых угловой момент импульса электрона равен целому кратному значению постоянной Планка
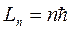 ( п = 1; 2; 3; … ) .
( п = 1; 2; 3; … ) .
3. Испускание или поглощение кванта излучения происходит при переходе атома из одного стационарного состояния в другое.
|
|
|
Частота излучения
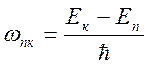
Расчёт атома водорода по Н.Бору
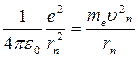 те - масса электрона
те - масса электрона
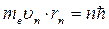 п = 1; 2; 3; …
п = 1; 2; 3; …
Решая систему из этих двух уравнений получаем:
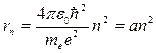 , где а = 0,529 . 10-10 м - радиус 1-ой стационарной
, где а = 0,529 . 10-10 м - радиус 1-ой стационарной
орбиты электрона в атоме водорода
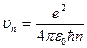
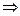
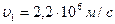
Кинетическая энергия электрона 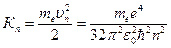
Потенциальная энергия электрона 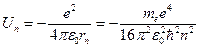
Полная энергия электрона на п-ой орбите
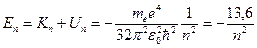 эВ
эВ
Для частоты излучения при переходе из к в п состояние получаем
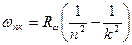 , где
, где 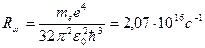 - постоянная Ридберга
- постоянная Ридберга
Существуют также постоянные Ридберга для ν и λ :
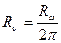 для
для 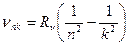 ;
;
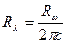 для
для 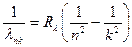
Для водородоподобных атомов ( ион гелия Не+ с Z = 2, двухкратно- ионизованный литий Li++ c Z = 3, трёхкратноионизованный бериллий Ве+++ с Z = 4 и т.д. ) радиусы орбит электрона оказываются в Z раз меньше, чем в атоме водорода, а энергетический спектр водородоподобного иона получается умножением на Z2
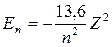 эВ .
эВ .
Квантовая теория атома
Хотя теория Бора даёт хорошие результаты для водородоподобных атомов, она не может рассматриваться как законченная теория атомных явлений.
|
|
|
С позиций современной физики атом является физической системой, которая заведомо не может быть описана классической теорией, не учитывающей волновых свойств движущегося в атоме электрона, так как длина волны де Бройля такого электрона сравнима с размерами атома.
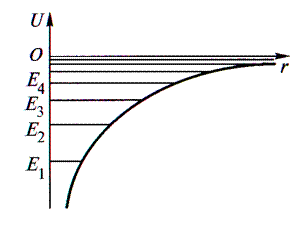
Потенциальная энергия взаимодействия электрона с ядром водородо- подобного атома
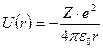 , где
, где
r – расстояние между электроном и ядром, которое в первом приближении
 будем считать точечным.
будем считать точечным.
Движение электрона в таком поле можно рассматривать как движение в некоторой сферической потенциальной яме.
Спектр энергий электрона должен быть дискретным, т.е. состоять из отдельных энергетических уровней со
значениями полной энергии электрона Е1; Е2; Е3 и т.д.
Уравнение Шрёдингера 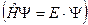 имеет вид
имеет вид
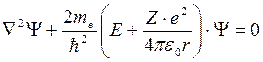
Решение этого уравнения проводят в сферической системе координат r , θ, φ , центр которой совпадает с центром ядра атома. В такой системе Ψ = Ψ( r , θ , φ ) , а оператор Лапласа
|
|
|
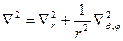 , где
, где 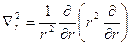 ,
, 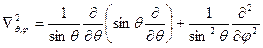
Используя оператор квадрата момента импульса в сферической системе координат
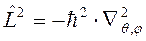
уравнение Шрёдингера преобразуют к виду
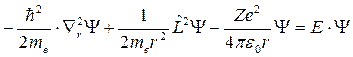
Решение этого уравнения ищут в виде произведения двух функций с разделяющимися переменными
Ψ = X( r ) . Y( θ, φ ).
C учётом естественных требований, налагаемых на Ψ-функцию она должна быть однозначной, конечной, непрерывной и гладкой.
В процессе решения обнаруживается, что этим требованиям можно удовлетворить при любыхположительных значениях энергии Е , но вобласти отрицательных значений Е – только при дискретных значениях, а именно, если
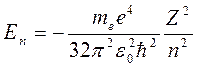 , где п = 1; 2; 3; … ,
, где п = 1; 2; 3; … ,
что соответствует связанным состояниям электрона в атоме.
Таким образом решениеуравнения Шрёдингера приводит в случае Е < 0 к тому же результату, что и теория Нильса Бора но без использования каких либо дополнительных постулатов.
Основное различие заключается в интерпретации состояний электрона: в теории Бора – это движение по стационарным круговым орбитам, а в решении уравнения Шрёдингера орбиты теряют физический смысл – их место занимают Ψ-функции.
Лекция 10
Волновые функции и квантовые числа
|
|
|
Собственные функции уравнения Шрёдингера для атома, т.е. Ψ-функции содержат, как выяснилось, три целочисленных параметра – n , l , m :
Ψ = Ψ nlm ( r, θ, φ )
n - главное квантовое число( то же, что и в выражениях для Еп )
п = 1; 2; 3; …
l – орбитальное (азимутальное) квантовое число, определяющее модуль орбитального момента импульса движущегося ватоме электрона.
В квантовых состояниях с заданным значением главного квантового числа п орбитальное квантовое число может иметь следующие значения:
l = 0 ; 1; 2; 3; … ; (п – 1).
Стационарные волновые функции Ψ nlm ( r ,θ, φ), описывающие различные квантовые состояния атома, являются собственными функциями не только оператора полной энергии 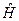 , но и оператора квадрата момента импульса
, но и оператора квадрата момента импульса 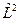 , т.е.
, т.е.
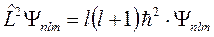 .
.
Следовательно, в любом квантовом состоянии атом обладает определённым значением квадрата момента импульса.
Орбитальное квантовое число l однозначно определяет модуль орбитального момента импульса движущегося в атоме электрона:
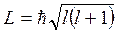
Данное условие квантования момента импульса не совпадает с квантованием момента импульса в теории Н.Бора ( 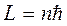 ).
).
Принципиальное отличие этих соотношений состоит в том, что в квантовой теории возможны состояния с L = 0 , а при классическом описании движения электрона в атоме по определённой орбите в любом состоянии атом должен обладать ненулевым моментом импульса.
Эксперименты подтверждают существование квантовых состояний атома с нулевыми орбитальными моментами. Следовательно, опыт подтверждает, что только отказ от классического траекторного способа описания движения электрона в атоме позволяет правильно рассчитать и предсказать свойства атома.
Дата добавления: 2019-02-12; просмотров: 2310; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!
