Тема: «Кинетика химических реакций»
1. Имеет ли размерность (единицы измерения) константа скорости реакции?
1) не имеет размерности
2) имеет размерность скорости
3) размерность определяется порядком реакции
4) зависит от условий протекания реакции.
2. Скорость гомогенной каталитической реакции зависит от:
1) природы катализатора
2) концентрации катализатора
3) площади поверхности катализатора
4) способности катализатора участвовать в реакции
5) температуры.
3. Порядком реакции по концентрации реагирующего вещества называется:
1) масса вещества, вступившая в реакцию к определенному моменту времени
2) показатель степени при концентрации в кинетическом уравнении
3) стехиометрический коэффициент при концентрации кинетическом уравнении
4) молекулярность реакции
5) сумма показателей степени при концентрациях в кинетическом уравнении.
4. При 140°С реакция заканчивается за 30 с. Сколько времени
потребуется для той же реакции при 20°С, если γ = 2?
1) 1,2 ∙104 с 2) 12,3∙104 с 3) 7,3∙10 -3 с
5. Укажите названия приведенных уравнений: 421
А. k 2 = k 1 • γ 2 Б.  0 В.
0 В. 
1. уравнение Аррениуса, преобразованное для расчета температурного коэффициента
|
|
|
2. период полупревращения реакции второго порядка
3. уравнение Михаэлиса - Ментен
4. правило Вант - Гоффа для интервала 20 градусов
5. интегральное уравнение реакции нулевого порядка
6. Как меняется 1nК с ростом величины  ?
?
1) Линейно возрастает с ростом 
2) Линейно уменьшается с ростом 
3) Не меняется
4) Зависит от величины Еа
7. Порядок и молекулярность реакции
1) могут совпадать
2) порядок всегда больше молекулярности
3) порядок всегда меньше молекулярности
4) всегда равны между собой
8. Что называется молекулярностью химической реакции:
1) показатель степени при концентрации в дифференциальном уравнении скорости
2) показатель степени при концентрации в уравнении ЗДМ
3) число частиц, принимающих участие в элементарном акте химического взаимодействия
4) число молекул, пересекающих вершину активационного барьера за 1 секунду
9. Радикальной реакцией называется …
1) очень быстрая реакция
2) реакция, в элементарных актах которой участвуют свободные радикалы
3) реакция, протекающая с изменением состава радикалов в реагирующих веществах
4) реакция, протекающая в 2 или более стадий
|
|
|
5) реакция, протекающая с обязательным участием катализатора
10. В присутствии катализатора энергия активации некоторой реакции снижается с 89,3 до 70,8 кДж/моль. Во сколько раз возрастет скорость реакции при постоянной температуре (30оС)?
1)1,55 ∙102 2)1552 3)7,3 ∙10-3
11. Для какого порядка реакции скорость и константа скорости не зависят от начальной концентрации реагента?
1) 0 2) 1 3) 2 4) 3
12. Период полупревращения газофазной реакции второго порядка зависит от:
1) температуры
2) концентрации реагирующих веществ,
3) природы реагирующих веществ
4) числа реагирующих веществ.
13. Свободными радикалами называются…
1) одинаковые группы атомов, входящие в состав разных молекул
2) ионы, участвующие в обменных реакциях
3) любые частицы, ускоряющие протекание реакций
4) частицы, имеющие неспаренные электроны.
14. Введением катализатора энергия активации реакции при 270С снижена на 2,5 кДж/моль. Во сколько раз возрастет скорость реакции?
1) 2,7 2) 27 3) 270 4) 0,0027
15. Скорость реакции увеличилась в 124 раза, γ = 2,8. На сколько градусов была повышена температура?
1) 470 2) 340 3) 940 4) 570
|
|
|
16. Зависит ли и если да, то как, период полупревращения от исходных концентраций реагирующих веществ для реакции II порядка?
1) не зависит
2) линейно возрастает с ростом с0
3) возрастает с ростом 1/с02
4) уменьшается с ростом с0
17. Время достижения максимальной концентрации промежуточного вещества В в последовательной реакции 1-го
порядка А →К1 → В→ К2 → С зависит:
1)от значения константы скорости К1
2)от значения константы скорости К2
3)от соотношения величин К1 и К2
4)от начальной концентрации вещества А
18. Скорость химической реакции возросла в два раза при повышении температуры на 100С. Вычислить энергию активации при 3000С
1)53,6кДж/моль
2)536 кДж/моль
3)5,4 ∙105Дж/моль
19. Для прямой реакции Eа = 80 кДж/моль; ΔН0 рц = 25 кДж/моль. Чему равны энергия активации и стандартная энтальпия обратной реакции?
1)-80 кДж/моль,-105 кДж/моль
2)55 кДж/моль, -25 кДж/моль
3) 80 кДж/моль, -25 кДж/моль
4) -80 кДж/моль, -25 кДж/моль
20. Реакция 2-го порядка протекает по механизму 1-го порядка при условии:
1) концентрация одного из реагентов значительно больше второго,
2) концентрации исходных реагентов равны,
|
|
|
3) наличие катализаторов,
4) при всех указанных выше условиях.
21. Уравнение Аррениуса k = A exp(-Eа/RT) – это
1) зависимость энергии активации от температуры,
2) зависимость константы скорости от энергии активации,
3) зависимость константы скорости от температуры,
4) зависимость числа соударений от температуры.
22. В каких координатах должна быть представлена зависимость для графического определения энергии активации?
1) ln k - 1/T;
2) k - T;
3) ln k - T;
4) k - 1/T.
23. Реакция А ↔ В. Что изменится в этой реакции, если она будет протекать в присутствии катализатора?
1) А полностью превратится в В,
2) быстрее наступит состояние равновесия,
3) увеличится равновесная концентрация вещества В,
4) увеличится равновесная концентрация вещества А.
24. Для реакции А ↔ В ΔG > 0. Как будет протекать эта реакция в присутствии катализатора?
1) реакция будет протекать с большой скоростью,
2) произойдет полное превращение А в В,
3) установятся равновесные концентрации А и В,
4) реакция не пойдет.
25. Введение катализатора в реакцию сопровождается:
1) увеличением скорости реакции,
2) снижением энергии активации процесса,
3) возможностью осуществления термодинамически невыгодных реакций,
4) все перечисленные характеристики верны.
Тема V : «Поверхностные явления. Адсорбция. Дисперсные системы»
1. Осмотическое давление π в дисперсной системе можно рассчитать:
1) π = С(х)· R·T, 2) π = Cυ·R·T , 3) π = Сυ·КБ·Т, 4) π = (Сυ/NА)·R·T
2. Для дисперсной системы известны коэффициент диффузии, температура и вязкость дисперсионной среды. Как рассчитать радиус сферической частицы?
1) r = Т/D×η, 2) r = RT/6π×η×D×Nа, 3) r = КБТ/6π×η×D, 4) r = T D×η
3. Скорость седиментации тем меньше, чем меньше:
1) вязкость дисперсионной среды
2) температура
3) размер частицы
4) плотность дисперсной фазы
5) плотность дисперсионной среды
4. Какие из перечисленных веществ будут поверхностно-неактивными на границе раздела вода – воздух?
1) Na2СO3 2) С6Н12О6 3) С12Н25NH3Сl
4) С12Н22О11 5) Na2SO4
5. Какой вид приобретает уравнение изотермы Ленгмюра Г = Г∞ (К ∙ с равн / 1 + К· с равн ) при малых значениях с?
1) Г = Г∞ 2) Г = Г∞ · сравн 3) Г = сравн 4) Г = const · cравн.
6. Электрофоретическая подвижность частиц дисперсной фазы тем больше, чем больше:
1) вязкость дисперсионной среды,
2) диэлектрическая проницаемость,
3) электрокинетический потенциал,
4) напряженность электрического поля.
7. Какие из приведенных МПАВ будут нужны для получения эмульсии бензола в воде:
| ПАВ | ГЛБ |
| 1) Лауриловый спирт | 40 |
| 2) Натрия олеат | 18 |
| 3) Моностерат глицерина | 3,8 |
| 4) Олеиновая кислота | 1,0 |
8. Способность ПАВ изменять поверхностное натяжение характеризуется величиной поверхностной активности
g = lim(-Δσ / Δc)
с → 0
Какие из перечисленных соединений имеют g < 0?
1) CuSO4 2) C17H33COONa 3) C6H12O6 4) H2SO4
9. Назовите вещества, которые дадут подобную изотерму на границе раздела
 1) Na2СO3 Г, вода - воздух
1) Na2СO3 Г, вода - воздух
2) С2Н5СООН моль/м2


 3) С12Н25NН3Сl Г∞
3) С12Н25NН3Сl Г∞
4) KNO3
0 С(ПАВ),равн.
10. Осмотическое давление в дисперсных системах мало по сравнению с истинными растворами той же массовой концентрации, потому что:
1) малы размеры частиц дисперсной фазы
2) мала вязкость дисперсионной среды
3) велики размеры частиц дисперсной фазы
4) мала скорость седиментации частиц
11. Скорость седиментации равна 0 для частиц грубодисперсной системы, если:
1) вязкость дисперсионной среды мала
2) плотность дисперсной фазы ρд.ф. мала
3) плотность дисперсионной среды ρд.ср. мала
4) ρд.ф. = ρд.ср.
5) температура - const.
12. Золь AgJ получен при избытке ионов J-. Добавление каких электролитов по мере роста их концентрации может изменить направление движения коллоидных частиц золя при электрофорезе:
1) NaNO3 2) LiCl 3) Al(NO3)3 4) AgNO3
13. При каких значениях рН можно разделить фракции двух белков с изоэлектрическими точками Jэ1 = 3,6 и Jэ2 = 4,8 методом электрофореза?
1) рН = 3,6 2) рН > 4,8 3) 3,6 < рН < 4,8 4) рН < 3,6
14. Найти соответствие между прямыми и конфигурацией молекулы ВМС:
 I. линейная, II. сферическая
I. линейная, II. сферическая

 π/см 3 1 1) I – 2 ; II – 1
π/см 3 1 1) I – 2 ; II – 1
 2 2) I – 1, 3; II – 2
2 2) I – 1, 3; II – 2
3) I – 2; II – 3
4) I – 1; II – 2
0 см
15.  Назовите вещества, которые дадут подобную изотерму на границе
Назовите вещества, которые дадут подобную изотерму на границе
1. Na2СO3 Г раствор – воздух
2. С2Н5СООН моль/м2 Г∞


 3. С12Н25NH3Сl I.
3. С12Н25NH3Сl I.
4. KNO3
5. С5Н1111ОН
 6. С10Н21SO3Na
6. С10Н21SO3Na
7. Na2SO4 0 CПАВ, равн.
II.
16. Краевой угол смачивания раствора ПАВ по сравнению с краевым углом чистого растворителя:
1) уменьшается 2) увеличивается
3) не изменяется 4)стремится к нулю
17. Назовите причины возникновения ДЭС в следующих системах:
I. золь AgJ в растворе AgNO3
II. водная суспензия ТiO2
III. водная суспензия Аl(ОН)3
1. Переход ионов с поверхности твердой фазы в раствор.
2.Переход ионов из раствора на твердую поверхность.
3. Поляризация поверхности внешним источником.
18. Расположите в ряд по возрастанию значений ККМ следующие соединения:
I. C12H23SO3Na II. C8H17SO3Na III. C10H21SO3Na
231
19. Какая из прямых находится в соответствии с уравнением Эйнштейна для концентрационной зависимости вязкости дисперсных систем?



 ηуд./φ 3 2
ηуд./φ 3 2
1
1) 1
2) 2
3) 3
0 φ, %
20. Тиксотропия - это:
1) механическое разрушение дисперсных систем
2) самопроизвольное восстановление разрушенной структуры со временем
3) 1 и 2 варианты ответа
4) самопроизвольное уменьшение размеров геля (студня) с одновременным выделением из него дисперсионной среды.
21. Способность ПАВ изменять поверхностное натяжение характеризуется величиной поверхностной активности
g = lim(-Δσ /Δc)
c(ПАВ) → 0
Для каких из приведенных ПАВ значения поверхностной активности g возрастают примерно в 10 раз?
I. СН3(СН2)2СООН II.HCOOH III.СН3СН2СООН IV.(СН3 )3 CСООН
22. Какой из перечисленных ниже систем соответствует приведенная ориентация ПАВ на границе раздела фаз?
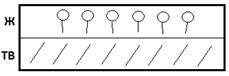
1) гидрофобная твердая поверхность в водном растворе ПАВ
2) гидрофильная твердая поверхность в водном растворе ПАВ
3) гидрофобная твердая поверхность в углеводородном растворе ПАВ
4) гидрофильная твердая поверхность в углеводородном растворе ПАВ
23. В какой системе координат уравнение изотермы Фрейндлиха представляет собой прямую линию?
1) Г, с; 2) lg Г, с; 3) Г, lg c; 4) lg Г, lg с.
24. Даны следующие дисперсные системы: эмульсии, золи, пыли, туманы, суспензии, пены.
К каким типам систем они относятся?
1) тв/ж, тв/г, ж/тв, ж/ж, ж/г, г/тв
2) ж/ж, ж/тв, тв/г, г/ж, тв/ж, ж/г
3) ж/г, тв/ж, г/тв, ж/г ж/тв , г/ж
4) ж/ж, тв/ж, тв/г, ж/г, тв/ж, г/ж
25. К золю AgJ, полученному в избытке ионов Ag+, добавляется электролит. Какие электролиты по мере роста их концентрации могут вызвать перезарядку частиц золя?
1) NaCl 2) NaNO3 3) Ca(NO3)2 4) KJ
26. Коагуляция необратима, если
1) Еэл. = Евд, ξ << 0, λ >> δ, Cэл. мала
2) Еэл. > Eвд, ξ > 0, λ > δ, Сэл. = γм.коаг.
3) Еэл. = 0, ξ = 0, λ = 0, Сэл. = γб.коаг
4) Еэл. ‹ Eвд, ξ > 0, λ > δ, Сэл. = γм.коаг
27. По теории ДЛФО Еэл. тем больше, чем больше :
1) ξ - потенциал,
2) радиус частиц,
3) толщина диффузного слоя,
4) диэлектрическая проницаемость среды
5) концентрация электролита-коагулятора
6) заряд иона - коагулятора
28. В какой из приведенных макрогетерогенных систем при увеличении концентрации ПАВ наиболее вероятно самопроизвольное возникновение коллоидной системы? (Т = сonst) :
1) водный раствор ПАВ – воздух;
2) водный раствор ПАВ - гептан
3) водный раствор ПАВ – ртуть
29. Поверхностное натяжение является работой увеличения поверхности раздела фаз при постоянстве:
1) температуры, объёма (давления) и состава смеси;
2) температуры, объёма (давления);
3) температуры, объёма (давления), состава смеси, отнесенного к единице поверхности;
4) объёма (давления) и состава смеси, отнесенного к единице поверхности
30. Скорость седиментации тем больше, чем меньше:
1) вязкость дисперсионной среды
2) плотность дисперсной фазы
3) температура
4) плотность дисперсионной среды
31. К каким типам дисперсных систем относятся следующие: пены, золи, суспензии, пемзы, эмульсии, туманы, порошки?
1) тв/ж, тв/г, ж/тв, ж/ж, ж/г, г/тв тв/г
2) ж/ж, ж/тв, тв/ж, г/тв, ж/ж, г/ж тв/ж
3) г/ж, тв/ж, тв/ж, г/тв ж/ж , ж/г тв/г
4) ж/г, тв/ж, тв/г, тв/г г/ж, г/ж г/тв
32. Какие из перечисленных веществ будут поверхностно-инактивными на границе раздела вода - воздух?
1. Na2СO3 4. С6Н12О6 7. С12Н25NH3Сl
2. С12Н22О11 5. Na2SO4 8. KNO3
3. С5Н11ОН 6. С10Н21SO3Na
33. Какой из перечисленных ниже систем соответствует приведенная ориентация ПАВ на границе раздела фаз?

1. гидрофобная твердая поверхность в водном растворе ПАВ,
2. гидрофильная твердая поверхность в водном растворе ПАВ,
3. гидрофобная твердая поверхность в углеводородном растворе ПАВ,
4. гидрофильная твердая поверхность в углеводородном растворе ПАВ
34. Как изменится интенсивность рассеянного света (Ip,1/ Ip,2), если золь ВаSО4 подвергнуть действию света с λ1 = 430 нм и λ2 = 680 нм?
35. Расположите в ряд электролиты по возрастанию их коагулирующей способности по отношению к золю AgJ с отрицательно заряженными частицами
1) Ca(NO3)2 3) Al(NO3)3 5) Ba(NO3)2
2) NaNO3 4) LiNO3 6) RbNO3
426153
36. Золь AgJ получен в избытке ионов J-. При добавлении каких электролитов (по мере роста их концентрации в растворе) коагуляция может смениться пептизацией.
1) NaNO3 2) AlCl3 3) Na2SO4 4) Th(NO3)4 5) AgNO3
37. В лиотропных рядах ионы одного заряда расположены по мере роста:
1) адсорбционной способности
2) радиуса
3) гидратации
4) поляризации
5) коагулирующей способности
6) порога коагуляции.
38. Осмотическое давление в растворах ВМС может быть рассчитано:
1) π = Сν·КБ·Т
2) π = С(Х)·КБ·Т
3) π = η · ρ · g
4) π = (R·Т/М)·См + β·См2
5) π / См = const + β·См
39. Стадия набухания ВМС в растворителе характеризуется:
1) ΔН > 0 2) ΔS = 0 3) ΔG > 0 4) ΔН < 0 5) ΔS > 0 6) ΔG > 0
40. Один и тот же объём кварцевого песка измельчается в шаровой мельнице:
1) на воздухе 2) в воде 3) гептане.
Укажите, в каком случае работа диспергирования будет минимальна?
41. Имеются суспензии BaSO4 с размерами частиц:

Найти соответствие между кинетической кривой седиментации и размерами частиц.
1) 1- I, 2 –II, 3 – III; 2) 1 – II, 2 – III, 3 – I; 3) 1 – II, 2 – I, 3 - III
42. Расположите в ряд электролиты по возрастанию их коагулирующей способности по отношению к золю As2S3 с отрицательно заряженными частицами
1) Ca(NO3)2 3) Al(NO3)3 5) Ba(NO3)2
2) NaNO3 4) LiNO3 6) RbNO3
426153
43. Согласно теории ДЛФО Евд. изменяется в зависимости от расстояния между частицами по:
1) экспоненциальному закону
2) степенному закону
3) линейному закону.
44. Пептизация - это процесс:
1) самопроизвольного слияния капелек эмульсии
2) самопроизвольного агрегирования
3) самопроизвольного диспергирования
4) самопроизвольного разрушения дисперсной системы.
45. Из перечисленных ниже МПАВ выделите анионные:
1) С12Н25ОSO3Na
2) [C10Н21О(С2Н4О)6]2РООК
3) С17Н35СООСН2СН2ООС17Н35
4) С9Н19С6Н4О(С2Н4О)7Н
46. Из перечисленных ниже МПАВ выберите катионные:
1) С10Н21О(С2Н4О)3SO3Na
2) CF3(CF2)7COONH4
3) [С17Н35С5Н5N]Cl
4) С12Н25О(С2Н4О)7Н
47. Из перечисленных ниже МПАВ выберите неионогенные:
1) СН3С6Н4NSO3Na
2) [C10H21N(CH3)9]Cl
3) C13H27NH2
4) С15Н31СОО(С2Н4О)7Н
48. Вещества, которые могут образовывать структурно-механический барьер на границе раздела вода-масло и использоваться в качестве эмульгаторов прямых эмульсий:
1) натрий пропионат
2) валериановая кислота
3) желатина
4) мел
49. Электрофорез – явление перемещения частиц дисперсной фазы относительно дисперсионной среды в:
1) переменном электрическом поле
2) постоянном электрическом поле
3) гравитационном поле
4) магнитном поле
5) под давлением
50. ДЭС – это:
1) потенциалопределяющие ионы + противоионы
2) потенциалопределяющие ионы + противоионы адсорбционного слоя
3) противоионы адсорбционного и диффузного слоев.
51. Электроосмос – явление перемещения дисперсионной среды относительно неподвижной дисперсной фазы в:
1) переменном электрическом поле,
2) постоянном электрическом поле,
3) гравитационном поле,
4) магнитном поле,
5) под давлением
52. Изоэлектрическая точка рJ для альбумина равна 4,8. Как заряжена белковая глобула при рН = 8?
1) «+» 2) «-» 3) не заряжена
53. Стадия сольватации ВМС растворителем при набухании характеризуется:
1) ΔS > 0 2) ΔG > 0 3) ΔН < 0 4) ΔH = 0 5) ΔG < 0
54. Какие из приведенных ПАВ могут быть использованы для стабилизации обратной эмульсии (в/м):
1) С17H35COOK 2) С17H35COOH 3) С17H33COOK 4) С17Н35OH
55. Молярную массу ВМС с палочкообразными макромолекулами можно рассчитать, используя уравнения:
1) Штаудингера 2) Марка-Куна -Хаувинка 3) Вант-Гоффа
Дата добавления: 2019-01-14; просмотров: 987; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!
