Полиморфизм и свойства железа.
Содержание железа в земной коре составляет около 4,5%. Это четвертый по распространенности в природе элемент. Ниже температуры 911°C железо существует в низкотемпературной модификации a-Fe, которая имеет объёмно центрированную кубическую элементарную ячейку (ОЦК), с параметром, а = 0.2862 нм. Важной особенностью a-Fe является его ферромагнетизм, проявляющий себя при температурах ниже 768°С, называемой точкой Кюри. В интервале температур от 911°C до 1392 °C железо существует в модификации g-Fe, имеющей гранецентрированную элементарную ячейку (ГЦК) с параметром, а = 0,364 нм. Выше температуры 1392°C железо снова существует в модификации a-Fe. Температура плавления железа составляет 1539 °С.
Размеры пространства, которое может быть занято сторонними атомами, в ОЦК структуре a-Fe составляет около 0,06 нм, в ГЦК структуре g-Fe около 0,1 нм. Различие в размерах структурных вакансий влияет на величину растворимости углерода в a- и g - железе. Диаметр атома углерода равен 0,154 нм. Растворимость углерода в a - железе в основном обусловлена размещением атомов углерода в дефектах кристаллической решетки, так как диаметр структурных вакансий в ОЦК структуре меньше, чем диаметр атома углерода. Величина растворимости углерода в низкотемпературном феррите достигает 0,02% при 727°C, а в высокотемпературном - 0,1% при 1499°С.
 а)
а)
 б)
б)
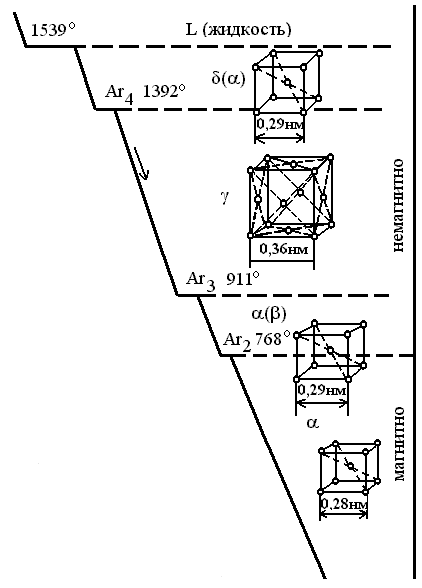
Рис. 2.1 Температурная зависимость параметра элементарных ячеек α-, γ- и δ - модификаций железа (слева). Виды элементарных ячеек аллотропных модификаций железа и температуры их фазовых превращений (справа).
|
|
|
В g-Fe атомы углерода с обобществленными электронами размещаются в структурных вакансиях ГЦК решетки. Растворимость углерода достигает 2.14 масс % при 1147 °С.
Плотность железа составляет 7680 кг/м3. Предел прочности при растяжении технически чистого железа, содержащего около 0,1% примесей, равен 200 – 250 МПа, относительное удлинение 50 – 60%, твердость 70 – 80 НВ. Повышение степени очистки приводит к снижению прочности и твердости железа. Сплавы железа с углеродом, содержащие до 0,02 масс % C называют техническим железом.
2.2. Диаграмма состояния системы Fe – Fe3C.
В системе железо-углерод существуют следующие фазы: жидкий расплав, твердые растворы (феррит и аустенит), химическое соединение Fe3C (цементит), свободный углерод в виде графита. К структурным составляющим системы Fe – Fe3C относят фазово-зёренные образования перлит и ледебурит, представляющие собой механические смеси сосуществующих фаз.
Феррит – твердый раствор внедрения углерода в a-Fe , имеющем объемно гранецентрированную кристаллическую структуру. На диаграмме Fe – Fe3C обозначается буквой Ф. Твёрдый раствор, как и α-Fe имеет ОЦК структуру, что определяет малую протяжённость области гомогенности. Низкотемпературный a - феррит содержит до 0,02 масс % углерода, высокотемпературный a - феррит до 0,1 масс % углерода. Техническое железо имеет структуру феррита, который вытравливается на шлифах в виде однородных зерен. Феррит высокопластичен и мягок (80 – 120 НВ), хорошо обрабатывается давлением в холодном состоянии.
|
|
|
Аустенит – твердый раствор внедрения углерода в g- Fe (гранецентрированная кубическая структура) с максимальным содержанием углерода 2,14%, при 1147оC. Условия, ограничивающие область существования аустенита на диаграмме состояния системы Fe -Fe3C. На диаграмме обозначается буквой A. Аустенит существует в температурном интервале от 727 °C до 1490 °C. Микроструктура сплава представлена однородными зернами. Аустенит высокопластичен, но более тверд, чем феррит (160 – 200 НВ). Заметные размеры структурных вакансий около 0,1нм определяют заметную растворимость в аустените различных химических элементов.
Цементит – химическое соединение Fe3C, содержит 6,67 масс % углерода. Самая твердая (800 НВ) и хрупкая составляющая сплавов железа с углеродом. Имеет сложную ромбическую, плотноупакованную структуру. Температура плавления равна 1250°C. До температуры 210 °C цементит магнитен. При высоких температурах разлагается на графит и аустенит. Образует твердые растворы замещения, в которых углерод замещается неметаллами (кислородом, азотом), а железо металлами (марганцем, хромом, вольфрамом и т. д.). Сплавы на основе цементита в чистом виде не используют. Чем больше цементита в железоуглеродистом сплаве, тем выше твердость последнего.
|
|
|
Графит – аллотропическая модификация углерода со слоистой гексагональной структурой и слабой связью между слоями. Графит мягок, прочность его очень низкая. Температура плавления около 3800 °C, плотность 2500 кг/ м3. Химически стоек и имеет электропроводность, как у металлов.
Перлит – механическая смесь феррита и цементита, содержащая 0,8 масс % углерода и образующаяся в процессе медленного охлаждения при перекристаллизации (распаде) аустенита, ниже температуры 727оС. Образуется при перекристаллизации (распаде) аустенита при t = 723 °C на феррит и цементит. Такой распад называется эвтектоидным, а перлит — эвтектоидом. Перлит обладает высокими прочностью (ав = 800 МПа), твердостью 200 НВ и повышает механические свойства сплава. Зёренная структура перлита образована чередующимися пластинками феррита и цементита.
|
|
|

Рис. 2.2. Диаграмма состояния системы Fe – Fe3C. На верхней оси абсцисс отложены массовые % углерода; на нижней оси абсцисс отложены мольные % Fe3C.
Ледебурит – механическая смесь кристаллов аустенита и цементита, образуется при кристаллизации сплава с 4,3 масс % углерода при t = 1147°C, (эвтектика между фазами аустенита и цементита). Ледебурит является эвтектикой, образованной между аустенитом и цементитом. При температурах ниже 727 °C аустенит в ледебурите превращается в перлит, и после охлаждения до комнатной температуры ледебурит представляет собой смесь перлита с цементитом. Ледебурит тверд (700 НВ). Имеет сотовое или пластинчатое строение и содержится во всех белых чугунах.
Диаграмма состояния Fe-Fe3C (рис. 2.2) характеризует фазовый состав и превращения в системе железо – цементит (6,67 % С). На оси абсцисс, которая является осью составов, представлено две шкалы показывающие содержание углерода и цементита. Часть диаграммы, имеющая практическое значение, расположена в диапазоне концентраций углерода до 6,67 %, что соответствует химическому соединению Fe3C (цементит Ц). Координаты характерных точек диаграммы приведены в табл. 2.1. Точка A определяет температуру плавления чистого железа, а точка D- температуру плавления (разложения) цементита. Точки N и G соответствуют температурам полиморфных превращений железа. Точки H и P характеризуют предельную концентрацию углерода соответственно в высокотемпературном и низкотемпературном феррите. Точка E определяет наибольшую концентрацию углерода в аустените. Значения остальных точек будут обсуждены позже.
Превращения в сплавах системы Fe – Fe3C происходят как при затвердевании жидкой фазы, так и в твердом состоянии. Первичная кристаллизация идет в интервале температур, определяемых на линиях ликвидус (ABCD) и солидус (AHJECF).
Таблица 2.1
Характерные точки диаграммы состояния железо-цементит
| Обозначение точки на диаграмме | Температура в оС | Концентрация углерода в % | Обозначение точки на диаграмме | Температура в оС | Концентрация углерода в % |
| А | 1539 | 0 | C | 1147 | 4.3 |
| Н | 1499 | 0.1 | F | 1147 | 6.69 |
| J | 1499 | 0.16 | G | 911 | 0 |
| B | 1499 | 0.51 | P | 727 | 0.02 |
| N | 1392 | 0 | S | 727 | 0.8 |
| D | 1560 | 6.67 | K | 727 | 6.69 |
| E | 1147 | 2.14 |
Вторичная кристаллизация вызвана превращением железа одной модификации в другую и переменной растворимостью углерода в аустените и феррите. При понижении температуры растворимость уменьшается. Избыток углерода из твердых растворов выделяется в виде цементита. Линии ES и PQ характеризуют изменение концентрации углерода в аустените и феррите соответственно. Цементит имеет почти неизменный состав (двойная вертикальная линия DFKL). Цементит, выделяющийся из жидкости, называют первичным; цементит, выделяющийся из аустенита - вторичным; цементит, выделяющийся из феррита — третичным. Соответственно линию DC на диаграмме состояния называют линией первичного цементита, ES- линией вторичного цементита; PQ-линией третичного цементита. В системе железо – цементит происходят три изотермических превращения.
Перитектическое превращение на линии HJB (1499 °С)
Фн + Жв®Аj.
Эвтектическое превращение на линии ECF (1147 °С)
Жс®[АЕ + Ц] ≡ Ледебурит.
Эвтектоидное превращение на линии PSK (727 °С)
Аs®[ФР + Ц] ≡ Перлит.
Эвтектическая смесь аустенита и цементита называется ледебуритом (В честь немецкого ученого А. Ледебура), а эвтектоидная смесь феррита и цементита - перлитом.
Еще раз отметим, что эвтектоид - перлит (содержит 0,8 %С) и эвтектику - ледебурит (4,3 %С) рассматривают как самостоятельные структурные составляющие, оказывающие заметное влияние на свойства сплавов. Перлит чаще всего имеет пластинчатое строение и является прочной структурной составляющей. При охлаждении ледебурита до температур ниже линии SK входящий в него аустенит превращается в перлит, и при температуре 20 – 25°C ледебурит представляет собой смесь цементита и перлита. В этой структурной составляющей цементит образует сплошную матрицу, в которой находятся колонии перлита. Такое строение ледебурита служит причиной его большой твердости и хрупкости. Присутствие ледебурита в структуре сплавов обусловливает их неспособность к обработке давлением, затрудняет обработку резанием.
Железоуглеродистые сплавы подразделяют на две основные группы: стали, содержащие до 2,14% C и чугуны, содержащие свыше 2,14% C (табл.2.2).
Дата добавления: 2019-02-22; просмотров: 1037; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!
