Агрегатные состояния вещества.
Атом – наименьшая частица химического элемента, обладающая его основными свойствами. Атом является химически не делимым. Взаимные превращения атомов происходят при ядерных реакциях.
Молекула – наименьшая частица вещества, обладающая основными химическими свойствами вещества и состоящая из атомов, соединенных химическими связями.
Состояния вещества, переходы между которыми сопровождаются скачкообразным изменением ряда физических свойств, называют агрегатными. В зависимости от физических условий, главным образом от температуры (Т) и давления (Р), вещества могут существовать в твердом, жидком и газообразном агрегатном состояниях.
Газ — агрегатное состояние вещества (атомы, молекулы), характеризующие частицы, которые не связаны или слабо связаны силами взаимодействия и хаотически движутся, заполняя весь возможный объем. Ионизированный газ, в котором плотности положительных и отрицательных зарядов практически одинаковы, образует плазму. Плазму считают четвертым агрегатным состоянием вещества.
Жидкость - агрегатное состояние вещества, характеризующееся объемом, поверхностью раздела, малой сжимаемостью и текучестью, ближним порядком в расположении атомов и молекул; в отличие от газов в жидкости имеется более сильное взаимодействие между атомами и молекулами.
Тепловое движение молекул (атомов) жидкости представляет собой сочетание малых колебаний около положения равновесия и перескоков из одного положения равновесия в другое. Этим обусловлена текучесть — свойство жидкости (и газа) пластически или вязко деформироваться под действием механической нагрузки. Давление в любой точке покоящейся жидкости одинаково во всех направлениях, поэтому жидкости подобно газам не обладают упругостью формы и практически несжимаемы.
|
|
|
Кристаллическая структура веществ.
Кристаллами называют твердые тела, обладающие упорядоченной трехмерно-периодической пространственной атомной (молекулярной) структурой и имеющие вследствие этого при определенных условиях образования форму многогранника. Таковы природные кристаллы минералов, возникшие в результате процессов, происходивших в земной коре, или синтетические кристаллы, выращиваемые в лабораториях.
Кристаллическая структура – конкретное распределение материальных частиц (атомов, ионов, групп атомов) в пространстве. Как синоним кристаллической структуры используется также термин кристаллическая решётка.
В 1860г. Е. С. Федоровым была выдвинута гипотеза о том, что в кристаллах существует закономерное расположение атомов (частиц). Экспериментально эта гипотеза была подтверждена в 1912г. М. Лауэ с помощью рентгенографического анализа. Современные методы исследования позволяют получать реальные изображения расположения атомов (светлые сферы) в структуре металлов, полупроводниковых материалов, химических соединений (рис. 1.1).
|
|
|
В кристаллической структуре имеется дальний порядок, который проявляется в строгой повторяемости во всех направлениях одного и того же структурного элемента на протяжении сотен и тысяч периодов кристаллической решетки.
В кристаллической структуре выделяют элементарную ячейку. Существует три правила выбора элементарной ячейки: симметрия элементарной ячейки должна оставаться такой же, как и симметрия кристаллической решётки, число прямых углов в элементарной ячейке должно быть максимальным, а объём ячейки - минимальным.

с) 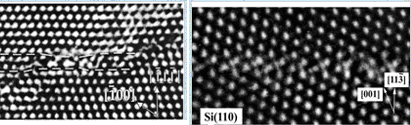
Рис. 1.1 Расположение атомов:
а) - в кристаллографической плоскости, б) – в пространственной кристаллической структуре (решетке), в)- в элементарной примитивной кубической ячейке; с) в кристалле кремния Si (электронная микроскопия).
Элементарной ячейкой называется параллелепипед повторяемости, построенный на кристаллографическом базисе. Элементарная ячейка является частью структуры кристалла, путем её переноса (трансляции) в пространстве параллельно самой себе по трём кристаллографическим осям воссоздается кристаллическая структура материала.
|
|
|
По признаку точечной симметрии элементарной ячейки все кристаллические структуры группируются в сингонии -подразделения кристаллов по конфигурации элементарной ячейки. Всего сингоний семь: кубическая, тетрагональная, ромбическая, гексагональная, тригональная, моноклинная, триклинная (рис. 1.2).
Сингонии характеризуют длинами ребер и углами между ними. Для кубической сингонии a=b=c, α=β=γ=900. В элементарной ячейке атомы могут располагаться только в узлах геометрических фигур – такие элементарные ячейки называются примитивными и обозначаются буквой Р. При расположении атомов в узлах и центре граней образуется объёмно центрированная элементарная ячейка I. Элементарная ячейка, в которой атомы располагаются в узлах и центре всех боковых граней называется гранецентрированной, и обозначается буквой F. Элементарная ячейка с расположением атомов в центре нижней и верхней граней является базоцентрированной элементарной ячейкой С. Всего таких ячеек 14, и они называются элементарными ячейками Бравэ.
|
|
|
| 14 элементарных ячеек (решёток) Бравэ | Сингонии |
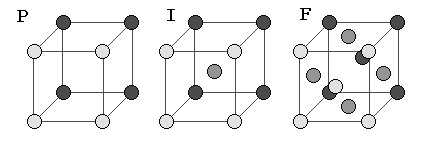
| Кубические a=b=c α=β=γ=900 |
| Pmim Imim Fmim | |
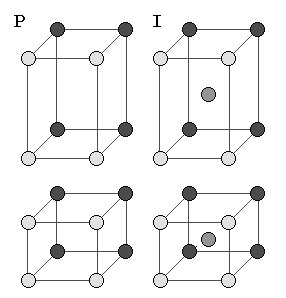
| Тетрагональные a=b≠c α=β=γ=900 |
| P4/mmm I4/mmm | |

| Ромбические a≠b≠c α=β=γ=900 |
| Pmmm Immm Cmmm Fmmm | |

| Гексагональные и тригональная a=b≠c a=b=c α=β=900,γ=1200 α=β=γ≠900
|
| P6/mmm Rim | |

| Моноклинные и триклинная a≠b≠c a≠b≠c α=γ=900≠β α≠β≠γ≠900
|
P2/m C2/m P 
|
Рис. 1.2. Кристаллографические сингонии:
кубическая, тетрагональная, ромбическая, гексагональная, тригональная, моноклинная, триклинная; 14 видов элементарных ячеек Бравэ, под которыми указаны их пространственные группы.
Каждая ячейка Бравэ – параллелепипед повторяемости – характеризуется своими параметрами – константами решетки: тремя координатными векторами  либо соответствующими скалярными величинами
либо соответствующими скалярными величинами 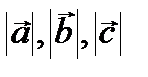 и углами
и углами  (рис. 1.2).
(рис. 1.2).
Являясь наиболее крупным классификационным подразделением в симметрии кристаллов, каждая сингония включает несколько пространственных групп симметрии,присущих кристаллической структуре. Существует 230 пространственных групп. Все известные кристаллические структуры веществ соответствует какой-либо из пространственных групп. На рис. 1.2 под элементарными ячейками указаны их пространственные группы.
Металлы и сплавы являются одной из обширных и значимых групп материалов. Структуры металлов в основном имеют следующие виды элементарных ячеек: кубическую объемно центрированную (ОЦК), кубическую гранецентрированную (ГЦК), гексагональную, тетрагональную объёмно центрированную (рис. 1.2).
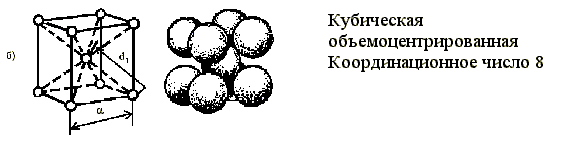



Рис. 1.3. Виды элементарных ячеек:
б – кубическая объемно-центрированная, координационное число 8; в – кубическая гранецентрированная, координационное число 12; г – гексагональная, координационное число 12; д – тетрагональная объемно-центрированная, координационное число 8.
Важнейшей характеристикой кристаллической структуры является координационное число атомов, образующих структуру.
Координационное число соответствует количеству химических связей А – В, образованных атомом А с атомами В. Структуры чистых веществ образованы атомами одного элемента. Для таких структур координационное число численно равно количеству атомов, находящихся от данного атома на одинаковом и минимальном расстоянии. Так, К6 означает, что атом данного элемента в кубической решетке окружён 6 атомами, находящимися от него на минимальном и одинаковом расстоянии.
В зависимости от вида элементарной ячейки и координационного числа атомов выделяют следующие основные типы пространственных кристаллических решёток (рис. 1.3): а) — примитивная кубическая, координационное число 6 (К6); б) — кубическая объемно-центрированная, координационное число 8 (К8); в) — кубическая гранецентрированная координационное число 12 (К12), г) — гексагональная плотноупакованная координационное число 12 (Г12), д) — тетрагональная объёмно-центрированная (Т8).
Значения параметров элементарных ячеек определяются расчётным путём на основе экспериментальных данных изучения проб образцов методами рентгеновской дифракции. Рассчитываются параметры элементарных ячеек и углы между ними. Для кубических элементарных ячеек рассчитывается только один параметр величина стороны куба а. Параметры по абсолютным значениям имеют порядок атомных размеров и измеряются в нанометрах (нм), 1 нм=10-9м. Параметры элементарных ячеек для большинства металлических элементов находятся в пределах 0,3÷0,7 нм. Так, Сr с решеткой типа К8 имеет, а=0,28788 нм, а у Ni с решеткой типа К12 значение, а=0,35165нм. У решеток типа Г12, Г6 и Т6 наряду с параметром a имеется второй параметр, которым является величина ребра призмы или параллелепипеда с. Кристаллическая структура типа Г12 характеризуется постоянным значением отношения с/a=1,6333; при с/а ≠ 1,6333 кристаллическая решетка считается не плотно упакованной.
Полиморфизм – свойство некоторых веществ существовать в нескольких кристаллических модификациях с разной структурой.
Дата добавления: 2019-02-22; просмотров: 1143; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!
