Взаимодействие с галогенами и серой при высокой температуре.
Железо и его соединения
Кларк в земной коре 4,65 % по массе (4-е место по распространенности среди элементов, 2-е - среди металлов). В свободном виде почти не встречается. Основные формы рудоносных минералов - оксиды и сульфиды: магнетит Fe3O4, гематит Fe2O3, пирротин FeS, пирит FeS2 (железный колчедан).
В организме человека содержится около 5 г железа, большая часть его (70%) входит в состав гемоглобина крови.


Физические свойства
В свободном состоянии железо - серебристо-белый металл с сероватым оттенком. Чистое железо пластично, обладает ферромагнитными свойствами. На практике обычно используются сплавы железа - чугуны и стали.
Fe - самый главный и самый распространенный элемент из девяти d-металлов побочной подгруппы VIII группы. Вместе с кобальтом и никелем образует «семейство железа».
При образовании соединений с другими элементами чаще использует 2 или 3 электрона (В = II, III ).
Железо, как и почти все d-элементы VIII группы, не проявляет высшую валентность, равную номеру группы. Его максимальная валентность достигает VI и проявляется крайне редко.
Наиболее характерны соединения, в которых атомы Fe находятся в степенях окисления +2 и +3.
| Fe+2 | Fe+3 | Fe+6 | ||
| Оксиды | FeO основный | Fe2O3 | FeO3 - не выделен | |
| Гидроксиды | Fe(OH)2 слабое основание | Fe(OH)3 ↔ HFeO2 + H2O | H2FeO4 кислота, в свободном состоянии не выделена | |
| Соли | FeCl2, FeSO4, Fe(NO3)2 и др. | Тип I FeCl3 | Тип II KFeO2 | K2FeO4 BaFeO4 SrFeO4 ферраты (IV) |
|
|
|
Способы получения железа
1. Техническое железо (в сплаве с углеродом и другими примесями) получают карботермическим восстановлением его природных соединений по схеме:

Восстановление происходит постепенно, в 3 стадии:
1) 3Fe2O3 + СО = 2Fe3O4 + СO2
2) Fe3O4 + СО = 3FeO +СO2
3) FeO + СО = Fe + СO2
Образующийся в результате этого процесса чугун содержит более 2% углерода. В дальнейшем из чугуна получают стали - сплавы железа, содержащие менее 1,5 % углерода.
2. Очень чистое железо получают одним из способов:
а) разложение пентакарбонила Fe
Fe(CO)5 = Fe + 5СО
б) восстановление водородом чистого FeO
FeO + Н2 = Fe + Н2O
в) электролиз водных растворов солей Fe+2
FeC2O4 = Fe + 2СO2
оксалат железа (II)
Химические свойства
Fe - металл средней активности, проявляет общие свойства, характерные для металлов.
Уникальной особенностью является способность к «ржавлению» во влажном воздухе:
4Fe + 6Н2O + 3O2 = 4Fe(OH)3
В отсутствие влаги с сухим воздухом железо начинает заметно реагировать лишь при Т > 150°С; при прокаливании образуется «железная окалина» Fe3O4:
3Fe + 2O2 = Fe3O4
В воде в отсутствие кислорода железо не растворяется. При очень высокой температуре Fe реагирует с водяным паром, вытесняя из молекул воды водород:
|
|
|
3 Fe + 4Н2O(г) = 4H2
Процесс ржавления по своему механизму является электрохимической коррозией. Продукт ржавления представлен в упрощенном виде. На самом деле образуется рыхлый слой смеси оксидов и гидроксидов переменного состава. В отличие от пленки Аl2О3, этот слой не предохраняет железо от дальнейшего разрушения.
Виды коррозии
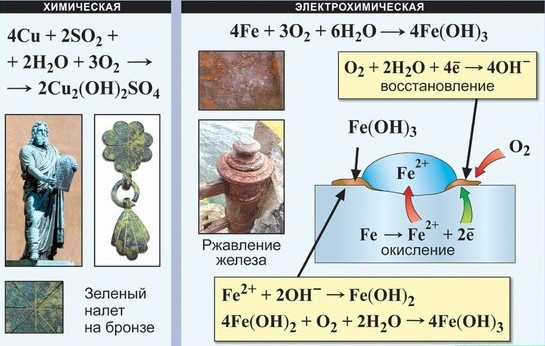
Защита железа от коррозии

Взаимодействие с галогенами и серой при высокой температуре.
2Fe + 3Cl2 = 2FeCl3
2Fe + 3F2 = 2FeF3
2Fe + 3Br2 = 2FeBr3
Fe + I2 = FeI2
Fe + S = FeS
Образуются соединения, в которых преобладает ионный тип связи.
2. Взаимодействие с фосфором, углеродом, кремнием (c N2 и Н2 железо непосредственно не соединяется, но растворяет их).
Fe + Р = FexPy
Fe + C = FexCy
Fe + Si = FexSiy
Образуются вещества переменного состава, т к. бертоллиды (в соединениях преобладает ковалентный характер связи)
3. Взаимодействие с «неокисляющими» кислотами (HCl, H2SO4 разб.)
Fe0 + 2Н+ → Fe2+ + Н2↑
Поскольку Fe располагается в ряду активности левее водорода (Е°Fe/Fe2+ = -0,44В), оно способно вытеснять Н2 из обычных кислот.
Fe + 2HCl = FeCl2 + Н2↑
Fe + H2SO4 = FeSO4 + Н2↑
|
|
|
4. Взаимодействие с «окисляющими» кислотами (HNO3, H2SO4 конц.)
Fe0 - 3e- → Fe3+
Концентрированные HNO3 и H2SO4 «пассивируют» железо, поэтому при обычной температуре металл в них не растворяется. При сильном нагревании происходит медленное растворение (без выделения Н2).
В разб. HNO3 железо растворяется, переходит в раствор в виде катионов Fe3+ а анион кислоты восстанавливется до NO*:
Fe + 4HNO3 = Fe(NO3)3 + NO↑ + 2Н2O
Очень хорошо растворяется в смеси НСl и HNO3
Отношение к щелочам
В водных растворах щелочей Fe не растворяется. С расплавленными щелочами реагирует только при очень высоких температурах.
Дата добавления: 2018-10-27; просмотров: 172; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!
