Систематический и дробный качественный анализ
Тесты по качественному анализу
Аналитическая химическая реакция
1. Аналитическая химическая реакция - это реакция, сопровождающаяся
а) изменением окраски раствора
б) определенным аналитическим эффектом за счет образования продукта
реакции, обладающего специфическими свойствами
в) растворением осадка
г) образованием осадка
2. Микрокристаллоскопическая реакция сопровождается образованием
а) кристаллов характерной формы
б) кристаллического осадка
в) мелкокристаллического осадка
г) окрашенных кристаллов
3. Селективность аналитической реакции можно повысить
а) добавлением щелочи
б) применяя химически чистые реактивы
в) варьируя pH раствора
г) маскируя мешающие ионы
4. Специфические аналитические реакции - это реакции
а) идущие до конца
б) с помощью которых в данных условиях можно обнаружить только одно вещество
в) с помощью которых можно обнаружить все вещества в данных условиях
комплексообразования
г) осаждения
5. Аналитическими сигналами в качественном анализе являются
а) изменение окраски раствора
б) образование осадка
в) точка эквивалентности
г) исчезновение окраски раствора
6. При работе с пробой объемом 0,01 - 0,1 см3 и массой 0,001 - 0,01 г используют
а) макрометод
б) ультрамикрометод
в) микрометод
г) полумикрометод
7. Требования к качественной аналитической химической реакции
|
|
|
а) наличие аналитического эффекта
б) полнота протекания
в) чувствительность
г) избирательность
8. Повысить чувствительность аналитической химической реакции можно
а) уменьшив концентрацию реагентов
б) увеличив концентрации реагентов
в) применяя аналитическое концентрирование
г) маскированием посторонних ионов
9.Для понижения предела обнаружения используют
а) разбавление растворов
б) каталитические реакции
в) реакции на носителях
г) абсолютное концентрирование
10. Аналитическую химическую реакцию можно сделать избирательной путем
а) уменьшения концентрации реагентов
б) применения маскирующих агентов
в) относительного концентрирования
г) экстракции
Типы аналитических химических реакций
11. Реакции, используемые в качественном анализе, приводящие к распределению определяемого компонента между двумя фазами
а) эндотермические
б) экстракционные
в) ионного обмена
г) комплексообразования
12. Тип аналитической химической реакции
NaСl + K[Sb(OH)6] → Na[Sb(OH)6] + KCl
а) обмена ионов
б) комплексообразования
в) осаждения
г) окисления-восстановления
13. Тип аналитической химической реакции
[Ag(NH3)2]Cl + 2HNO3 → AgCl + 2NH4NO3
|
|
|
а) обмена ионов
б) комплексообразования
в) окисления-восстановления
г) осаждения
14. Тип аналитической химической реакции
CuSO4 + 4NH4OH → [Cu(NH3)4]SO4 + 4H2O
а) обмена ионов
б) осаждения
в) комплексообразования
г) окисления-восстановления
15. Тип аналитической химической реакции
PbS + 4H2O2 → PbSO4 + 2H2O
а) обмена ионов
б) осаждения
в) комплексообразования
г) окисления-восстановления
16. Тип аналитической химической реакции
2 CoСl2 + 12 KCN + Cl2 → 2 K3[Co(CN)6] + 6 KCl
а) обмена ионов
б) окисления-восстановления
в) комплексообразования
г) осаждения
17. Окислительно-восстановительные аналитические химические реакции
а) fNaСl + K[Sb(OH)6] → Na[Sb(OH)6] + KCl
б) 6 FeSO4 + K2CrO4 + 7 H2SO4→ 3Fe2(SO4)3 + Cr2(SO4)3 + K2SO4 + 7 H2O
в) AlСl3 + 6 KOH → K3[Al(OH)6] + 6 KCl
г) [Cu(NH3)4]SO4 + K2S → CuS + 4 NH3 + K2SO4
18. Аналитические химические реакции осаждения
а) NaСl + K[Sb(OH)6] → Na[Sb(OH)6] + KCl
б) 6FeSO4 + K2CrO4 + 7H2SO4 → 3Fe2(SO4)3 + Cr2(SO4)3 + K2SO4 + 7H2O
в) AlСl3 + 6KOH → K3[Al(OH)6] + 6KCl
г) [Cu(NH3)4]SO4 + K2S → CuS + 4NH3 + K2SO4
19. Стадии комбинированной аналитической реакции
2AsO 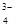 + 5H2S + 6H → As2S3 + 8H2O + 2S
+ 5H2S + 6H → As2S3 + 8H2O + 2S
а) окисление-восстановление; комплексообразование
б) окисление-восстановление; осаждение
в) растворение; окисление-восстановление
г) нейтрализация; комплексообразование
|
|
|
20. Стадии комбинированной аналитической реакции
As2S3 + 14H2O2 + 12NH3 → 2AsO 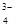 + 3SO
+ 3SO 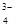 + 12NH
+ 12NH 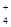 + 8H2O
+ 8H2O
а) нейтрализация; комплексообразование
б) окисление-восстановление; осаждение
в) окисление-восстановление; комплексообразование
г) окисление-восстановление; растворение
Аналитические реактивы
21. Аналитические реактивы – химические вещества, предназначенные для
а) проведения химических опытов
б) поддерживания постоянного значения pH растворов
в) использования в аналитических, учебных и научно-исследовательских целях
г) приготовления растворов
22. Согласно кислотно-основной классификации групповым реактивом II аналитической группы катионов является
а) Na2CO3
б) H2S
в) H2S + HCl
г) HCl
23. Согласно кислотно-основной классификации групповым реактивом Ш аналитической группы катионов является
а) Na2CO3
б) H2SО4
в) HCl
г) NH4OH
24. Согласно кислотно-основной классификации групповым реактивом V аналитической группы катионов является
а) Na2CO3
Б) NaOH
в) HCl
г) NH4OH
25. Реактивы, с помощью которых можно обнаружить ионы железа (III) в водном растворе, в отсутствии мешающего влияния других ионов
а) K3[Fe(CN)6]
б) (NH4)2SO4
в) NH4SCN
г) KI
26. Реактивы, с помощью которых можно обнаружить ионы железа (II) в водном растворе, в отсутствии мешающего влияния других ионов
|
|
|
а) K3[Fe(CN)6]
б) K4[Fe(CN)6]
в) NH4SCN
г) KI
27. Реактивы, с помощью которых можно обнаружить ионы меди (II) в водном растворе, в отсутствии мешающего влияния других ионов
а) NH3
б) FeC13
в) ZnSO4
Г) KI
28. Реактив для определения ионов аммония
а) NaNO3
б) Na2HPO4
в) К2[HgI4] + КОН
г) Na3PO4
29. Соответствие между катионами и реактивами, используемыми для их обнаружения Катион Реактив
а) Ba2+ K2Cr2O7
б) Sr2+ NaCl
в) Ca2+ (NH4)2C2O4
г) Са2+ (NH4)2SO4
30. Соответствие между катионами и реактивами, используемыми для их обнаружения Катион Реактив
а) Ni2+ H2S
б) Zn2+ NaOH + Br2
в) Co2+ NH4SCN
г) Со2+ HNO3
Систематический и дробный качественный анализ
31. При систематическом анализе смеси катионов I и II аналитических групп по кислотно-основной классификации присутствие катионов II аналитической группы устанавливают добавлением раствора
а) Na2НРО4
б) H2S
в) HCl
г) NH4OH
32. При систематическом анализе смеси катионов I, II и III аналитических групп по кислотно-основной классификации отделение катионов III аналитической группы проводят добавлением раствора
а) Na2НРО4
б) H2SО4
в) HCl
г) NH4OH
33. При анализе выделенной смеси катионов III и IV аналитической группы отделение катионов хрома, алюминия и цинка проводят добавлением избытка раствора
а) Na2НРО4
б) H2S
в) HCl
г) NaOH
34. При систематическом анализе выделенной смеси катионов V и VI аналитической групп по кислотно-основной схеме, после выделения VI группы катионов действием NH3+NH4Cl отделение от ионов меди (II) и ртути (II) проводят добавлением раствора
а) Na2НРО4
б) H2S
в) HCl
г) NH4OH
35. При систематическом анализе смеси анионов I аналитической группы выделение ионов хлорида, бромида и иодида осуществляют добавлением водного раствора
а) NH3
б) NаOH
в) K3[Co(NO2)6]
г) AgNO3 + HNO3
36. При анализе смеси осадков AgCl, AgBr и AgI – отделение хлорид- и бромид-ионов от иодид-ионов осуществляют добавлением 25%-ного водного раствора
а) Н2SO4
б) NH3
в) HNO3
г) NаOH
37. Диметилглиоксим используют для обнаружения ионов никеля(II) в присутствии ионов железа(III) при условии добавления в исследуемый раствор
а) Н2SO4
б) NH3
в) KI
г) NаOH
38. При систематическом анализе смеси катионов I аналитической группы определению ионов аммония реактивом Несслера мешают ионы
а) Li +
б) Na+
в) Mg 2+
г) K+
39. Для обнаружения сульфат-ионов дробным способом используют реактив
а) BaCl2 + HCl
б) CaCl2 + HCl
в) MnCl2 + HCl
г) MgCl2 + HCl
40. Для обнаружения фосфат-ионов в пробе минерализата свободного от арсенатов дробным способом используют реактив
а) гипсовую воду
б) хлорид бария
в) бромную воду
г) молибденовую жидкость
Дата добавления: 2018-09-22; просмотров: 1406; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!
