По формуле Элея определить температуру вспышки бензола
В закрытом тигле
Решение:Для расчета по формуле(4.5) необходимо знать температуру кипения бензола (С6Н6) и значение коэффициента К. Температура кипения бензола 353К или 800С. Величину К определим по формуле (4.6):
К=4∙6+6=30
Определим искомую величину температуры вспышки:
tBC=80-18  -18,60 илими254,4 К.
-18,60 илими254,4 К.
Согласно справочным данным, температура вспышки бензола равно 259К. Определим ошибка расчета:
∆  ∙100=-1,3%
∙100=-1,3%
Результат расчета занижен менее чем на 2 %.
Контрольные задачи
1. По формуле Блинова определить температуру вспышки в открытом сосуде уксуснометилового эфира.
2. По формуле Блинова рассчитать температуру воспламенения бензола.
3. По формуле Элея рассчитать температуру вспышки 2-метилгексана (tкип=90).
4. Рассчитать температуру вспышки в закрытом тигле стирола (С8Н8)по формуле Блинова и Элея. Оценить точность расчета, если tBCстирола по справочным данным равна 303 К.
5. Определить температуру вспышки в закрытом тигле акриловой кислоты по формуле Блинова и Элея.
Домашнее задание 5
Рассчитать температуру вспышки (воспламенения) i-того вещества по формуле В.И. Блинова и Элея. Значение Д0 взять из справочной литературы или определить по формуле (4.4). Сравнить вычисление значения температуры вспышки (воспламенения) с имеющимися справочными данными и оценить погрешность расчета (табл.4.3).
Таблица 4.3.
| Вариант | Горючее вещество | Химическая формула | Определяемая величина Т-температура |
| 1 | Уксусный альдегид | С2Н4О | Т вспышки в закрытом тигле |
| 2 | Ацетон | С3Н6О | Т воспламенения |
| 3 | Пропилбензол | С9Н12 | Т вспышки в открытом тигле |
| 4 | Окись этиленан | С2Н4О | Т воспламенения |
| 5 | Сероуглерод | С S2 | Т воспламенения |
| 6 | Метиловый спирт | СН4О | Т вспышки в закрытом тигле |
| 7 | Толуол | С7Н8 | Т воспламенения |
| 8 | Этилбензол | С8Н1`0 | Т воспламенения |
| 9 | Диэтиловый эфир | (С2Н5)2О | Т вспышки в открытом тигле |
| 10 | Метилэтилкетон | С4Н8О | Т воспламенения |
| 11 | Бутилформиат | С5Н10О2 | Т вспышки в открытом тигле |
| 12 | Амиловый спирт | С5Н12О | Т вспышки в открытом тигле |
| 13 | Бутиловый спирт(третичный) | С2Н10О | Т воспламенения |
| 14 | 2-метилбутан | С5Н12 | Т вспышки в закрытом тигле |
| 15 | Октан | С8Н18 | Т воспламенения |
| 16 | Этилциклопентан | С7Н14 | Т воспламенения |
| 17 | Уксуснопропиловый эфир | С5Н12О | Т вспышки в закрытом тигле |
| 18 | Уксусно этиловый эфир | С4Н10О | Т воспламенения |
| 19 | Пропиловый спирт | С3Н8О | Т воспламенения |
| 20 | Бутилбензол | С10Н14 | Т вспышки в открытом тигле |
Расчет стандартной температуры самовоспламенения
Температура воспламенения – наименьшая температура вещества, при которой пары над поверхностью горючего вещества выделяются с такой скоростью, что при воздействии на них источника зажигания наблюдается воспламенение. Воспламенение – пламенное горение вещества, инициированное источником зажигания и продолжающееся после его удаления, то есть возникает устойчивое горение
Температура вспышки – наименьшая температура горючего вещества, при которой пары над поверхностью горючего вещества способны вспыхивать при контакте с открытым источником огня; устойчивое горение при этом не возникает. Вспышка – быстрое сгорание газопаровоздушной смеси над поверхностью горючего вещества, сопровождающееся кратковременным видимым свечением. Как правило, при отсутствии указания на метод измерения используется метод Пенски-Мартенса.
По температуре вспышки из группы горючих жидкостей выделяют легковоспламеняющиеся. Легковоспламеняющимися называются горючие жидкости с температурой вспышки не более 61 °C в закрытом тигле (з.т.) или 66 °C в открытом тигле (о.т.).
Температу́ра самовоспламене́ния – наименьшая температура горючего вещества, при нагреве до которой происходит резкое увеличение скорости экзотермических объёмных реакций, приводящее к возникновению пламенного горения и/или взрыва. Эта температура требуется для достижения энергии активации реакции горения.
Измерение.Из-за сложностей прямого измерения температуры самовоспламенения газов и паров, за неё принимают минимальную температуру стенки реакционного сосуда, при которой наблюдают самовоспламенение. Эта температура зависит от условий тепломассообмена как внутри реакционного сосуда, так и самого сосуда с окружающей средой, объёма смеси, а также каталитической активности стенки сосуда и ряда других параметров.
Показатель применяется для определения допустимой температуры нагревания горючих веществ, электрического и технологического оборудования, а также для установления группы взрывоопасной смеси. Для измерения температуры самовоспламенения жидкостей используют метод ASTM E 659 и метод Кливленда ASTM D92 (ГОСТ 4333).
Общеизвестна температура самовоспламенения бумаги: 451 °F, или 233 °C, благодаря знаменитому роману Рэя Брэдбери «451 градус по Фаренгейту», в заглавие которого и вынесено это значение.
Энергия активации в химии и биологии – минимальное количество энергии, которую требуется сообщить системе (в химии выражается в джоулях на моль), чтобы произошла реакция. Термин введён Сванте Августом Аррениусом в 1889. Типичное обозначение энергии реакции Ea.
Энергия активации в физике – минимальное количество энергии, которое должны получить электроны донорной примеси, для того чтобы попасть в зону проводимости.
В химической модели, известной как Теория активных соударений (ТАС), есть три условия, необходимых для того, чтобы произошла реакция:
Молекулы должны столкнуться. Это важное условие, однако его не достаточно, так как при столкновении не обязательно произойдёт реакция.
Молекулы должны обладать необходимой энергией (энергией активации). В процессе химической реакции взаимодействующие молекулы должны пройти через промежуточное состояние, которое может обладать большей энергией. То есть молекулы должны преодолеть энергетический барьер; если этого не произойдёт, реакция не начнётся.
Молекулы должны быть правильно ориентированы друг относительно друга. При низкой (для определённой реакции) температуре большинство молекул обладают энергией меньшей, чем энергия активации, и неспособны преодолеть энергетический барьер. Однако, в веществе всегда найдутся отдельные молекулы, энергия которых значительно выше средней. Даже при низких температурах большинство реакций продолжают идти. Увеличение температуры позволяет увеличить долю молекул, обладающих достаточной энергией, чтобы преодолеть энергетический барьер. Таким образом, повышается скорость реакции.
Расчет температуры воспламенения проводят в следующей последовательности.
1. Определяют количество углеродных цепей:
м = МР (МР-1):2 (4.8)
где м-общее число молей
МР- количество функциональных групп в молекуле горючего вещества –СН, -ОН, фенильная группа может быть как концевой, так и в середине цепи.
2. Определяют длину каждой цепи(количество атомов углерода) и длину цепи:
𝜄cp=  (4.9),
(4.9),
где 
При определении  надо иметь в виду, что группа ОН удлиняет цепь, а фенильная группа уменьшает ее на один атом углерода.
надо иметь в виду, что группа ОН удлиняет цепь, а фенильная группа уменьшает ее на один атом углерода.
3. По табл.8-10 приложения по средней длине цепи определяют температуру самовоспламенения. Температуру самовоспламенения можно также рассчитать по формуле:
tс = 300+116 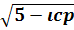 при 𝜄cp≤5 (4.10)
при 𝜄cp≤5 (4.10)
tс = 300-38 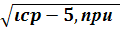 𝜄cp≥5 (4.11)
𝜄cp≥5 (4.11)
Примеры решения задач
Дата добавления: 2018-08-06; просмотров: 2601; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!
