Кальциферолы(производные вит D)
Карденолиты – сердечные гликозиды. Классификация. Связь между строением и биологическим действием. Стандартизация сердечных гликозидов. Факторы влияющие на стабильность. Методы идентификации и кол опред кардиотонич стероидов. Фармакопейный метод анализа дигитоксина
КАРДЕНОЛИДЫ — группа кардиотонических стероидных гликозидов, содержащих пятичленное лактонное кольцо с одной двойной связью.
Образуются при ферментативном или кислом гидролизе соответствующих гликозидов.

В зависимости от заместителя в положении C10 карденолиды подразделяются на три подгруппы.
1.Подгруппа наперстянки включает гликозиды, агликоны которых в положении С10 имеют метильную группу - СН3. Гликозиды этой подгруппы медленно всасываются и медленно выводятся из организма, обладают кумулятивным действием, например гликозид гитоксигенин.

2. Подгруппа строфанта - агликон имеет в положении 10 альдегидную группу -С-OH. Эти гликозиды быстро всасываются, быстро выводятся из организма и не обладают кумулятивным действием, например строфантидин.

3. Подгруппа объединяет сердечные гликозиды, имеющие в положении 10 спиртовую группу (-OН2OН):

Количественное определение.
Проводится различными методами: фотоколометрическим, спектрофотометрическим, флюориметрическим, газожидкостной хроматографии и биологической стандартизации.
НТД на лекарственное растительное сырье, содержащее сердечные гликозиды, требует обязательной стандартизации сырья биологическими методами, которая проводится на лягушках, кошках, голубях. Активность оценивают по сравнению со стандартным кристаллическим препаратом и выражают в единицах действия (лягушачьих, кошачьих и голубиных). Чаще других используется стандартизация на лягушках. За единицу (1 ЛЕД) принято наименьшее количество испытуемого вещества, способное вызвать систолическую остановку сердца у животных в течение 1 ч. Для биологической стандартизации используют лягушек массой 25-40 г, предпочтительно самцов. Стандарты изготовляют и выпускают специализированные научно-исследовательские организации. В НТД на лекарственное растительное сырье, содержащее сердечные гликозиды, обязательно указывается валор. Валер сырья - это количество единиц действия в 1 г сырья. Например, при испытании на лягушках в 1 г листьев наперстянки пурпуровой должно содержаться не менее 50-66 ЛЕД, в траве ландыша майского - 120 ЛЕД, а в цветках ландыша - 200 ЛЕД. При испытании кардиотонических средств на кошках или голубях активность выражают в кошачьих и голубиных единицах действия: КЕД и ГЕД. Гликозиды действуют на сердце в 5-6 раз сильнее, чем их агликоны.
|
|
|
Все реакции на сердечные гликозиды можно разделить на 3 группы:
|
|
|
1) реакции на углеводную часть молекулы (2-дезоксисахара) (реакция Келлер — Килиани);
2) реакции на стероидное ядро (реакция Либермана — Бурхарда; реакция Розенгейма и др.;
3) реакции на лактонное ненасыщенное кольцо.
Для установления наличия пятичленного лактонного кольца проводятся реакции: Легаля (с нитропруссидом натрия); Раймонда (с 3,5-динитробелзолом); Кедде (с 3,5-динитробензойной кислотой); Балье (с пикриновой кислотой). Реакции проводятся в щелочной среде.
Анализ дигитоксина
Подлинность. К раствору 1-2 мг препарата в 1 мл 95% спирта прибавляют I мл раствора нитропруссида натрия и 1-2 капли раствора едкого натра; появляется постепенно исчезающее красное окрашивание.
К раствору 1-2 мг препарата в 1 мл 95% спирта прибавляют 1 мл 1% спиртового раствора м-динитробензола и 2 капли раствора едкого натра; появляется постепенно исчезающее красно-фиолетовое окрашивание.
1-2 мг препарата растворяют в 2 мл ледяной уксусной кислоты, содержащей 0,05% хлорида окисного железа. Полученный раствор осторожно по стенке вливают в пробирку с 2 мл концентрированной серной кислоты; на границе двух слоев появляется бурое окрашивание. Верхний ч;лой постепенно окрашивается в сине-зеленый или синий цвет.
|
|
|
кальциферолы(производные вит D)
В природных продуктах содержится провитамины D2 и D3-эргостерин и холестерин.
Эргостерин-одноатомн.ненасыщ.циклич спирт.в основе - циклопентан пергидрофенантрен.Под действием УФ излучения превращается в D2.

 Предшественник вит D3-7-дегидрохолестерин.кот под действием УФ ИЗЛУЧЕНИЯ превращается в вит D3.(Это писать не надо!!!!!Дегидрохолестерин-такой же как эргостерин но без СН3 в 25 положении и в 23-24 положении нет двойной связи.)
Предшественник вит D3-7-дегидрохолестерин.кот под действием УФ ИЗЛУЧЕНИЯ превращается в вит D3.(Это писать не надо!!!!!Дегидрохолестерин-такой же как эргостерин но без СН3 в 25 положении и в 23-24 положении нет двойной связи.)
7-Дегодрохолестерин---->( УФ)--> витамин D3 (холекальциферол)
Вит Д2 :бесцвет или слегка желтоват. кристаллы без зап.Практич НР в воде.ЛР в этанол, хлороформе,ацетоне,ацетоне,эфире.
Вит Д3 :бесцвет кристаллы или бел кристаллический. пор без зап.Практич НР в воде.Р в этанол, хлороформе,ацетоне,,эфире.
Подлинность:1)р-ция либермана:в-ва растворяют в хлороформе+укс ангидрид и серн.кту.появл красное окрашив.кот переходит в фиолет.затем в синее и зеленое.
2)р-ция с сурьмой в хлороформе. на эргостерин : -С=С- --(Sb3+)->-С=(<--(Sb3+))С- оранжевое окрашивание.Химизм этой р-ция основан на образ межмолекулярного комплекса с переносом заряда.
|
|
|
3) р-ция на эргокальциферол с 3,5-динитробензоилхлоридом(в среде безводного пиридина при нагревании на вод бане. ) полученный после перекристаллизации эргокальцифирил- 3,5-динитробензоат изменяет темпер плавл. Эргокальциферол+(NO2)2-C6H5-C (=O)-Cl --> (NO2)2-C6H5-C (=O)-O-эргокальциферол
4)на эргокальциферол с этанолом при добавлении серн.кислоты красное окрашивание :эргокальциферол +этанол -->замещение по ОН группе
Эргокальциферол и его производные.испытывают на микробов чистоту.на наличие примесей (методом ТСХ).восстанавливающ в-ва и эргостерин.
Колич.определение -спектоофотометрия .Растворитель -этанол.
Хранят по сп Б.вгерметически укупоренных доверху заполненных склонах оранжевое стекла а сухом защищенном от света месте
Производные прегнана. Кортикостероиды. Зависимость между строением и биологическим действием: минералкортикоиды и глюкокортикоиды. ЛС: дезоксикортона ацетат, картизона ацетат, гидрокартизона ацетат, преднизолон. Фторзамещенные вещества: дексаметазон. Требования к качеству и методы анализа.

В реакция рекомендуемых для оценки качества много общего. 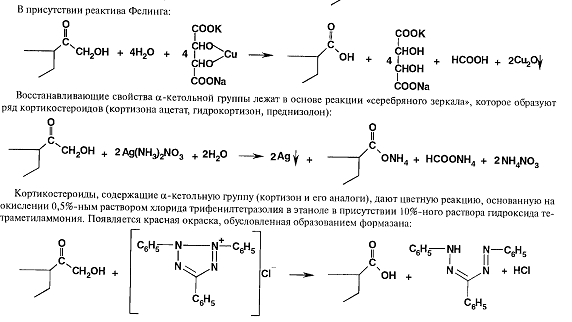

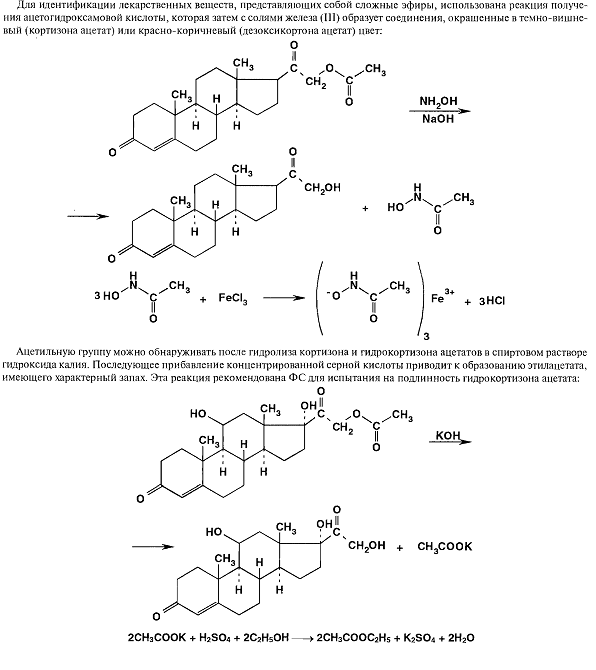


В результате исследования влияния галогенов, введенных в молекулу кортикостероидов, на их фармокологическуюактивность были синтезированы моно- и дифторпроизводные преднизолона. 
Химические свойства кортикостероидов определяются наличием αβ-ненасыщенной кетоннойгруппировки в кольце А и α-кетонной группировки в боковой цепи кольца D. Кетогруппа и гидроксил в положении 11 из-за стерических препятсвий довольно инертны ( не образуют гидразонов, семикарбазонов, не ацилируются)
Спектрофотометрия в ультрофиолетовой области и ее использование в анализе витаминов и стероидных гормонов. Характеристика дезоксикортона ацетата (дезоксикортикостерона ацетата), кортизона ацетата как фарм субст гф. Фармакопейный метод количественного определения преднизолона и таблеток преднизолона.
Образец анализируемого вещества при спектрофотометрических определениях обычно растворяют в соответствующем растворителе. Для этих областей пригодны многие растворители, в том числе вода, спирты, хлороформ, низшие углеводороды, эфиры, разведенные растворы аммиака.
Спектрофотометрический анализ по непосредственному измерению оптической плотности может быть проведен для веществ, обладающих лишь определенными особенностями строения (ароматические соединения, соединения с сопряженными кратными связями, соединения ряда металлов и др.).
Для определения концентрации растворов спектрофотометрический путем используется закон Бугера — Ламберта — Бера в форме:
В ряде случаев даже при использовании монохроматического излучения могут наблюдаться отклонения от закона Бугера — Ламберта — Бера, обусловленные процессами диссоциации, ассоциации и комплексообразования.
Эффективным методом, позволяющим обеспечить количественный контроль содержания витаминов в многокомпонентных объектах, является высокоэффективная жидкостная хроматография (ВЭЖХ) - универсальный аналитический метод разделения и определения компонентов сложных смесей. Метод ВЭЖХ незаменим при анализе термически и химически лабильных жирорастворимых витаминов (ЖРВ) групп A, D, Е и К. Основан на элюировании их неполярными органическими растворителями после сорбции на полярных сорбентах. Однако такой вариант ВЭЖХ не обеспечивает эффективного разделения сложных смесей, с полным набором жирорастворимых витаминов(A, D, Е) в пробах с водосодержащей матрицей, так как даже небольшие количества воды могут негативно влиять на воспроизводимость результатов.
 Дезоксикортикостерон-ацетат— белый или белый с кремовым оттенком кристаллический порошок без запаха, т. пл. 154—160°. Растворим в хлороформе, ацетоне, диоксане и спирте, не растворим в воде.
Дезоксикортикостерон-ацетат— белый или белый с кремовым оттенком кристаллический порошок без запаха, т. пл. 154—160°. Растворим в хлороформе, ацетоне, диоксане и спирте, не растворим в воде.
Восстанавливает аммиачный раствор нитрата серебра и окрашивается концентрированной серной кислотой; при прибавлении хлороформа последний окрашивается в оранжевый цвет с красной флуоресценцией, водный слой окрашивается в зеленоватый цвет.
Подлинность.
0,01 г препарата растворяют в I мл метилового спирта, прибавляют 1 мл реактива Фелинга и нагревают на водяной бане; образуется оранжево-красный осадок.
2 мг препарата растворяют в 2 мл концентрированной серной кислоты. Прибавляют 1,5 мл воды, встряхивают, добавляют еще 1,5 мл воды и вновь встряхивают. Появляется вишневое окрашивание с зеленовато-коричневой флюоресценцией. Раствор охлаждают, приливают 3 мл хлороформа и энергично встряхивают; нижний слой окрашивается в желтый цвет, верхний - в зеленый.
0,03 г препарата растворяют в 1 мл спирта, прибавляют 1 мл щелочного раствора гидроксиламина, встряхивают и оставляют на 5 минут. Затем добавляют 2 мл разведенной соляной кислоты, встряхивают и приливают 0,5 мл 10% раствора хлорида окисного железа в 0,1 н. растворе соляной кислоты; появляется красно-коричневое окрашивание.
 Кортизона ацетат
Кортизона ацетат
Cortisonum aceticum
Прегнен-4-диол-17альфа, 21-триона-3,11,20 21-ацетат
Описание.Белый или белый со слабым желтоватым оттенком кристаллический порошок.
Растворимость. Практически нерастворим в воде, очень мало растворим в 95% спирте, легко растворим в хлороформе, трудно растворим в ацетоне.
Подлинность.1 мг препарата растворяют в 1 мл метилового спирта, прибавляют 5 мл раствора сульфата фенилгидразина и нагревают на водяной бане; через 5 минут появляется желтое окрашивание.
0,01г препарата растворяют в 1 мл метилового спирта, прибавляют
1 млреактива Фелинга и нагревают на водяной бане; образуется крас
но-оранжевый осадок.
1 мгпрепарата растворяют в 2 мл концентрированной серной кислоты; постепенно появляется желтое окрашивание (отличие от преднизо-лона). Через 15-20 минут раствор просматривают в ультрафиолетовом свете; наблюдается желтая флюоресценция (отличие от преднизона).
0,01г препарата растворяют в 2 мл метилового спирта и прибавляют
2 млщелочного раствора гидроксиламина. Встряхивают в течение 3-5
минут, прибавляют 2 мл разведенной соляной кислоты и 0,5 мл 10% раствора хлорида окисного железа в 0,1 н. растворе соляной кислоты; появляется темно-вишневое окрашивание.
Количественное определение. Измеряют оптическую плотность 0,001% раствора препарата в 95% спирте на спектрофотометре при длине волны 238 нм в кювете с толщиной слоя 1 см. Повторяют такое же измерение с 0,001% раствором стандартного образца кортизона ацетата.
Преднизолон
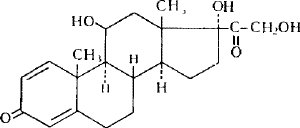 Для количественного определения преднизолона нами предлагается спектрофотометрическая методика. Липосомы разрушают под действием раствора тритона Х-100, преднизолон экстрагируют метиловым спиртом, измеряют оптическую плотность экстракта при длине волны 242 нм. Расчет содержания проводят с использованием значения удельного показателя поглощения преднизолона (415). Среднее содержание преднизолона в липосомах составило 0,4 %. Погрешность определения не превышала 3 %.
Для количественного определения преднизолона нами предлагается спектрофотометрическая методика. Липосомы разрушают под действием раствора тритона Х-100, преднизолон экстрагируют метиловым спиртом, измеряют оптическую плотность экстракта при длине волны 242 нм. Расчет содержания проводят с использованием значения удельного показателя поглощения преднизолона (415). Среднее содержание преднизолона в липосомах составило 0,4 %. Погрешность определения не превышала 3 %.
Таблетки преднизолона:
Количественное определение. 0,06-0,07 г (точная навеска) порошка растертых таблеток помещают в небольшой стакан, прибавляют 10 мл метилового спирта и растворяют преднизолон при легком подогревании на водяной бане и помешивании палочкой в течение 10 минут По охлаждении декантируют раствор через стеклянный фильтр № 3 (без вакуума) в мерную колбу емкостью 100 мл с притертой пробкой. Стакан промывают метиловым спиртом, декантируя каждый раз через тот же фильтр. Объем раствора доводят метиловым спиртом до метки и хорошо перемешивают. Измеряют оптическую плотность полученного раствора на спектрофотометре при длине волны 242 нм в кювете с толщиной слоя 1 см. В качестве контрольного раствора применяют метиловый спирт.
Содержание преднизолона в одной таблетке в граммах (X) вычисляют по формуле:
X = (D*б)/415*a
Дата добавления: 2018-06-01; просмотров: 1571; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!
