Химизм обжига цинковых концентратов
Лекция №12. МЕТАЛЛУРГИЯ ЦИНКА, Технологические схемы производства цинка.
Переработка цинковых руд началась в глубокой древности при выплавке латуни (сплав цинка с медью). В настоящее время производство цинка по масштабам уступает только производству железа, алюминия и меди. Значительная доля цинка расходуется на оцинкование железа (от 30 до 50 % потребляемого цинка). Антикоррозионные цинковые покрытия наносят на листы, трубы, проволоку. Оцинковывают также аппаратуру, фермы мостов, перекрытия зданий и многие другие конструкции.
В промышленности широкое применение находят сплавы цинка с другими цветными металлами (40- 50%). Наиболее широко используют латуни и бронзы. Низкая температура плавления и хорошие литейные свойства сплавов на основе цинка позволяют отливать из них под давлением сложные изделия высокой прочности с хорошим качеством поверхности. Изделия, получаемые литьем под давлением, широко используют в авиационной, автомобильной и других отраслях промышленности.
Цинковый прокат, на который тратится 5-10 % Zn, применяют для изготовления сухих батарей, типографских плит и строительных конструкций. Оксид цинка (~10 % от цинка) расходуют на производство цинковых белил, используют в производстве резины для улучшения ее качества. Цинк в виде цинковой пыли применяют как реагент в производстве свинца, благородных и других цветных металлов, а также в химической промышленности.
Технологические схемы производства цинка.
Пирометаллургия цинка сохранилось в небольших масштабах. Технологическая схема (рис.11.1) цинковых дистилляционных заводов включает операции: обжиг, восстановление с отгонкой и конденсацией цинка, рафинирование цинка ректификацией.

Рис.12.1 Технологическая схема пирометаллургического производства цинка.
В настоящее время схема дистилляции применяется в ограниченных масштабах. Однако основы процессов дистилляции цинка используются в других технологических процессах при переработке сложного комплексного сырья. В процессе шахтной плавки по способу фирмы «Империэл смэлтинг» совмещены технологии получения чернового свинца собирающегося во внутреннем горне печи и отгонки паров цинка с отходящими газами. Пары цинка из газов конденсируются в виде жидкого металла.
Цинковые концентраты подвергаются спекающему обжигу на агломашинах с удалением серы в газы. Огарок в смеси с коксом поступает на высокотемпературное восстановление с отгонкой цинка (дистилляция) в горизонтальных или вертикальных ретортах, в шахтных электропечах или в рудно-термических печах. При этом цинк, имеющий низкую температуру кипения, в виде паров выносится из дистилляционного агрегата и конденсируется в виде расплава в специальных конденсаторах. Компоненты пустой породы и примеси концентрируются в остатке от дистилляции (раймовка) либо переходят в шлак, при плавке в рудно-термических печах. Более 65% цинка в мировом производстве получают на гидрометаллургических заводах. На рис.12.2 приведена принципиальная схема гидрометаллургического производства, включающая двухстадийное противоточное выщелачивание цинкового огарка. Цинковые сульфидные концентраты подвергаются окислительному обжигу в печах кипящего слоя при температурах 650-1050 оС. Огарок содержит 0,1-0,3% сульфидной серы и до 1,5% серы в виде сульфатов. Сульфатную серу в огарке оставляют для восполнения потерь серной кислоты в технологической схеме.
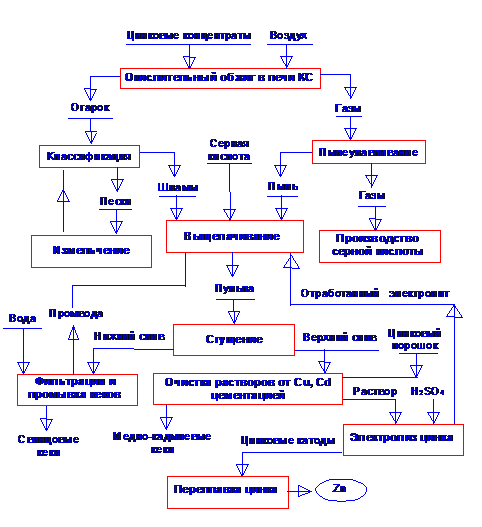
Рис.12.2 Технологическая схема гидрометаллургического производства цинка.
На первой стадии огарок поступает на нейтральное выщелачивание отработанными растворами последующей (кислой) стадии и промывными растворами. Полученная пульпа (смесь жидкого и твердого при соотношении (Ж:Т=10:1) направляется на сгущение в чанах-сгустителях. При нейтральном выщелачивании и сгущении происходит гидролитическая очистка раствора сульфата цинка от примесей трехвалентного железа, сурьмы и мышьяка. Компоненты пустой породы, сульфиды металлов и сульфат свинца не растворяются и концентрируются в остатке от выщелачивания. Полученный при сгущении раствор сульфата цинка подвергается контрольной фильтрации и направляется на медно-кадмиевую очистку.
Сгущенная пульпа нейтральных сгустителей (Ж:Т = 3:1) направляется во вторую стадию выщелачивания отработанным электролитом, содержащим 110-120 г/л свободной серной кислоты. На этой стадии добавляется свежий раствор кислоты. При повышенной кислотности на второй стадии происходит довыщелачивание огарка. Промывные воды являются оборотными в цикле выщелачивания, а кеки, снимаемые с фильтров, содержащие свинец и цинк, направляются на переработку вельцеванием.
Очистка растворов сульфата цинка от примесей меди, кадмия и кобальта проводится методом цементации на цинковом порошке. Получаемый медно-кадмиевый кек направляется в медно-кадмиевое производство, а очищенный раствор в электролизные ванны.
Электролиз растворов сульфата цинка проводится в ваннах с нерастворимыми свинцовыми анодами. При электролизе на катодах из холоднокатаного алюминия осаждается цинк. Металл после осаждения отделяется от катодной матрицы в виде тонких листов, промывается, пакетируется и с целью удаления поверхностной пленки оксидов подвергается переплавке в индукционных печах. Товарный цинк разливается в виде слитков и направляется потребителю.
Обжиг цинковых концентратов
Химизм обжига цинковых концентратов
Для процессов обжига характерны следующие семь основных реакций:
2 ZnS + 3 O2 = 2 ZnO + 2 SO2 + 890 кДж/моль
2 FeS2 + 5,5 O2 = Fe2O3 + 4 SO2 + 1673 кДж/моль
Эти две реакции обеспечивают протекание обжига без затраты топлива. Остаток сульфидной серы составляет 0,3%. Сульфидный цинк не извлекается ни при дистилляции, ни при выщелачивании.
Примерно 70% (не менее) железа вступает в реакцию с ZnO:
ZnO + Fe2O3 = ZnO. Fe2O3
Феррит легко восстанавливается, но не растворяется в 3 - 6%-ной серной кислоте.
Образование силикатов при обжиге в кипящем слое (t = 950 °С) протекает минимум на 60% (в некоторых случаях 90% SiO2 вступало в реакцию). При 800 °С реагирует 16 - 18% SiO2. Образование неустойчивых силикатов мало влияет на восстановление цинка,
но осложняет сгущение в гидрометаллургии. Силикаты цинка образуются в боль
шей степени в присутствии свинца:
2 ZnO + SiO2 = Zn2SiO4 +48,1 кДж/моль
2 Pb + SiO2 = Pb2SiO4 + 8,4 кДж/моль
Образование сульфата цинка происходит по следующим реакциям:
ZnS + 2 O2 = ZnSO4 + 775,7 кДж/моль
ZnO + SO3 = ZnSO4 + 242,7 кДж/моль
Н.Диев и А.Окунев приводят для реакции (7) следующие термодинамические данные:
 и
и 
Для образования ZnSO4, по данным О.Кубашевского, справедливо уравнение

Расчеты по уравнениям с учетом равновесия в системе и состава печных газов приводят к выводу о возможности существования сульфата цинка при температуре, близкой к 900° С.
SO3 = SO2 + ½ O2

Образование основных сульфатов типа ZnSO4 .0,5 ZnO, возможно, имеет место даже при 930 – 950 °С в печах с кипящим слоем, хотя и в незначительных количествах (0,40% SO4 в огарке печей Челябинского завода и 0,8% по заводу «Электроцинк)».
Присутствие ZnSO4 в огарке, видимо, может быть объяснено механическими причинами (пыль из стояков падает в слой). При агломерации (1100 - 1150° С) сульфаты меди, цинка, свинца и другие почти полностью разлагаются. Сульфатизация, однако, протекает в циклонах.
Высокое содержание сульфатной серы наблюдается в пылях из газоходов и электрофильтров. Присутствие некоторого количества ZnSO4 в огарке и пыли полезно для -гидрометаллургического процесса (компенсация потерь H2SO4) и нежелательно в агломерате, направляемом на дистилляцию.

Рис.12.3 Состав газов и номограмма для расчета отвода тепла при обжиге в КС
В условиях обжига в кипящем слое при 950 °С мышьяк, сурьма, германий, индий и галлий практически полностью остаются в огарке. Свинец возгоняется до 20%, кадмий до 50%, таллий на 80 - 90%.  Десульфуризация в результате обжига достигает 94 – 96 %. Состав газов можно определить по рис.11.3.; теоретическое содержание SO2 в печных газах составляет 15 -15,2%.
Десульфуризация в результате обжига достигает 94 – 96 %. Состав газов можно определить по рис.11.3.; теоретическое содержание SO2 в печных газах составляет 15 -15,2%.
Дата добавления: 2018-06-01; просмотров: 1313; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!
