УРАВНЕНИЕ СОСТОЯНИЯ ИДЕАЛЬНОГО ГАЗА
Министерство образования и науки Российской Федерации
Архангельский государственный технический университет
МОЛЕКУЛЯРНАЯ ФИЗИКА. ТЕРМОДИНАМИКА
Методические указания к выполнению контрольного задания № 2 для студентов заочного факультета
инженерно – технических специальностей
Архангельск
2004
Рассмотрены и рекомендованы к изданию методической
комиссией факультета промышленной энергетики
Архангельского технического университета
26 мая 2004 г.
Составители:
Л.В. Филимоненкова, доц. канд. техн. наук;
А.Г. Корельская, ассистент.
Рецензент
Ю.Л. Леухин, канд.тех.наук
УДК 530.1
Филимоненкова Л.В., Корельская А.Г. Молекулярная физика. Термодинамика: Методические указания к выполнению контрольного задания № 2 для студентов – заочников инженерно – технических специальностей. Архангельск: Изд-во АГТУ, 2004. – 27 с.
Подготовлены кафедрой физики АГТУ.
В указаниях излагаются основные законы и формулы по молекулярной физике и термодинамике, приведены примеры решения задач.
Предназначены для студентов-заочников инженерно-технических специальностей.
Ил. 5. Табл. 3.
© Архангельский государственный
|
|
|
технический университет, 2004
РЕКОМЕНДАЦИИ К ВЫПОЛНЕНИЮ КОНТРОЛЬНОЙ РАБОТЫ
К выполнению контрольной работы следует приступить только после изучения материала, соответствующего данному разделу программы, внимательного ознакомления с примерами решения задач, приведенных в данном пособии по каждому разделу курса.
При выполнении контрольной работы необходимо руководствоваться следующими правилами.
1. Контрольная работа выполняется в обычной школьной тетради (каждая контрольная выполняется в отдельной тетради). Для замечаний рецензента на страницах тетради оставляются поля. Каждая следующая задача должна начинаться с новой страницы. Условия задач переписываются полностью без сокращений.
2. При решении задач следует пользоваться международной системой единиц ( СИ ). Все величины, входящие в условия задачи, выражаются в единицах этой системы.
3. Решения задач должны сопровождаться краткими, но исчерпывающими пояснениями, раскрывающими физический смысл употребляемых формул. В тех случаях, когда это возможно, дать чертеж, выполненный с помощью чертежных принадлежностей.
Если при решении задачи применяется формула, получаемая для частного случая, не выражающая какой-нибудь физический закон или не являющаяся определением какой-нибудь физической величины, то её следует вывести.
|
|
|
4. Решать задачу надо в общем виде, то есть выразить искомую величину в буквенных обозначениях величин, заданных в условии задачи. При таком способе решения не производятся вычисления промежуточных величин.
Получив решение в общем виде, сделать анализ его размерности. Для этого надо подставить в правую часть полученной рабочей формулы вместо символов величин обозначения единиц, провести с ними необходимые действия и убедиться в том, что полученная при этом единица соответствует искомой величине. Если такого соответствия нет, то это означает, что задача решена неверно.
5. В конце контрольной работы следует указать учебники и учебные пособия, которыми пользовались при решении задач.
6. Получив из университета проверенную работу, следует внимательно ознакомиться с замечаниями и указаниями рецензента. Если при выполнении контрольной работы были допущены ошибки, необходимо выполнить работу над ошибками в той же тетради и направить ее на повторную проверку.
7. После получения положительной рецензии студент обязан пройти собеседование по существу решенных задач. Итогом собеседования является зачет по контрольной работе.
|
|
|
8. Студентам, проживающим вблизи университета или филиалов и учебно-консультационных пунктов, рекомендуется прослушать курс лекции по физике, организуемых для студентов заочников, а также использовать очные консультации преподавателей кафедры физики.
МОЛЕКУЛЯРНОЕ СТРОЕНИЕ ВЕЩЕСТВА
1.1. Количество вещества (n) – физическая величина, определяемая числом структурных элементов, из которых состоит вещество. В молекулярной физике для измерения количества вещества вводится единица – моль. В одном моле различных веществ содержится одинаковое число молекул (число Авогадро):
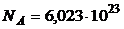 моль-1.
моль-1.
1.2. Молярная масса (масса моля) любого вещества выражается соотношением:
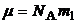 ,
,
где m1-масса одной молекулы данного вещества.
Масса моля µ численно равна относительной молекулярной массе Мr данного вещества, умноженной на 10-3 (m = Мr ×10-3 кг /моль), например:
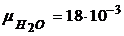 кг/моль.
кг/моль.
1.3. Число молей n, содержащихся в данной массе вещества m:
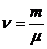 .
.
1.4. Число молекул Ν, содержащееся в данной массе вещества m:
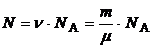 .
.
1.5. Плотность вещества:
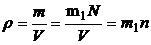 ,
,
где m –масса вещества, заключенного в объеме V; n - число молекул в единице объема.
|
|
|
1.6. Закон Авогадро: моли любых газов при одинаковых температурах и давлениях занимают одинаковые объемы. При нормальных условиях этот объем Vμ=22,41×10-3 м3/моль.
1.7. Массовая доля α i-того компонента смеси газов:
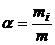 ,
,
где mi – масса i-того компонента смеси, m – масса смеси.
УРАВНЕНИЕ СОСТОЯНИЯ ИДЕАЛЬНОГО ГАЗА
2.1. Состояние данной массы идеального газа описывается уравнением Менделеева - Клапейрона:
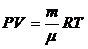 ,
,
где P,T - давление и температура газа; V - объем, занимаемый данной массой газа (объем сосуда); 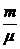 - число молей, содержащихся в данной массе газа; R - универсальная газовая постоянная, R = 8,31Дж/(моль·K).
- число молей, содержащихся в данной массе газа; R - универсальная газовая постоянная, R = 8,31Дж/(моль·K).
2.2. Исходя из уравнения состояния, можно определить плотность идеального газа:
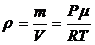 .
.
Между температурой t (по шкале Цельсия) и температурой T (по шкале Кельвина) существует следующая связь:
T=(t + 273,15)К 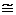 (t+273) К.
(t+273) К.
2.3. Вводя постоянную Больцмана 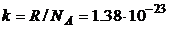 Дж/К уравнение состояния (2.1) примет вид:
Дж/К уравнение состояния (2.1) примет вид:
р = nkT,
где n – концентрация молекул.
2.4. Закон Дальтона для смеси газа.
Если в сосуде V при температуре T содержится смесь газов, то необходимо считать, что каждый из компонентов этой смеси распространяется по всему объему сосуда. Парциальное давление pi, создаваемое отдельным i-м компонентом смеси, определяется из уравнения Менделеева - Клапейрона:
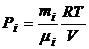 ,
,
где mi- масса данного компонента в смеси; 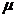 i - масса одного моля этого компонента.
i - масса одного моля этого компонента.
Давление смеси газов равно сумме парциальных давлений, входящих в нее газов:
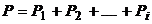
или
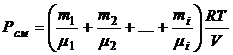 .
.
В равновесном состоянии плотность смеси ρсм равна сумме плотностей компонентов смеси:
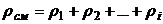 .
.
Пример 1. Смесь азота и гелия при температуре 270С находится под давлением Р = 1,3·102Па. Масса азота составляет 70% от общей массы смеси. Найти концентрацию молекул каждого из газов.
Дано: Р=1,3·102Па; m1=0,7m; m1 =28г/моль=28·10-3кг/моль; 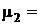 4г/моль=4·10-3 кг/моль; Т = 27+ 273 = 300К.
4г/моль=4·10-3 кг/моль; Т = 27+ 273 = 300К.
Найти: n1 и n2.
Решение. Давление смеси выразим по закону Дальтона:
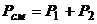 .
.
где Р1 – парциальное давление азота в смеси; Р2 – парциальное давление гелия.
Выразим Р1и Р2 из уравнения Менделеева - Клапейрона:
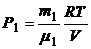 ;
; 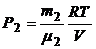 .
.
Найдем соотношение между Р1 и Р2:
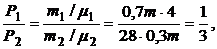 т. е. Р2 = 3Р1.
т. е. Р2 = 3Р1.
Так как
Рсм = Р1 + Р2 = Р1 + 3Р1 = 4Р1,
Следовательно,
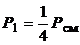 ,
, 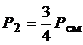 .
.
С другой стороны, давление любого газа можно легко выразить через концентрацию его молекул (n) и температуру:
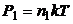 ;
; 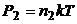 .
.
Отсюда
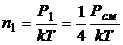 ;
; 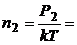
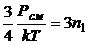 .
.
Проверим размерность:

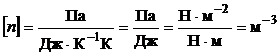 .
.
Произведем вычисления:
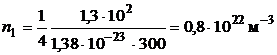 ;
;
n2 = 3n 1 = 2,4 ·1022 м-3.
Ответ: n1 = 0,8·1022 м-3; n2 = 2,4·1022м-3.
Дата добавления: 2018-06-27; просмотров: 184; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!
