Приготовление рабочего раствора
В стакане объемом 50 мл из исходных растворов сульфата меди(II) и хлорида железа(III) в соответствии с таблицей 1 приготовьте рабочий раствор смеси двух соединений (по указанию преподавателя).
Таблица 1.1
| № образца | 1 | 2 | 3 | 4 |
| Объем, мл | ||||
| FeCl3, 0,1М | 1 | 1 | 1 | 1 |
| CuSO4, 0,1М | 1,5 | 2 | 2,5 | 3 |
Разделение гидроксида железа (III) и комплексной соли меди (II)
В стакан с рабочим раствором добавить из бюретки 5 мл 10 % раствора гидроксида аммония и перемешать. Полученный осадок гидроксида железа(III) отфильтроватьна воронке с бумажным фильтром в коническую колбу. Осадок промыть на фильтре дистиллированной водой до полного удаления ионов меди(II) (отсутствие голубой окраски на фильтре).
4. Определение концентрации Cu2+ в фильтратеспектрометрическим методом
Порядок работы на спектрофотометре, построение градуировочного графика и определение концентрации окрашенного вещества по градуировочному графику описано в работе № 5, стр. 68-74 (лабораторный практикум).
Перед началом работы на спектрофотометре (фотоколориметре) проверьтеградуировочный график выданный преподавателем по контрольной точке.
Для приготовления контрольного раствораCuSO4в мерную колбу на 100 мл внесите 4 мл 0,1 М раствора CuSO4 и 5 мл 10% раствора NH4OH, доведите до метки дистиллированной водой, перемешайте. Рассчитайте концентрацию полученного контрольного раствора,проведите измерение его оптической плотности на фотокалориметре.Сравните значение концентрации, полученной с помощью градуировочного графика с расчетной. При расхождении расчетных и экспериментальных данных более чем на 5%, необходимо построить новый колибровочный график.
|
|
|
Далее приступают к определению концентрацииCu2+ в фильтрате.
Для этого фильтрат, содержащий комплексную соль меди [Cu(NH3)4]SO4,нужно перенести в мерную колбу на 100 мл и довести объем водой до метки. Перемешать раствор в мерной колбе, переворачивая ее не менее 10 раз вверх дном, придерживая пробку.
В полученном растворе фотометрическим методом определяют концентрацию ионов меди(II).
На спектрофотометре КФК-2 измерьте оптическую плотность (D)фильтрата раствора сульфата тетраамминмеди(II)[Cu (NH3)4]SO4, находящегося в мерной колбе на 100 мл, и определите по градуировочному графику (выданному преподавателем) концентрацию ионов меди в растворе (С2).
ВНИМАНИЕ!!!
Перед измерением оптической плотности кювету необходимо ополаскивать исследуемым раствором.
Оформление опыта
Масса меди(II) в исходном рабочем растворе:
m1(Cu2+) = V1(Cu2+)·C1·М(Cu2+), г
C1 – концентрация ионов меди(II) в исходном растворе сульфата меди(II), моль/л;
|
|
|
V1(Cu2+) – объем раствора сульфата меди(II), взятый на приготовление рабочего раствора, л; (таблица 1)
М(Cu2+) – молярная масса ионов меди (II), г/моль.
Масса меди в растворе сульфата тетраамминмеди(II) [Cu (NH3)4]SO4:
m2(Cu2+) = V2(Cu2+)·C2·М(Cu2+), г
C2 – концентрация ионов меди(II), найденная по градуировочному графику, моль/л;
V2(Cu2+) – объем мерной колбы с раствором комплексной соли [Cu (NH3)4]SO4, л,
Степень извлечения меди(II) (в %):
η = (m2(Cu2+) / m1(Cu2+))·100
Занесите результаты опыта в таблицу 1.2, используя данные полученные студентами группы. Наосновании результатов сделайте вывод о влиянии соотношения реагентов. на степень извлечения.
Таблица 1.2
| Соотношение VFe3+ / VCu2+ | 1:1,5 | 1:2 | 1:2,5 | 1:3 |
| m1(Cu2+) г | ||||
| C2(Cu2+) моль/л | ||||
| m2(Cu2+) г | ||||
| η % |
ОПЫТ 2
Очистка и разделение химических соединений методом ионообменной сорбции
Для разделения и очистки широко используется метод ионного обмена, который основан на обратимой реакции обмена одноименными ионами между твердым катионитом 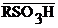 или анионитом
или анионитом 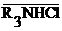 и жидким электролитом.
и жидким электролитом.
|
|
|
СuSO4 + 2 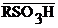 ®H2SO4 +
®H2SO4 + 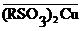
СuSO4 + 2 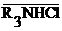 ®СuСl2 +
®СuСl2 + 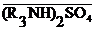
Дата добавления: 2018-05-13; просмотров: 330; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!
