Числом не спаренных электронов определяется валентность элемента.
Вопросы с ответами.
Периодический закон и периодическая система химических элементов Д.И.Менделеева в свете учения о строении атома.
Периодический закон, который формулировал Д.И.Менделеев:
Свойства простых тел, а также формы и свойства соединений элементов находятся в периодической зависимости от величины атомных весов элементов.
Периодическая система элементов.
Горизонтальный ряд хим. элементов, начинающийся щелочным металлом и заканчивающийся инертным газом, называется периодом.
I, II, III - малые периоды, т.к. состоят из одного ряда хим. элементов, имеют малое число элементов.
I - 2 элемента
| 8 элементов |
III
IV - VII - большие периоды, т.к. состоят из двух рядов (четного и нечетного) элементов.
В четных рядах больших периодов располагаются типичные металлы. Нечетный ряд начинается металлом, затем металлические свойства ослабляются и нарастают свойства неметаллические, заканчивается период инертным газом.
Группа- это вертикальный ряд хим. элементов, объединенных по хим. свойствам.
Группа
Главная подгруппа побочная подгруппа
В главную подгруппу входят В побочную подгруппу входят
элементы и малых, и больших элементы только больших периодов.
периодов.
H, Li, Na, K, Rb, Cs, Fr Cu, Ag, Au
малые большие большие
Для элементов, объединенных в одну и ту же группу, характерны следующие закономерности:
1. Высшая валентность элементов в соединениях с кислородом ( за некоторым исключением) соответствует номеру группы.
Элементы побочных подгрупп могут проявлять и другую высшую валентность. Например, Cu - элемент I группы побочной подгруппы - образует оксид Cu2O. Однако, наиболее распространенными являются соединения двухвалентной меди.
2. В главных подгруппах (сверху вниз) с увеличением атомных масс усиливаются металлические свойства элементов и ослабевают неметаллические.
Строение атома. Электронные формулы и графические схемы строения электронных слоев атомов.
Атомы, представляют собой сложные образования, построенные из более мелких структурных единиц.
| атом |
| ядро |
n0 - нейтрон
ē - электрон - вне ядра
Число электронов в атоме равно числу протонов, т.е. порядковому номеру элемента, так как атом электронейтрален.
Каждый хим. элемент в периодической системе был пронумерован. Номер, который получает каждый элемент, называется порядковым номером.
Физический смысл порядкового номера:
1. Каков порядковый номер элемента, таков и заряд ядра атома.
2. Столько же электронов вращается вокруг ядра .
Z = р+ Z - порядковый номер элемента
Z = ē
n0 = А - Z
n0 = А - р+ А - атомная масса элемента
n0 = А - ē
Например, Li.
Z = 3 р+ = 3
ē = 3
n0= 7- 4 = 3
Физический смысл номера периода.
В каком периоде находится элемент , столько электронных оболочек (слоев) он будет иметь.

Определение максимального числа электронов на одной электронной оболочке:
2n2 n - номер уровня 2, 8, 18, 32
Типичными Ме являются те элементы, которые на внешней эл. оболочке содержат от 1 до 2 ē.
Типичные НеМе на внешней эл. оболочке содержат от 4 до 8 ē.
В каждом периоде Ме свойства уменьшаются, а НеМе усиливаются.
В пределах одной и той же группы (в главной подгруппе) Ме свойства усиливаются, а НеМе ослабевают.
Электронное строение атома.
+ n
S S P S P d S P d f
Каждый энергетический уровень делится на энергетические подуровни: S, P, d, f и т.д.
|
|
S 2 ē
|
|
|
|
d 10 ē
| электронная конфигурация (электронная формула) |
|
|
|
|
|
|
|
|
|
|
не спаренный спаренные
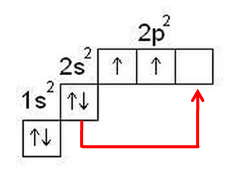
Числом не спаренных электронов определяется валентность элемента.
II, IV
С - 1S22 S2 2Р2
Дата добавления: 2018-05-13; просмотров: 396; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!
