ОПРЕДЕЛЕНИЕ ЭЛЕКТРОПРОВОДНОСТИ ВОДЫ
МОСКОВСКИЙ ПОЛИТЕХНИЧЕСКИЙ КОЛЛЕДЖ
МЕТОДИЧЕСКОЕ ПОСОБИЕ
к лабораторным работам
по дисциплине
«МОНИТОРИНГ ЗАГРЯЗНЕНИЯ ПРИРОДНОЙ СРЕДЫ»
АВТОРЫ: ПАХОМОВА О.К.
ЩЕРБАКОВА Г.С.
МОСКВА - 2004 год
АНАЛИЗ ВОДЫ
ОПРЕДЕЛЕНИЕ рН ВОДЫ
РН воды – один из важнейших показателей ее качества, определение которого предусмотрено обязательными программами соответствующих наблюдений. Величина рН имеет большое значение для химических и биологических процессов, происходящих в природных водах: от нее зависит развитие и жизнедеятельность водных растений, устойчивость различных форм миграции элементов, агрессивное действие воды на металлы и бетон.
Величина рН речных вод обычно изменяется в пределах 6,5-8,5; атмосферных осадков – 4,6-6,1; болот – 5,5-6,0; океана – 7,9-8,3. Наблюдаются суточные и сезонные колебания рН, связанные с изменением фотосинтетической активности водорослей.
Временное снижение рН воды до 5,5 (например, в результате выпадения кислых осадков) отвечает первой стадии закисления водоема. Если рН поддерживается на уровне 5,5 постоянно, то водоем вступает во вторую стадию окисления. При падении рН ниже 5 наблюдается третья стадия закисления, возврат водоема из которой в первоначальное состояние невозможен.
При снижении рН увеличивается скорость растворения тяжелых металлов и алюминия в воде, что приводит в конечном итоге к гибели фитопланктона, водорослей, рыб.
|
|
|
Величину рН при анализе вод определяют в свежеотобранных пробах, длительное хранение проб не допускается.
рН представляет собой отрицательный логарифм концентрации ионов водорода:
 .
.
рН воды определяют потенциометрическим методом анализа.
Потенциометрический метод анализа основан на зависимости электродного потенциала от концентрации раствора. В основе метода лежит уравнение Нернста:
 ,
,
где Y - равновесный электродный потенциал,
Y0 - стандартный электродный потенциал,
Z - заряд иона,
C - концентрация иона.
рН воды определяют на приборе рН-340. К прибору подключают электроды:
- измерительный электрод – стеклянный (индикаторный на ион Н+);
- вспомогательный электрод сравнения – хлорсеребряный.
Измерение рН воды
1. Перед измерением электроды промывают дистиллированной водой, капли воды на них убирают фильтровальной бумагой.
2. В стакан наливают анализируемую воду так, чтобы электроды были опущены на 1 см. Электроды погружают в анализируемую воду.
3. Ручку «размах» ставят в положение «15 рН». По нижней шкале показывающего прибора определяют интервал измерения. Ручку «пределы измерения» устанавливают на соответствующий интервал. Ручку «размах» переключают в положение «3 рН» и берут отсчет по верхней шкале показывающего прибора.
|
|
|
ПРИМЕР:
Ручку «размах» ставят в положение «15 рН». По нижней шкале показывающего прибора получилось значение 5, ручкой «пределы измерения» устанавливают интервал «2-5» , так как 5 входит в этот интервал. Ручку «размах» переключают в положение «3 рН» и берут отсчет по верхней шкале показывающего прибора, считая, что крайнее левое положение по шкале соответствует значению 2, то есть будет не 0, а 2.
4. Записывают значение рН. Указывают среду. Вычисляют рОН; С(Н+), моль/л; С(ОН-), моль/л.
ПРИМЕР
рН = 2,3
Среда кислая
рН + рОН = 14
рОН = 14 – 2,3 = 11,7
рН = -lg С(Н+)
lg С(Н+) = -2,3
lg С(Н+) = lg 10–2,3
C(Н+) = 10-3.10+0,7
С(Н+) = 5.10-3 моль/л
С(ОН-) = 10-14 / 5.10-3 = 10.10-15 / 5.10-3 = 2.10-12 моль/л.
ОПРЕДЕЛЕНИЕ ЭЛЕКТРОПРОВОДНОСТИ ВОДЫ
Электропроводностью называют способность вещества пропускать электрический ток. Вещества способные проводить электрический ток называют электролитами.
Электропроводность является интегральным (обобщенным) показателем качества воды, который определяют в рамках обязательной программы мониторинга поверхностных вод суши. Она отражает общее содержание солей в анализируемой воде и является неселективным показателем степени загрязнения последней, так как одной и той же величине электропроводности может соответствовать различный ионный состав воды. Увеличение электропроводности воды природного водоема или водотока является явным свидетельством повышения антропогенной активности.
|
|
|
Электропроводность воды определяют кондуктометрическим методом анализа. Кондуктометрический метод анализа основан на зависимости электропроводности от концентрации раствора.
Электропроводность представляет собой величину, обратную сопротивлению R. Единица измерения электропроводности - каппа Х [Ом-1cм-1]. Электропроводность зависит от концентрации, температуры, природы электролита.
Электропроводность определяют на приборе АНИОН – 410:
Измерение электропроводности воды
1. Включают прибор нажатием кнопки ОN.
2. Нажимают Еsc и кнопку 6.
3. Записывают значение общей электропроводности.
ОПРЕДЕЛЕНИЕ ЖЕЛЕЗА В ВОДЕ
Главными источниками соединений железа в природных водах являются процессы химического выветривания и растворения горных пород. Значительные количества железа поступают с подземным стоком и со сточными водами предприятий металлургической, металлообрабатывающей, текстильной, лакокрасочной промышленности, с сельскохозяйственными стоками.
|
|
|
Железо в воде присутствует в растворимой и нерастворимой формах, как в свободном виде, так и в виде комплексов с неорганическими и органическими лигандами, главным образом с гуминовыми кислотами. Концентрация железа в поверхностных пресных водах составляет обычно десятые доли миллиграмма, в болотных водах, где концентрация гумусовых веществ достаточно велика, единицы миллиграммов.
Являясь биологически активным элементом, железо в определенной степени влияет на интенсивность развития фитопланктона и качественный состав микрофлоры в водоеме.
При содержании железа выше 1 мг/л вода становится мутной, окрашивается в желто-бурый цвет, у нее ощущается характерный металлический привкус. Такая вода практически неприемлема как для технического, так и для питьевого применения. По органолептическим признакам предел содержания (ПДК) железа в воде практически повсеместно установлен на уровне 0,3 мг/л (по нормам ЕС даже 0,2 мг/л). По показаниям вредности для здоровья такой параметр не установлен.
Железо в воде можно определять в виде Fe2+ и Fe3+. Обычно определяют общее содержание железа, для этого пробу воды окисляют концентрированной азотной кислотой (Fe2+ переходит в Fe3+). Объем пробы воды для определения массовой концентрации железа должен быть не менее 200 мл, пробу не консервируют.
Определение железа в воде проводят фотоэлектроколориметрическим методом. Фотоэлектроколориметрический метод анализа основан на зависимости светопоглощения раствора от его концентрации. Использование света видимой области спектра в данном методе дает возможность анализировать окрашенные вещества или вещества, которые можно перевести в окрашенные растворы.
В основе фотоэлектроколориметрического метода анализа лежит закон Бугера – Ламберта – Бера: абсорбционность прямо пропорциональна концентрации раствора и толщине поглощающего слоя.
А = Е.L.С,
Где А - абсорбционность,
Е - молярный коэффициент поглощения (абсорбционности),
L - толщина поглощающего слоя,
С - концентрация раствора.
Определение содержания железа проводят на приборе КФК-2. На приборе КФК-2 работают в видимой области спектра. Видимая область спектра лежит в диапазоне длин волн 400-750 нанометров (нм).
Сущность метода определения
Метод основан на образовании окрашенного иона при взаимодействии Fe3+ с сульфосалициловой кислотой. При рН = 8 - 10 комплексный ион железа образует желтый раствор.
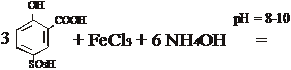
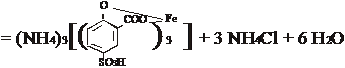
Область обнаружения железа данным методом составляет 0,1 - 1 мг/л.
Ход работы
Дата добавления: 2018-05-12; просмотров: 947; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!
