ГЛАВА 9. ДИ- И ПОЛИГАЛОГЕНОПРОИЗВОДНЫЕ ПРЕДЕЛЬНЫХ УГЛЕВОДОРОДОВ
РАЗДЕЛ III. СОЕДИНЕНИЯ С ОДНОРОДНЫМИ ФУНКЦИЯМИ ГЛАВА 8. ГАЛОГЕНОПРОИЗВОДНЫЕ УГЛЕВОДОРОДОВ Галогенопроизводные можно рассматривать как продукты замещения в углеводородах одного или нескольких атомов водорода атомами галогенов. В соответствии с этим могут существовать предельные и непредельные моно- и полигалогенопроизводные.
Моногалогенопроизводные предельных углеводородов
Моногалогенопроизводные предельных углеводородов носят название галогеналкилов, их общая формула CnH2n+1Hal.
В зависимости от положения атома галогена, характера атома углерода, с которым атомы галогена связаны, различают первичные: R–CH2–Cl; вторичные: R2–CH–Cl; третичные: R3C–Cl – галогеналкилы.
Изомерия. Номенклатура
Изомерия галогенопроизводных зависит от строения углеродного скелета и положения атома галогена в цепи. Следовательно, галогенопроизводные имеют большее число изомеров, чем предельные углеводороды. Изомерия начинается с третьего члена ряда.
Названия галогенопроизводных строятся из названий соответствующих им предельных углеводородов с добавлением названия галогена с цифрой, указывающей его положение в цепи.
Простейшие галогенопроизводные называют по названиям входящих в них радикалов:
CH3–Cl хлорметан, хлористый метил
CH3–CH2Cl хлорэтан, хлористый этил
CH3–CH2–CH2Cl 1 -хлорпропан, хлористый пропил
CH3–CHCl–CH3 2-хлорпропан, хлористый изопропил или хлористый вторичный пропил
|
|
|
CH3–CH2–CH2–CH2–Cl 1-хлорбутан, хлористый бутил
CH3–CHCl–CH2–CH3 2-хлорбутан, хлористый вторичный бутил
CH3–CH(CH3)–CH2Cl 1-хлор-2-метилпропан, хлористый изобутил
 2-хлор-2-метилпропан, хлористый третичный бутил
2-хлор-2-метилпропан, хлористый третичный бутил
Способы получения
Моногалогенопроизводные получают наиболее часто из предельных углеводородов реакцией замещения, из олефинов – присоединением галогеноводородов, из спиртов – реакцией с галогеноводородами фосфора.
1. Получение моногалогенопроизводных из предельных углеводородов реакцией замещения атомов водорода галогенами – наиболее важный технический метод.
Особенности реакции замещения водорода атомами галогена были подробно рассмотрены при изучении химических свойств предельных углеводородов:

Следует отметить, что в органической химии ярко выражена взаимосвязь различных ее разделов. Одни и те же реакции на протяжении всего курса приводятся в одних случаях как характеризующие свойства данного класса соединений, а в других – как метод получения другого класса веществ.
2. Присоединение галогенопроизводных к олефинам (алкенам). Опять мы возвращаемся к свойствам, в этот раз олефинов и вспоминаем правило В. В. Марковникова. «При присоединении галогеноводородов к несимметричным олефинам водород присоединяется к более гидрогенизированному атому углерода, а галоген – к другому, связанному с первым двойной связью, т. е. менее гидрогенизированному.»
|
|
|

3. Замещение гидроксильной группы спиртов на галоген действием галогеноводородов:

Физические свойства
Физические свойства галогенопроизводных зависят от природы атомов галогена, состава и строения углеводородного радикала.
При обычных условиях фтористые метил, этил, пропил и бутил, хлористые метил и этил, бромистый метил являются газами. Все остальные галогеналкилы – жидкости, высшие представители – твердые вещества.
Химические свойства
1. Получение предельных углеводородов из галогенопроизводных путем замены галогена (при действии металлического натрия радикалом, реакция Вюрца):

2. При каталитическом гидрировании галогеноалкинов или действии на них водорода в момент выделения, а также иодистого водорода происходит замещение атома галогена водородом:

3. Гидролиз. При действии воды на галоидные алкилы образуются спирты:

4. Реакции с едкими щелочами можно представить как реакции обмена:
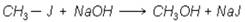
5. Действием аммиака (аммонолиз) можно получить амины:
|
|
|

6. Действием азотистокислого серебра получают нитросоединения:

7. Действием цианидов получают нитрилы или изонитрилы:

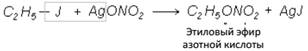
8. Получение сложных эфиров.
С серебряными или иными солями кислот получаются сложные эфиры:
9. При действии металлов (Zn, Mg) получаются металлоорганические соединения.
Особый интерес представляет действие магния на галогеноводороды в присутствии безводного диэтилового эфира с получением растворов, содержащих смешанные магнийорганические соединения – Гриньяровские реактивы.
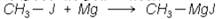
Такие растворы применяются для многих синтезов. Например:

ГЛАВА 9. ДИ- И ПОЛИГАЛОГЕНОПРОИЗВОДНЫЕ ПРЕДЕЛЬНЫХ УГЛЕВОДОРОДОВ
Ди- и полигалогенопроизводные могут иметь одинаковые или разные атомы галогенов у одного и того же или различных атомов углерода.
Изомерия. Номенклатура
Галогенопроизводные с атомами галогена у одного и того же атома углерода называются гименальными, у рядом стоящих атомов углерода – вицинальными.
| CH2Cl2 | дихлорметан, хлористый метилен |
| CHCl3 | трихлорметан, хлороформ |
| CCl4 | тетрахлорметан, четыреххлористый углерод |
| CH3 – CHCl2 | 1, 1-дихлорэтан, этилиден* |
| CH2Cl – CH2Cl | 1, 2-дихлорэтан, хлористый этилен |
* Названия двухвалентных радикалов, имеющих две свободные валентности у одного и того же углеродного атома, производятся заменой окончания –ан предельного углеводорода на -иден (кроме метилена)
|
|
|
| CHCl2 – CH2Cl | 1, 1, 2-трихлорэтан |
| CCl3 – CH3 | 1, 1, 1-трихлорэтан |
| CCl3 – CH2Cl | 1, 1, 1, 2-тетрахлорэтан |
| CHCl2 – CHCl2 | 1, 1, 2, 2-тетрахлорэтан |
| CCl3 – CHCl2 | 1, 1, 1, 2, 2-пентахлорэтан |
Способы получения
1. Полигалогенопроизводные обычно получают из углеводородов или из кислородосодержащих соединений:

2. Гименальные дигалогенопроизводные образуются при действии пентагалоидов фосфора (пятигалоидных соединений фосфора) на альдегиды и кетоны:

3. Вицинальные дигалогенопроизводные получают присоединением галогенов к непредельным углеводородам:

Физические свойства
Ди- и полигалогенопроизводные предельных углеводородов – тяжелые масла или твердые вещества, нерастворимые в воде.
Химические свойства
1. Если атомы галогена находятся при различных атомах углерода, то при гидролизе образуются двухатомные спирты (гликоли).

2. Если атомы галогена находятся при одном углеродном атоме (геминальные соединения), то при гидролизе образуются альдегиды, кетоны или кислоты. Например:

Дата добавления: 2018-04-05; просмотров: 2850; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!
