Преимущества при использовании моноклональных антител. Доставка лекарственных веществ, основанная на использовании моноклональных антител
Бактерии - продуценты антибиотиков. Строение клетки. Антибиотики, образуемые бактериями.
Прокариоты и эукариоты. Все живые организмы принято делить на две основные группы: прокариоты и эукариоты. Приблизительно 1,5 млрд лет назад произошел переход от маленьких клеток со сравнительно простой внутренней структурой (так называемых прокариот, к которым относятся различные бактерии) к большим по размеру и значительно более сложно устроенным эукариотическим клеткам, подобным клеткам высших животных и растений.
Основные структурные различия про- и эукариот:
• наличие или отсутствие ядра, содержащего хромосомную ДНК;
• строение и химический состав клеточной стенки;
• наличие или отсутствие субклеточных цитоплазматических ор-ганелл.
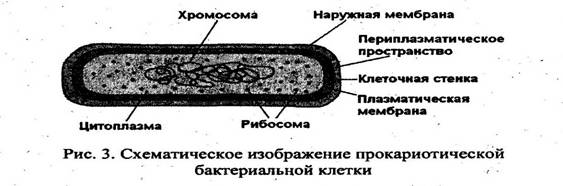
В прокариотической бактериальной клетке хромосомная ДНК находится непосредственно в цитоплазме, клетка окружена ригидной клеточной стенкой. В клетке нет субклеточных цитоплазматических орга-нелл (рис. 3). В оптимальных условиях прокариотическая клетка может делиться каждые 20 мин и таким образом давать жизнь более 10 млрд клеток менее чем за сутки.
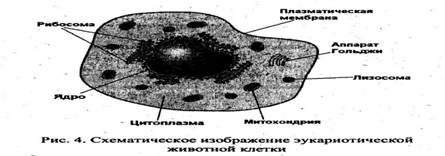
В эукариотической клетке (рис. 4) имеется ядро, отделенное от цитоплазмы ядерной мембраной, хромосомная ДНК находится в ядре. В цитоплазме содержатся различные субклеточные органеляы: мембраны, окружающие ядро, митохондрии, образующие лабиринт эндоплазмати-ческого ретикулума (ЭПР), где синтезируются липиды и мембранные белки. Мембраны формируют стопки уплощенных пузырьков, составляющих аппарат Гольджи, который участвует в синтезе и транспорте различных органических молекул. Мембраны окружают лизосомы (суб-
|
|
|
клеточные структуры диаметром 0,20-0,5 мкм), содержащие гидроли-тические ферменты, необходимые для внутриклеточного пищеварения.
Мембраны, таким образом, защищают от действия этих ферментов бел-ки и нуклеиновые кислоты самой клетки. Мембраны также окружают пероксисомы, содержащие окислительные ферменты, производящие и разрушающие опасные высокореакционоспособные перекиси (пероксиды). Обмен между внутриклеточными, окруженными мембранами струк-\турами и внеклеточной средой происходит с помощью эндоцитоза.
Различают две группы бактерий - эубактерии, населяющие почву, воду и другие организмы, и архебактерии, встречающиеся в таких средах обитания, как болота, океанские глубины, очень соленые воды и горячие кислые источники.
Исходя из температурного режима, который предпочитают те или иные микроорганизмы, их подразделяют на термофилы (от 45 до 90 °С и выше), мезофилы (от 10 до 47 °С) и психрофилы или психротрофы (от -5 до 35 °С). Микроорганизмы, активно размножающиеся лишь в определенном диапазоне температур, - полезный инструмент для решения различных биотехнологических задач. Например, термофилы часто служат источником генов, кодирующих термостабильные ферменты, а генетически видоизмененные психротрофы используются при пониженной температуре для биодеградации токсичных отходов, содержащихся в почве и воде.
|
|
|
Среди множества биологических объектов, использующихся в МБТ, основными «рабочими лошадками» являются бактерии Еscherichia coli, одноклеточные дрожжи Sacharomyces сеrevisiae и различные клеточные линии животного происхождения. Все они играют важную роль в получении белков, кодируемых клонированными генами.
Е. сoli — грамотрицательная непатогенная подвижная палочка длиной менее 1 мкм. Традиционная среда ее обитания — кишечник человека, может также высеваться из почвы и воды. Штаммы Е. сoli культивируются на обогащенных жидких питательных средах, содержащих аминокислоты, витамины, соли, микроэлементы и источник углерода. Е. соН можно культивировать в аэробных и анаэробных условиях, но для оптимальной продукции рекомбинантных белков Е. соli и другие микроорганизмы обычно выращивают в аэробных условиях. Рост клеточной массы и продукция белка лимитируются содержанием в питательной среде растворенного кислорода, для этого в ферментерах создают условия аэрации.
|
|
|
Кроме Е. соН в МБТ используют множество других микроорганизмов, которые подразделяют на две группы:
• микроорганизмы как источники специфических генов (например, ген, кодирующий стабильную ДНК-полимеразу, которая используется в широкоприменяемой полимеразной цепной реакции — ПЦР; этот ген был выделен из термофильных бактерий и клонирован в Е. соН).
• микроорганизмы, созданные генноинженернымми методами для решения определенных задач (например, различные штаммы Согуnebacterium glutamicumт, генетически модифицирова-ные с целью повышения продукции промышленно важных аминокислот).
Saccharomycesс cereае - непатогенные одноклеточные организмы с диаметром клетки около 5 мкм, во многих отношениях представляют эукариотический аналог Е. сoli. S. сегеvisiае размножаются почкованием, их способность к превращению сахара в этанол и углекислый газ издавна использовалась для изготовления напитков и хлеба. Клетки дрожжей делятся каждые 1,5-2 ч. S. сегеvisiае является удобной моделью для исследования других эукариот, в т.ч. человека, так как многие гены, ответственные за регуляцию клеточного деления S. ссегеvisiае, сходны с таковыми у человека. Это способствовало идентификации и характеристике генов человека, отвечающих за развитие новообразований. Генетическая система дрожжей является непременным участником всех исследований по изучению ДНК человека.
|
|
|
Синтезированный бактериальной клеткой эукариотический белок часто подвергают ферментативной модификации, присоединяя к белковой молекуле низкомолекулярные соединения, что необходимо для правильного функционирования белка. Однако Е. соН и другие прокариоты не способны осуществлять эту модификацию, поэтому для получения полноценных эукариотических белков используют S. сегеvisiае и другие виды дрожжей.
В качестве биологических систем в МБТ используют культуру эукариотических клеток. Кусочек ткани определенного организма (насекомого, растения, млекопитающего) обрабатывают протеолитическими ферментами (трипсином), расщепляющими белки межклеточного материала; при работе с растительными клетками используют ферменты, разрушающие клеточную стенку. Высвободившиеся клетки помещают в питательную среду, содержащую аминокислоты, антибиотики, витамины, соли, глюкозу, факторы роста. В этих условиях (деление клеток млекопитающих происходит примерно раз в сутки) на стенке емкости с культурой образуется клеточный монослой. Если после этого не перенести клетки в емкости со свежей питательной средой, рост прекращается. Обычно удается переносить (перевивать, субкультивировать) и поддерживать до 50-100 клеточных генераций исходной (первичной) клеточной культуры, затем клетки начинают терять способность к делению и гибнут.
В МБТ устойчивые линии используют для крупномасштабного производства вакцин и рекомбинантных белков, для размножения вирусов и выявления белков, которые кодируются клонированными последовательностями ДНК.
2. Химический синтез аскорбиновой кислоты и стадия биоконверсии в производстве витамина С.
Аскорбиновая кислота, или витамин С — это противоцинготный витамин, имеющийся у всех высших растений и животных; тальке человек и микробы не синтезируют ее, но людям она неотложно необходима, а микробы не нуждаются в ней. И, тем не менее, определенные виды уксуснокислых бактерий причастны к биосинтезу полупродукта этой кислоты — L-сорбозы. Таким образом, весь процесс получения аскорбиновой кислоты является смешанным, то есть химико-ферментативным.

Биологическая стадия процесса катализируется мембраносвя-занной полиолдегидрогеназой, а последняя (химическая) включает последовательно следующие этапы: конденсация сорбозы с диаце-тоном и получение диацетон — L-сорбозы, окисление диацетон — L-сорбозы до диацетон-2-кето- L-гулоновой кислоты, подвергаемой затем гидролизу с получением 2-кето-L-гулоновой кислоты; последнюю подвергают энолизации с последующей трасформацией в L-аскорбиновую кислоту.
Ферментацию Gluconobacter oxydans проводят на средах, содержащих сорбит (20%), кукурузный или дрожжевой экстракт, при интенсивной аэрации (8—10 г O2/л/ч). Выход L-сорбозы может достичь 98% за одни -двое суток. При достижении культурой log-фазы можно дополнительно внести в среду сорбит, доводя его концентрацию до 25%. Также установлено, что G. oxydans может окислять и более высокие концентрации полиспирта (30—50%), создаваемые на последних стадиях процесса. Это происходит благодаря полиолдегидрогеназы, содержащейся в клеточной биомассе. Ферментацию бактерий проводят в периодическом или непрерывном режиме. Принципиально доказана возможность получения L-сорбозы из сорбита с помощью иммобилизованных клеток в ПААГ.
Аскорбиновую кислоту используют как антиоксидант в здравоохранении и пищевой промышленности.
Преимущества при использовании моноклональных антител. Доставка лекарственных веществ, основанная на использовании моноклональных антител.
Направленное введение лекарственных препаратов.
Моноклональные антитела могут найти применение для введения лекарственных веществ и токсинов в определенную часть тела (например, в опухоль): либо путем их непосредственного присоединения к таким веществам, либо путем связывания с поверхностью липосом, содержащих внутри эти вещества.
Были получены комплексы антител к поверхностным антигенам раковых клеток со многими неспецифическими противораковыми средствами, но далеко не всегда они оказывались эффективными. Наиболее многообещающим является использование сильнодействующих растительных или бактериальных токсинов, одна молекула которых может вызывать гибель клетки.
Так, например, молекула токсина дифтерии: образована двумя полипептидными цепями, связанными дисульфидными мостиками. Цепь В связывается с клеточной поверхностью, а цепь А, обладающая ферментативной активностью, проникает внутрь клетки и нарушает работу механизма биосинтеза белка. Были предприняты попытки, заменить В-цепь токсина специфическими антителами, преимущественно гомогенными. Также недавно был получен препарат моноклональных антител к антигену раковых клеток прямой кишки, ассоциированных с А-цепью токсина, который избирательно действует на эти клетки в культуре.
С помощью моноклональных антител возможно также выделение биологически активных веществ (таких, например, как белки, гормоны, токсины) из сложных смесей. В случае интерферона Сичер и Берк из Уорвикского университета (Великобритания) с помощью метода иммуноадсорбции получили препарат со степенью около чистоты 1 %.
По этому методу антитела были пришиты к углеводным гранулам и исследованы для приготовления колонки с иммуносорбентом, на которой очищали грубый препарат интерферона. После одного пассажа через такую колонку с иммобилизованными моноклональными антителами препарат очищается в 5000 раз лучше.
Можно также использовать моноклональные антитела точной идентификации специализированных клеток, таких, например, как нейтроны, чтобы глубже изучить способы их взаимодействия и функционирование (т.е. локализацию химических нейромедиаторов).
Очень ценна техника моноклональных антител и для изучения клеточных мембран. Мембранные белки трудно выделить в чистом виде. Они присутствуют в клетках в малом количестве, их биологическую активность трудно измерить или же она и вовсе исчезает при растворении мембран в аналитических экспериментах. Эти трудности можно преодолеть, если прибегнуть к иммунологическим методам изучения мембранных белков, как это было сделано в случае антигенов клеточной поверхности, являющихся маркерами разных стадий дифференцировки тканей. Обычные препараты антител против клеточных антигенов, как правило, сложные и не способные распознавать отдельные молекулы.
Кроме того, еще одной сферой применения моноклональных антител является терапия различных заболеваний, так, например, эффективность серотерапии может быть увеличена благодаря применению моноклональных антител.
Также с помощью моноклональных антител можно изготовлять высокоспецифичные вакцины, особенно против определенных штаммов и паразитов.
Моноклональные антитела способны также нейтрализовать действие лимфоцитов, ответственных за отторжение трансплантата. В сочетании с лекарственными средствами они могут значительно усиливать эффективность действия последних на клетки-мишени, позволяя при этом избегать серьезных побочных явлений, столь обычных при химиотерапии рака.
Дата добавления: 2018-04-04; просмотров: 756; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!
