Влияние температуры на скорость реакции
Зависимость скорости реакции от температуры выражается правилом Вант - Гоффа: при увеличении температуры на каждые 10°С скорости реакции возрастает в 2-4 раза.
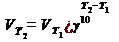
Где 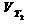 и
и 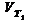 - скорости при температуре Т1 и Т2 . γ - температурный коэффициент.
- скорости при температуре Т1 и Т2 . γ - температурный коэффициент.
Примеры решения задач.
Пример 1: Как изменится скорость реакции протекающей в закрытом сосуде, если увеличить давление в 4 раза?
2NO(г.)+О2(г.)=2NO2
Решение:
увеличить давление в 4 раза означает увеличить и концентрацию газов во столько же раз.
1. Определяем скорость реакции до повышения давления.
V1 =K*C2NO*CO2
2. Определяем скорость реакции после повышения давления.
V2=K*(4CNO)2*(4CO2)=64K*C2NO*CO2
3. Определяем, во сколько раз возросла скорость реакции
V1/V2=64*K*C2NO*CO2 / K*C2NO*CO2
Ответ: скорость реакции возросла в 64 раза.
Пример 2: Во сколько раз возрастёт скорость реакции при повышении температуры с 20 С˚ до 50 С˚? Температурный коэффициент равен 3.
Решение:
По правилу Вант – Гоффа:
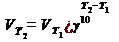
По условию требуется определить  . Подставим данные в формулу:
. Подставим данные в формулу:
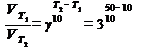
Ответ: скорость реакции возросла в 27 раз.
ОБЪЕКТ ИССЛЕДОВАНИЯ.
Зависимость скорости химической реакции от концентрации реагирующих веществ должна быть показана на основании измерения времени от момента сливания растворов до начала реакции, определяемой по помутнению раствора, обусловленному выделением свободной серы.
|
|
|
КОНТРОЛЬНЫЕ ВОПРОСЫ.
1.Что называется скоростью химической реакции?
2. Какова зависимость скорости реакции от концентрации реагирующих веществ?
3. Как называется величина К? Каков её физический смысл?
4. Зависит ли коэффициент К от изменения температуры?
5. Как влияет температура на скорость химической реакции?
6. Как влияет давление на скорость химической реакции между газообразными веществами?
ОПИСАНИЕ ЛАБОРАТОРНОЙ УСТАНОВКИ И ПОРЯДОК ПРОВЕДЕНИЯ ОПЫТА
Оборудование и реактивы: сернаякислота 2% раствор (ρ=1015 Кг/м³), тиосульфат натрия 2% раствор (ρ=1005 Кг/м³), пробирки, мерные цилиндры, термометр, секундомер, стаканы.
ОПЫТ 1. ЗАВИСИМОСТЬ СКОРОСТИ РЕАКЦИИ ОТ КОНЦЕНТРАЦИИ.
Реакция тиосульфата натрия Na2S2O3 с серной кислотой протекает по уравнению:
Na2S2O3+H2SO4=Na2SO4+S↓+H2SO3
Соответствующие объемы воды серной кислоты и тиосульфата натрия отмеряем мерным цилиндром. Растворы сливаются в одну пробирку и смешиваются быстрым движением, взбалтыванием. С этого момента до начала реакции измеряется время по секундомеру. Начало реакции указывает появление в растворе мути. Опытные данные вносят в таблицу 1.
|
|
|
Таблица 1.
| № опыта | V(мл) H2SO4 | V(мл) Na2S2O3 | V(мл) H2O | Vобщ(мл) смеси | Время t. сек | Скорость реакции |
| 1 2 3 | 20 20 20 |
На основании полученных данных выразить графически зависимость скорости реакции от концентрации тиосульфата натрия.
Отложить на оси абсцисс объемы в мл тиосульфата, а на оси ординат – время в секундах.
ОПЫТ 2.ЗАВИСИМОСТЬ СКОРОСТИ РЕАКЦИИ ОТ ТЕМПЕРАТУРЫ.
Зависимость скорости реакции от температуры должна быть показана на основании измерения времени от момента взаимодействия растворов серной кислоты и тиосульфата натрия при трех различных температурах. Во всех трех опытах концентрации и объемы растворов серной кислоты и тиосульфата натрия одинаковы.
В первом опыте в одну пробирку отмеряют 15 мл 2 % раствора тиосульфата натрия, а в другую – 5 мл 2% раствора серной кислоты. Обе пробирки опускают в стакан с горячей водой (tº~30ºС). В то же стакан опускают термометр. Спустя 5 мин. Измеряют температуру воды и, вынув из воды обе пробирки, сливают раствор серной кислоты в раствор тиосульфата натрия. Растворы смешивают быстрым взбалтыванием. С этого момента до начала реакции (появление мути) измеряется время по секундомеру.
|
|
|
Такие же опыты производятся с теми же объемами растворов серной кислоты и тиосульфата натрия при 40-50ºС и при охлаждении водопроводной водой.
Полученные данные вносятся в отчет по форме таблицы 2.
Таблица 2.
| № п/п | tº C | Время, сек. |
| 1 2 3 |
На основании полученных результатов выразить графически зависимость реакции от температуры, отложив на оси абсцисс температуры, а на оси ординат – время в секундах.
РЕКОМЕНДАЦИИ ПО ПЛАНИРОВАНИЮ И ПРОВЕДЕНИЮ ЭКСПЕРИМЕНТА.
При проведении лабораторного опыта необходимо каждый раствор отмерять своим цилиндром. Каждый опыт проводить в новой пробирке. При попадании на лицо, в глаза, на руки химических реактивов следует смыть немедленно водой и хорошо промыть пораженный участок большим количеством воды.
СОСТАВЛЕНИЕ ОТЧЕТА.
1. Цель работы, рабочее задание.
2. Химическая реакция, таблица, график.
3. Вывод о влиянии концентрации на скорость химической реакции.
4. Ответы на контрольные вопросы.
|
|
|
СПИСОК ЛИТЕРАТУРЫ.
1.Глинка Н.Л. Задачи и упражнения по общей химии . Москва: Интеграл –
пресс, 2001 – 2006,79-93 с.
2. Коровин Н. В. Общая химия. – М.: Высшая школа, 2004,142-158 с.
3.Белозерова Т.И. Химия. Конспект лекций. в двух частях для. инженерно- технических ( нехимических) специальностей.- Северодвинск: Севмашвтуз., 2009г.,часть1.
4. Белозерова Т.И. Термохимические расчеты. Химическое равновесие. Правило Ле Шателье. Методические указания к практическим работам. Севмашвтуз, 2006,
14с.
Дата добавления: 2018-04-05; просмотров: 293; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!
