Смещение равновесия под действием различных факторов
Обратимые и необратимые химические реакции. Химическое равновесие
Обратимые и необратимые химические реакции. Химическое равновесие. Смещение равновесия под действием различных факторов
Химическое равновесие
Химические реакции, протекающие в одном направлении, называют необратимыми.
Большинство химических процессов являются обратимыми. Это значит, что при одних и тех же условиях протекают и прямая, и обратная реакции (особенно если речь идет о замкнутых системах).
Например:
а) реакция
CaCO3
| t |
| → |
CaO+CO2↑
в открытой системе необратима;
б) эта же реакция
CaCO3⇄CaO+CO2
в замкнутой системе обратима.
Рассмотрим более подробно процессы, протекающие при обратимых реакциях, например, для условной реакции:
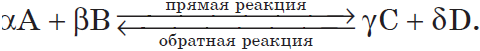
На основании закона действующих масс скорость прямой реакции
| → |
| υ |
=k1·CAα·CBβ
Так как со временем концентрации веществ А и В уменьшаются, то и скорость прямой реакции тоже уменьшается.
Появление продуктов реакции означает возможность обратной реакции, причем со временем концентрации веществ С и D увеличиваются, а значит, увеличивается и скорость обратной реакции:
| → |
| υ |
=k2·CCγ·CDδ
Рано или поздно будет достигнуто состояние, при котором скорости прямой и обратной реакций станут равными
| → |
| υ |
=
| ← |
| υ |
Состояние системы, при котором скорость прямой реакции равна скорости обратной реакции, называют химическим равновесием.
|
|
|
При этом концентрации реагирующих веществ и продуктов реакции остаются без изменения. Их называют равновесными концентрациями. На макроуровне кажется, что в целом ничего не изменяется. Но на самом деле и прямой, и обратный процессы продолжают идти, но с равной скоростью. Поэтому такое равновесие в системе называют подвижным и динамическим.
Константа равновесия
Обозначим равновесные концентрации веществ [A],[B],[C],[D].
Тогда так как
| → |
| υ |
=
| ← |
| υ |
,k1·[A]α·[B]β=k2·[C]γ·[D]δ, откуда
| [C]γ·[D]δ |
| [A]α·[B]β |
=
| k1 |
| k2 |
=Kравн.
где γ,δ,α,β — показатели степеней, равные коэффициентам в обратимой реакции; Kравн. — константа химического равновесия.
Полученное выражение количественно описывает состояние равновесия и представляет собой математическое выражение закона действующих масс для равновесных систем.
При неизменной температуре константа равновесия — величина постоянная для данной обратимой реакции. Она показывает соотношение между концентрациями продуктов реакции (числитель) и исходных веществ (знаменатель), которое устанавливается при равновесии.
Константы равновесия рассчитывают из опытных данных, определяя равновесные концентрации исходных веществ и продуктов реакции при определенной темпера туре.
|
|
|
Значение константы равновесия характеризует выход продуктов реакции, полноту ее протекания. Если получают Kравн.>>1, это означает, что при равновесии [C]γ·[D]δ>>[A]α·[B]β, т. е. концентрации продуктов реакции преобладают над концентрациями исходных веществ, а выход продуктов реакции большой.
При Kравн.<<1 соответственно выход продуктов реакции мал. Например, для реакции гидролиза этилового эфира уксусной кислоты
CH3COOC2H5+H2O⇄CH3COOH+C2H5OH
константа равновесия
Kравн.=
| [CH3COOH]·[C2H5OH] |
| [CH3COOC2H5]·[H2O] |
при 20°С имеет значение 0.28 (т.е. меньше 1). Это означает, что значительная часть эфира не гидролизовалась.
В случае гетерогенных реакций в выражение константы равновесия входят концентрации только тех веществ, которые находятся в газовой или жидкой фазе. Например, для реакции
CO2+C⇄2CO
константа равновесия выражается так:
Kравн.=
| [CO]2 |
| [CO2] |
Значение константы равновесия зависит от природы реагирующих веществ и темпера туры.
От присутствия катализатора константа не зависит, по скольку он изменяет энергию активации и прямой, и обратной реакции на одну и ту же величину. Катализатор может лишь ускорить наступление равновесия, не влияя на значение константы равновесия.
|
|
|
Смещение равновесия под действием различных факторов
Состояние равновесия сохраняется сколь угодно долго при неизменных внешних условиях: температуре, концентрации исходных веществ, давлении (если в реакции участвуют или образуются газы).
Изменяя эти условия, можно перевести систему из одного равновесного состояния в другое, отвечающее новым условиям. Такой переход называют смещением или сдвигом равновесия.
Рассмотрим разные способы смещения равновесия на примере реакции взаимодействия азота и водорода с образованием аммиака:
N2+3H2⇄2HN3+Q
Kравн.=
Дата добавления: 2018-02-28; просмотров: 417; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!
