Хроническое воспаление и инфекции
Возраст и наследственность
Перечисленные в этом разделе факторы являются "неизменяемыми", невозможно изменить возраст человека или его наследственность. Рак может встречаться в любой возрасте, но большинство случаев его развития отмечается после 50 лет. Рак - не наследственная болезнь, но необходимо учитывать, что вероятность заболеть может быть выше, если у кого-то из родственников ранее был установлен подобный диагноз.
Возраст
По мере старения организма повышается риск развития рака. Старение – один из наиболее «влиятельных» факторов риска его развития. Около 50% всех случаев возникновения злокачественных опухолей приходится на возрастную группу от 55 до 74 года (Рисунок 1). Тем не менее, не стоит забывать, что рак может возникать в любом возрасте, и молодой возраст не исключает этот диагноз. Кроме того, существует ряд опухолей, риск развития которых наиболее высок у молодых – например злокачественные новообразования костей, острые лейкозы, нейробластома и т.д.
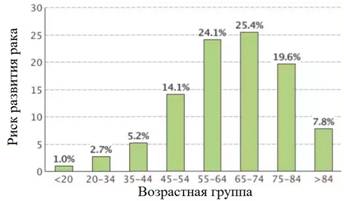
Рисунок 1. Риск развития рака в зависимости от возраста (из базы данных SEER 2007-2011)
Наследственный рак и наследственные синдромы
Как было отмечено в разделе «Что такое рак», рак – генетическая болезнь, которая развивается вследствие повреждения генов. Такие повреждения (мутации) могут развиваться в течение жизни под действием множества факторов, а могут наследоваться от родителей, в таких случаях говорят о развитии наследственного рака. При этом, если в первом случае мутации, вызывающие злокачественную трансформацию клеток обнаруживаются только в опухоли (спорадические или соматические мутации), то в последнем – во всех клетках человеческого организма (герминальные мутации).
|
|
|
Наличие герминальных мутаций может не приводить к каким-либо изменением функций генов («пассажирские мутации»), но в случае нарушения могут сами по себе резко повышать развитие рака или повышать уязвимость клетки к внешним воздействиям.
Наследственные синдромы отвечают за развитие относительно небольшого числа злокачественных опухолей, на их долю приходится от 5 до 10% всех случаев рака. Современной медицине известно около 50 таких синдромов. Ответить на вопрос, развилась ли опухоль на фоне какой-либо наследственной мутации призвано генетическое тестирование (подробнее – в соответствующем разделе). Как правило, его прохождение рекомендуется пациентам, у которых имеется отягощенный наследственный анамнез – то есть у кого-то в семье отмечались случаи развития злокачественных новообразований.
Кроме этого, существует опухоли, которые часто развиваются именно на фоне наличия таких синдромов, например рак яичников или определенный подтип рака молочной железы (тройной негативный вариант, т.е. опухоль, чей рост не зависит от влияния эстрогенов и прогестерона и активности сигнального пути фактора роста эпидермиса). В этих случаях, учитывая, что мутация, которая в дальнейшем будет передаваться по наследству, может возникнуть впервые, врач может рекомендовать консультацию генетика даже при отсутствии отягощенного семейного анамнеза.
|
|
|
Результаты такого тестирования могут быть важны для правильного составления плана обследования, лечения и дальнейшего наблюдения, а также для родных и близких пациента.
К наиболее распространенным мутациям, которые вызывают наследственные синдромы, относят следующие:
· Мутации в генах в генах BRCA1 или BRCA2 (в последнее время получивших в прессе названия «ген Джоли»), который вызывают синдром наследственного рака молочной железы и/или яичников. Данные гены участвуют в работе системы репарации генетического кода клетки – особых ферментов, которые восстанавливают ДНК после повреждения. В случае их неправильного функционирования клетка становится уязвима к внешним воздействиям. Также повышается риск развития рака молочной железы у мужчин, поджелудочной железы и рака предстательной железы (простаты).
|
|
|
· Мутации в гене TP53, которые участвуют в развитии множества опухолей. TP53 – один из ключевых генов, которые подавляют опухолевый рост, в случае, если клетка получает повреждения. Мутации в этом гене являются одними из наиболее часто встречающихся, герминальные мутации TP53 являются причиной развития синдрома Ли-Фраумени, на фоне которого резко повышается вероятность возникновения сарком костей и мягких тканей, рака молочной железы, надпочечников, опухолей головного мозга.
· Мутации в гене PTEN, который так же, как и TP53, является супрессором опухолевого роста. Развитие мутаций в этом гене приводит к возникновению синдрома Каудена (также называется «синдром множественных гамартром), который приводит к ростe множества доброкачественных образований на коже, в ткани молочной железы, кишечника и внутри полости рта. Это приводит к повышению риска развития рака вовлеченных органов.
Вредные привычки и образ жизни
В этом разделе собраны те факторы риска развития злокачественных новообразований, которые можно отнести к вредным привычкам или вредному образу жизни. Именно на их долю приходится подавляющее большинство случае развития рака. В отличие от возраста или наследственности на них можно повлиять - тем самым предотвратить развитие рака у многих людей.
|
|
|
Курение и употребление табака
Табак – ведущая причина развития рака и смертности, он вносит наибольший вклад в смертность от онкологических заболеваний. Доказано повышение развития большого количества злокачественных новообразований на фоне его применения – наиболее изучено его связь с развитием рака легкого, также он повышает риск рака гортани, глотки, полости рака, мочевого пузыря, печени, почек, желудка, толстой кишки, поджелудочной железы и т.д.
Не менее опасны т.н. "бездымные" виды употребления табака, например, жевательный табак, который выраженно повышает риск заболеть раком полости рта, пищевода и поджелудочной железы.
Причиной резкого повышения риска развития вышеперечисленных опухолей является то, что в табаке содержится около 7000 различных химических веществ, около 250 из них являются вредными для человека, 69 – доказано канцерогенными. К ним относятся ацетальдегид, ароматические амины, мышьяк, бензоперен, кадмий, формальдегид и т.д.
Употребление табака и курением обусловлено до 30% всех смертей от онкологических заболеваний.
Курение после установки диагноза онкологического заболевания повышает риск развития его рецидива на 42% по сравнению с некурящими пациентами. У бывших курильщиков этот показатель выше на 15%.
Курение в процессе лечения ухудшает заживление ран и снижает сопротивляемость организма к инфекции, что повышает риск развития осложнений после хирургических операций, в процессе лучевой терапии и химиотерапии
Отказ от курения после установления диагноза злокачественной опухоли снижает риск смерти от неё на 30-40%.
По мере увеличения количества выкуриваемых сигарет и стажа курения риск развития вышеперечисленных опухолей возрастает. Не существует «безопасной дозы» табака. Вне зависимости от возраста человека, отказ от употребление табака оказывает благоприятное влияние на состояние его здоровья.
Помимо вреда своему собственному здоровью, курильщики табака подвергают риску здоровье окружающих их людей – в выдыхаемом дыме остается множество канцерогенных веществ. Так, было показано, что риск развития рака легкого у некурящих людей, которые постоянно проживают с курильщиками, повышается на 20-30%. Помимо этого, у курильщиков и их близких повышается риск развития заболеваний сердца, сосудов, хронической обструктивной болезни легких и т.д.
Употребление алкоголя
Алкоголь (этанол) и содержащие его продукты повышают риск развития рака полости рта, глотки, гортани, пищевода, печени и молочной железы. Из этанола в процессе его метаболизма в организме образуется ацетальдегид, который способен повреждать ДНК и белки клеток, кроме того он приводит к развитию т.н. «оксидативного стресса» - повреждению клеток под действием активных форм кислорода.
У людей разных национальностей риск развития рака под действием алкоголя неодинаков, что, объясняется различиями в интенсивности метаболизма этанола – чем выше активность ферментов, которые его перерабатывают, тем выше риск развития рака.
Риск значительно повышается в случае употребления значительного количества алкоголя. Кроме того, алкоголь значительно усиливает негативное влияние табачного дымы и содержащихся в нем канцерогенных агентов на клетки.
Это не означает, что стоит полностью отказаться от употребления алкоголя – лишь ограничить его потребление, к примеру, рекомендации Американского Института Рака рекомендуют употреблять не более 100 г чистого этанола в неделю женщинам, 200 г – мужчинам (14 г и 28 г в день, соответственно).
Питание и ожирение
Влиянию особенностей питания на развитие онкологических заболеваний было посвящено множество исследований. Коротко, можно сказать, что на сегодняшний день нет данных, что употребление в пищу продуктов или добавок, содержащих антиоксиданты, кальций, витамин D, фтор снижает или повышает риск развития рака. Не было доказано также какого-либо влияния употребления зеленого чая, чеснока, овощей из группы крестоцветных.
Имеются данные, что употребление в пищу термически обработанного мяса может повышать риск развития рака, вследствие наличия в нем химических веществ, получивших название «гетероциклические амины». Однако, их канцерогенность была показано только в нескольких экспериментах на крысах, которым вводились очень высокие дозы этих веществ – в тысячи раз выше, чем то, которое можно употребить с пищей.
Ожирение – состояние, которое характеризуется переразвитием подкожно-жировой клетчатки и жира вокруг внутренних органов. Для диагностики ожирения применяется т.н. «индекс массы тела (ИМТ)», который вычисляется по следующей формуле (она применима только для взрослых пациентов старше 20 лет):
ИМТ = рост/вес2
ИМТ от 18,5 до 24,9 является показателем нормальной массы тела организма, от 25,0 до 29,9 – избыточным весом, 30,0 и более – ожирением.
По сравнению с людьми с нормальной массой тела люди с ожирением имеют повышенный риск развития множества заболеваний, включая сахарный диабет 2 типа, артериальную гипертензию и другие сердечно-сосудистые заболеваний, а также рака. Повышается риск развития злокачественных новообразований органов пищеварительной системы, рака молочной железы, тела матки, почек, желчного пузыря и желчевыводящих путей, а также щитовидной железы. До 40% случаев развития опухолей некоторых локализаций приходится на людей с ожирением, особенно рака эндометрия (тела матки) и пищевода.
Существует несколько механизмов при помощи которых ожирение ведет к развитию рака, основными являются следующие:
· Жировая ткань продуцирует эстрогены – естественные женские половые гормоны, которые повышают риск развития рака молочной железы, тела матки и некоторых других опухолей. Кроме того, она продуцирует ряд других биологически активных веществ, например лептина, который провоцирует процессы деления клеток;
· Ожирение приводит к снижению чувствительности тканей к инсулину (гормон, который вырабатывается в процессе и после приема пищи, необходим, в частности, для правильного распределения полученных питательных веществ), следствием чего является стойкое повышение выработки инсулина поджелудочной железой, а также концентрации в крови инсулин-подобного фактора роста. Инсулин, особенно в высоких концентрациях, стимулирует рост клеток и может оказывать канцерогенное действие;
По данным Организации Объединенных Наций (2013 год) избыточным весом или ожирением в России страдает около 24,9% населения. Существующие тенденции показывают, что при сохраняющихся темпах, ожирение «вытеснит» курение с лидирующих позиций среди причин развития рака. Изменение образа питания, повышение физической активности и нормализация массы тела снижает риск развития рака и его рецидива.
Хроническое воспаление и инфекции
Воспаление – нормальный физиологический процесс, в ходе которого организм пытается устранить причину, вызвавшую повреждение тканей и устранить полученные повреждения. В норме после этого процесс воспаления останавливается, но в некоторых случаях развивается хроническое воспаление.
Хроническое воспаление
В случае хронического воспаления процесс воспаления может начаться даже без явного воздействия внешнего повреждающего фактора и может продолжаться в течение длительного времени. Это может происходить под влиянием некоторых микроорганизмов (вирусов, бактерий, грибов и т.д.) или, например, как следствие ненормальной реакции организма на собственные ткани, что приводит к развитию различных аутоиммунных реакций (болезнь Крона, язвенный колит, атрофический гастрит и т.д.).
Под длительным воздействием воспалительных факторов происходит постоянное повреждение тканей на фоне которого возможно появление злокачественных клеток. Некоторые микроорганизмы-возбудители инфекционных болезней могут повышать риск развития рака. Ниже перечислены наиболее изученные из них.
Вирус папилломы человека (ВПЧ, HPV)
ВПЧ - причина развития практически всех случаев рака шейки матки (РШМ). Кроме того, у носителей данной инфекции значимо повышается риск развития других опухолей наружных половых органов, а также рака головы и шеи. Эта инфекция очень широко распространена в человеческой популяции, так, в США ВПЧ ежегодно поражает около 79 млн. человек. В настоящий момент известно более 150 штаммов этого вируса, при этом только около 15 из них являются онкогенными, т.е. способными приводить к развитию злокачественных новообразований.
В мире РШМ является второй по частоте встречаемости опухолью у женщин. Внедрение повсеместного обследования (скрининга), включающего в себя регулярные осмотры гинекологом со взятием цитологических мазков из шейки матки (цервикального канала), а также определение наличия ДНК ВПЧ в крови позволило резко снизить заболеваемость и смертность от РШМ в развитых странах. На сегодняшний день 9 из 10 случаев смерти от РШМ приходится на бедные регионы и страны.
На сегодняшний день не существует способов лечения ВПЧ, однако в клиническую практику уже внедрены вакцины, которые позволяют резко снизить вероятность развития РШМ, защищая человека от наиболее распространенных штаммов HPV. Очень важно, чтобы вакцинация проводилась до момента первого контакта человека с возбудителем этой инфекции, рекомендуется прививать детей в возрасте от 11 до 12 лет.
Кроме того, РШМ не развивается моментально. Его развитию предшествуют предопухолевые изменения эпителия – дисплазия, затем – т.н. «цервикальная неоплазия in situ», которая представляет собой самую раннюю стадию РШМ. Своевременная диагностика и лечение таких процессов позволяет предотвратить развитие РШМ.
Вирусные гепатиты С и В (HCV и HBV)
Хроническая инфекция, вызванная этими возбудителями, может приводить к развитию цирроза и рака печени, кроме этого доказана их связь с развитие некоторых лимфом. В настоящее время широко применяются вакцины против вирусного гепатита B, они позволяют эффективно предотвращать заражение и развитие хронической HBV инфекции, снижая тем самым вероятность развития рака печени.
К сожалению, не существует профилактических вакцин против вируса гепатита С. Это обусловлено высокой мутационной изменчивостью этого вируса, что резко затрудняет разработку и создание таких препаратов. Тем не менее, в настоящее время разработаны весьма эффективные противовирусные лекарственные препараты, которые могут подавить размножение или полностью уничтожить вирус в организме.
Вирус иммунодефицита человека (ВИЧ, HIV)
Этот широко известный вирус вызывает развитие СПИД – синдрома приобретенного иммунодефицита. ВИЧ ослабляет иммунную систему организма, делая её неспособной сопротивляться воздействиям различных микроорганизмов (например тех, что перечислены в этом разделе). Люди, инфицированные ВИЧ, характеризируются повышенным риском развития саркомы Капоши, лимфом, РШМ, печени, легких и других опухолей.
Вакцины от ВИЧ не существует, но разработаны специальные препараты для противовирусной терапии, которые позволяют подавить размножение этого вируса и значительно продлить жизнь пациентам.
На фоне подавления иммунитета другого происхождения, например у пациентов, получающих длительное лечение иммуносупрессивными препаратами после трансплантации органов или высокими доза глюкокортикостероидов (например, преднизолон, дексаметазон и т.д.) также повышается риск развития множества опухолей.
Вирусы герпеса
К наиболее онкогенным видам этих вирусов относят вирус Эпштейн-Барр (EBV), который повышает риск развития лимфомы и рака желудка, а также носоглотки. Штамм 8 вируса герпеса ассоциирован с развитием саркомы Капоши.
Бактерии и грибы
Helicobacter pylori (HP) – бактерия, которая может колонизировать слизистую оболочку желудка. На фоне вызванной ей инфекции повышается риск развития язвенной болезни желудка и двенадцатиперстной кишки, а также рака желудка. HP инфекция хорошо поддается лечению антибактериальными препаратами.
Кроме того, некоторые грибки (например,Aspergillus flavusи Aspergillus parasiticus) в процессе своей жизнедеятельности вырабатывают афлатоксины – вредные ещества, которые могут загрязнять сельскохозяйственную продукцию. Распространенность этих грибков велика в жарких и влажных странах, афлатоксины могут попадать в пищу в поле, в процессе сбора урожая и во время её хранения. Употребление в пищу афлатоксинов повышает риск развития рака печени.
Паразиты
К наиболее онкогенным паразитам относят Schistosoma hematobium(возбудитель шистосомоза), который может вызывать рак мочевого пузыря и Opisthorchis viverrini(возбудитель описторхоза), на фоне которого повышается риск развития рака желчевыводящих путей (холингиокарциномы).
Следует помнить, что отсутствие симптомов инфекции не означает отсутствия самой инфекции.
Гормоны
Некоторые гормоны, особенно женские половые гормоны эстрогены, обладают канцерогенными свойствами. Несмотря на то, что они являются физиологически необходимыми веществами, их воздействие может повышать риск развития и рецидива некоторых злокачественных новообразований.
Так, например, на фоне применения заместительной гормональной терапии (ЗГТ) с применением эстрогенов и прогестерона (комбинированная ЗГТ) отмечается повышение риска развития рака молочной железы (РМЖ), на фоне ЗГТ только эстрогенами (без прогестерона) – рака эндометрия.
ЗГТ наиболее часто применяется для контроля симптомов наступления менопаузы, например, таких, как «приливы» или снижение минеральной плотности костной ткани (остеопороз). Может применяться как однокомпонентная ЗГТ эстрогенами, так и комбинированная терапия эстрогенами в сочетании с прогестероном или прогестинами. Однокомпонентная терапия чаще назначается пациенткам, ранее перенесшим удаление матки (гистерэктомию), в остальных случаях, вследствие вышеупомянутого повышения риска развития рака эндометрия, назначается комбинированная ЗГТ.
В крупном исследовании было показано, что применение комбинированной ЗГТ обладает некоторыми преимуществами. Она примерно на 30% снижает риск развития переломов и возникновения колоректального рака. .Тем не менее, эти преимущества являются кратковременными, и исчезают после завершения применения ЗГТ. В то же время, только ЗГТ эстрогенами приводит к небольшому снижению риска развития РЖМ. Вместе с тем, применение ЗГТ ассоциировано со следующими рисками:
· Удвоение риска развития деменции (ухудшение памяти вплоть до развития слабоумия) на фоне применения комбинированной ЗГТ;
· Развитие инсульта, тромбозов и инфаркта на фоне применения обоих видов ЗГТ;
· Развитие РМЖ на фоне применения комбинированной ЗГТ, в том числе – распространенных его форм. Кроме того, применение ЗГТ снижает эффективность применения маммографии для раннего выявления этого злокачественного новообразования.
· Риск смерти от РМЖ повышается примерно в два раза, смерти от других причин – примерно на 50%.
Если Вы планируете начать прием ЗГТ – обязательно обсудите возможные риски и преимущества с Вашим лечащим врачом. Безопасность её применения у онкологических пациентов неизвестна.
Продукция гормонов в организме также изменяется при ряде физиологических состояний. Так, было показано, что риск развития РМЖ повышается при раннем появлении менструаций (менархе) и позднем наступлении менопаузы, и напротив – уменьшается при сокращении периода менструаций. Риск развития этого злокачественного новообразования также повышается у никогда не рожавших женщин, напротив – беременность и роды снижают этот риск.
Другим примером терапии с использованием женских половых гормонов являются некоторые противозачаточные препараты. В клинической практике широко применяются комбинированные оральные контрацептивы (КОК), которые как и препараты для ЗГТ содержат эстрогены и прогестерон, но в гораздо более низких дозах.
КОК используются как одно из наиболее эффективных средств для предотвращения нежелательной беременности, кроме того они применяются для лечения ряда гинекологических заболеваний, например, эндометриоза или поликистоза яичников.
Влияние КОК на риск развития злокачественных новообразований не одинаково. Так, было показано, что на фоне их применения наблюдается некоторое повышение вероятности развития РМЖ, которая, однако, снижается до среднего уровня течение 10 лет с момента прекращения их приема.
Кроме того, РМЖ у пациенток, принимающих КОК, как правило, диагностируется на более ранних стадиях. Предполагается также, что КОК могут незначительно повышать риск развития рака шейки матки и доброкачественных опухолей печени.
В то же время, КОК снижают риск развития рака яичников – примерно на 50% после их применения в течение 5 лет, в том числе, в одном исследовании было показано выраженное снижение риска развития этого новообразования у женщин-носителей мутации в гене BRCA1. Их применение также снижает риск развития рака эндометрия.
Ультрафиолетовое и радиоактивное излучение
Человек непрерывно подвергается воздействию различного облучения. Каждый раз выходя на солнце, на нас оказывает воздействием ультрафиолетовое излучение, вредное воздействие которого зачастую недооцениваются и многие люди беспечно проводят свое время под открытым солнцем не понимая, что это может привести к печальным последствиям.
Солнечный свет (ультрафиолетовое излучение)
Ультрафиолетовое (УФ) излучение – часть спектра естественного солнечного света. Оно всегда присутствует в составе солнечного света, свете солнечных ламп, а также устройствах для искусственного загара.
УФ излучение способно повреждать кожу, вызывать её преждевременное старение и повышать риск развитий злокачественных новообразований кожи, особенно - меланомы. Риск их развития особенно высок на фоне солнечных ожогов.
Вне зависимости от возраста людям следует ограничивать время пребывания под активным солнцем и избегать других источников УФ излучения, особенно – соляриев. Наиболее активное солнечное излучение отмечается в период с 10:00 до 16:00.
При неизбежности пребывания на солнце в «неблагоприятные часы» рекомендуется носить одежду с длинными рукавами, головной убор и солнечные очки с линзами, поглощающими УФ лучи. Нанесение на кожу солнцезащитного крема с фактором защиты (Sun Protection Factor [SPF]) ≥15 также может быть полезно. Важно помнить, что УФ лучи отражаются от песка, воды, снега и льда, а также свободно проходят через ветровые щиты и стекло.
Радиоактивное излучение
Радиоактивные волны определенной длины, называемые «ионизирующим излучение» обладают достаточной энергией, чтобы вызвать повреждение ДНК, что может привести к развитию рака. Примерами источников ионизирующего излучения является радон, радиоактивные элементы, рентгеновские установки и т.д. Кроме того, Земля и все живые организмы регулярно подвергаются воздействию космического излучения. Массивные выбросы радиоактивного излучения происходят при авариях на атомных электростанциях (АЭС) и после взрывов ядерных боеприпасов, наиболее известными примерами являются авария на Чернобыльской АЭС и бомбардировки японских городов Хиросимы и Нагасаки.
Проведения ряда медицинских обследований сопряжено с применением радиоактивного излучения. Наиболее часто применяются:
· Рентгенография, например, рентген легких, флюорография, рентген костей;
· компьютерная томография (КТ);
· позитронно-эмиссионная томография (ПЭТ);
· радионуклидные исследования, например, сцинтиграфия костей (скинирование).
Стоит отметить, что дозы излучения, которые используются при проведении этих исследований, как правило, минимальны и польза от их проведения значительно превосходит возможные риски.
Радон – радиоактивный газ, продукт естественного распада радия, который может излучаться некоторыми смолами и горными породами. Он не имеет цвета, запаха и вкуса, способен просачиваться сквозь почву и распространяться в воздухе и воде. Как правило, концентрация радона в окружающей среде минимальна и не представляет серьезной опасности для здоровья.
Тем не менее, в плохо вентилируемых местах возможно его накопление, например в подвалах и шахтах. Радон способен проникать в дома через трещины в полах, стенах и фундаменте, кроме того, его источниками могут быть строительные материалы Люди, которые подвергаются воздействию высоких доз радона, имеют повышенный риск развития рака легкого. Для бытового применения доступны специальные устройства-тестеры, которые позволяют измерять уровень радона в помещении.
На сегодняшний день невозможно абсолютно точно определить, почему одного человека развивается рак, а у другого нет. Тем не менее, установлен ряд факторов, которые повышают риск развития злокачественных новообразований – так называемых факторов риска. Они включают в себя долговременный контакт с различными химическими или физическими факторами (канцерогенами), а также возраст человека и его наследственность – риск развития рака возрастает по мере старения; наличие кровных родственников, у которых ранее отмечалось развитие рака, также может говорить о повышенном риске его развития у человека. Кроме того, современной медицине известно несколько наследственных синдромов, когда у членов одной семьи развиваются однотипные опухоли (см. раздел «Наследственные синдромы»).
Большинство факторов риска развития злокачественных новообразований было обнаружено в ходе широкомасштабных эпидемиологических исследований, в рамках которых ученые сравнивали между собой различных людей, больных и здоровых, и пытались определить, какие различия в их образе жизни, профессии, привычках, месте проживания и т.д. повышают или снижают риск развития рака.
Следует ещё раз подчеркнуть, что сами по себе такие исследования не способны определить точную причину развития рака у отдельного человека – только повышение или снижение риска его развития. После выявления связи между каким-либо фактором и развитием злокачественной опухоли необходимо проведение дальнейших исследований, включая выяснение механизмов возникновения рака под действием изучаемого фактора и воспроизведение полученных данных в эксперименте. В подразделах перечислены наиболее изученные факторы риска развития злокачественных новообразований. Кроме них, канцерогенным эффектом могут обладать продукты горения нефти и её производных, твердых источников топлива (древесный уголь), некоторые тяжелые металлы и т.д.
·
·
·
·
·
·
·
·
Дата добавления: 2018-02-28; просмотров: 371; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!
