Адсорбция. Изотерма адсорбции. Уравнение Гиббса.
Самопроизвольное изменение концентрации вещества в поверхностном слое, отнесенное к единице поверхности, называется адсорбцией, обозначается через Г и выражается в кмоль/м2, или моль/см2.
Если Г>0 адсорбцию называют положительной, если Г<0 - отрицательной.
Если растворенное вещество не изменяет 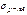 , адсорбция Г=0 и вещество равномерно распределено между поверхностным слоем и объемом.
, адсорбция Г=0 и вещество равномерно распределено между поверхностным слоем и объемом.
Простое термодинамическое соотношение между поверхностной концентрацией Г и изменением ПН с активной концентрацией растворяемого вещества  было выведено Гиббсом:
было выведено Гиббсом:

где  - активность раствора;
- активность раствора;
 - универсальная газовая постоянная;
- универсальная газовая постоянная;
 - абсолютная температура.
- абсолютная температура.
Для разбавленных растворов активность заменяют концентрацией С:
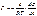
Из уравнения следует, что только те вещества показывают положительную адсорбцию, с повышением концентрации которых ПН понижается, 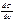 <0.
<0.
Если  >0, концентрация растворенного вещества в поверхностном слое будет уменьшаться: Г<0.
>0, концентрация растворенного вещества в поверхностном слое будет уменьшаться: Г<0.
Вещества, повышающие ПН, называются отрицательно поверхностно-активными веществами (инактивными, ими являются неорганические соли).
Вещества, понижающие ПН называют поверхностно-активными (ПАВ) (см. стр. 98-102).
К ПАВ относятся органические вещества, молекулы которых построены из участков с резко различающимися свойствами. Одна часть молекулы полярная, другая – неполярная (углеводородный радикал).
Полярная: -OH, -COOH, -SO3Na, -SO3H, -NH2, -SO2H.
|
|
|
Полярная часть гидрофильна, неполярная – гидрофобна.
ПАВ характеризуются величиной ГЛБ (гидрофильно-липофильного баланса).
Величина  , согласно Ребиндеру, является мерой способности вещества понижать поверхностную энергию, она называется поверхностной активностью и обозначается
, согласно Ребиндеру, является мерой способности вещества понижать поверхностную энергию, она называется поверхностной активностью и обозначается  . Ее размерность – Н/м.
. Ее размерность – Н/м.
В гомологическом ряду жирных кислот, спиртов и аминов понижение  тем больше, чем длиннее цепь.
тем больше, чем длиннее цепь.
Согласно правилу Дюкло-Траубе, при удлинении цепи на группу СН2 поверхностная активность  возрастает на границе раствор-воздух в 3-3,5 раз.
возрастает на границе раствор-воздух в 3-3,5 раз.
Для определения этой характеристики строят зависимость 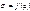 . Используя уравнение Гиббса, строят зависимость
. Используя уравнение Гиббса, строят зависимость  .
.
Адсорбция - протекание процесса сорбции только на поверхности, увеличивается концентрация вещества на границе раздела фаз.
Абсорбция - поглощение вещества всем объемом другого вещества. При абсорбции поглощаемое вещество диффундирует вглубь абсорбента
Вещество, на поверхности которого идет адсорбция, называется адсорбентом, т.е. адсорбент - это вещество, адсорбирующее другое вещество.
Вещество, которое адсорбируется, называется адсорбтивом или адсорбатом.
Различают адсорбцию физическую и химическую.
|
|
|
Физическая адсорбция обеспечивается силами Ван-дер-Ваальса, протекает самопроизвольно, молекулы адсорбтива могут перемещаться по поверхности (нелокализованная адсорбция), характеризуется обратимостью, отсутствием стехиометрических соотношений, уменьшением адсорбции при повышении температуры, сопровождается десорбцией. Процессы адсорбции и десорбции находятся в равновесии: адсорбция «десорбция.
Химическая адсорбция или хемосорбция обусловлена химическим взаимодействием адсорбента с адсорбтивом. Молекулы адсорбтива не могут перемещаться по поверхности адсорбента. Необратима. Тепловой эффект близок к энергии образования химических соединений. Повышение температуры способствует хемосорбции.
Применение ПАВ Даже очень малые добавки этих веществ изменяют условия взаимодействия соприкасающихся тел и природу их поверхности.
ПАВ используют:
- для облегчения разрушения, например, при тонком помоле веществ;
- при распылении жидкостей;
- для уменьшения трения между поверхностями;
- при стирке;
- в качестве эмульгаторов при производстве косметических и фармацевтических препаратов.
Дата добавления: 2015-12-18; просмотров: 18; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!
