Реагентная нейтрализация
Реагенты для нейтрализации кислых сточных вод выбирают в зависимости от вида кислот и их концентрации. Кроме того, учитывают, образуется ли в процессе реакции нейтрализации осадок. Для нейтрализации минеральных кислот применяют любой щелочной реагент, но чаще всего следующие: известь в виде пушонки или известкового молока, а также карбонаты кальция или магния в виде суспензии.
В практике очистки сточных вод доза нейтрализующего реагента обычно принимается на 10 % больше стехиометрического соотношения. Указанные данные представлены в табл. 5.2.
Количество реагентов для нейтрализации сточных вод может быть рассчитано по следующей формуле: 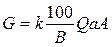 ,
,
где G— количество реагентов, кг; k— коэффициент запаса расхода реагента по сравнению с теоретическим (для известкового молока k= 1,1, для известкового теста и сухой извести k= 1,5); В — количество активной части в товарном продукте, %; Q- количество сточных вод, подлежащих нейтрализации, м; а- расход реагента для нейтрализации, кг/кг; А- концентрация кислоты или щелочи, кг/м3. Следует указать, что наиболее дешевым реагентом является гидроксид кальция (известковое молоко) с содержанием активной извести Ca(OH)2 5-10%.
При нейтрализации сточных вод, содержащих серную кислоту кальциевыми реагентами, образуется гипс CaSO4·2Н2О, растворимость которого в температурном интервале 0-40 °С лежит в пределах 1,76-2,11 г/л. При более высокой концентрации CaSO4·2H2O выпадает в осадок, забивая трубопроводы и аппаратуру. Для устранения этого явления рекомендуется промывать трубопроводы чистой водой и увеличивать скорость движения нейтрализованных вод в них. Кроме того, хороший эффект дает введение в сточные воды специальных умягчителей (гексаметафосфат), а также замена металлических трубопроводов на пластмассовые.
Дата добавления: 2016-01-06; просмотров: 86; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!
