Тұндыру әдісінің теориялық негізі.Гей-Люссак және Мор әдістеріне сипаттама.
Тұндыру әдісімен титрлеу нашар ертін қосылыста түзілетін реакцияларға негізделген. Бұл реакциялар бөлме температурасында жеткілікті тез және іс жүзінде қайтымсыз өтеді.Тұндыру реакцияларының көптігіне қарамастан, тұндырып титрлеу кең таралмады. Тұндыру тәсілімен титрлеу әдістерінің ең кең тараған аргентометрия және меркуриметрия, сондай ақ роданидометрия және цианометрияны атап көрсете аламыз. Тұндырып титрлеуді басқа әдістері сирегірек қолданылады, себебі олар үшін эквиваленттіе нүктесін белгілеп алатын сенімді индикаторлар табылған жоқ.
Гей-Люссак тәсілі -1832жылы ашқан (тепе-тең лайлану тәсілі)Тең лайлану әдісі. Хлоридті күміс нитратымен титрлегенде бұл әдісте эквиваленттік нүктесінің маңында мөлдір ерітіндіден шамалы порциядан алып, бір порциясына 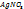 , екіншісіне натрий хлор қосады. Егер эквиваленттік нүктесіне жетсе, екі порциядағы да лайлану бірдей болады. Титрін жетпеген ерітінділерде лайлану тек қана бірінші жағдайда, яғни
, екіншісіне натрий хлор қосады. Егер эквиваленттік нүктесіне жетсе, екі порциядағы да лайлану бірдей болады. Титрін жетпеген ерітінділерде лайлану тек қана бірінші жағдайда, яғни 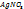 қосқанда, ал артық титрленген ерітінділерде – тек натрий хлор қосқанда болады. Бұл әдістің дәлдігі өте жоғары болса да, оны өте сирек қолдануда, себебі оған қарағанада қарапайым әдістер бар.
қосқанда, ал артық титрленген ерітінділерде – тек натрий хлор қосқанда болады. Бұл әдістің дәлдігі өте жоғары болса да, оны өте сирек қолдануда, себебі оған қарағанада қарапайым әдістер бар.
Мор әдісі. Титрлеудің соңындағы нүктеде  күміс хроматынын қызыл кірпіш тұнбасының түзілуіне әдістің идеясы негізделген. Бұрын көрсетілгендей, эквиваленттік нүктесінде
күміс хроматынын қызыл кірпіш тұнбасының түзілуіне әдістің идеясы негізделген. Бұрын көрсетілгендей, эквиваленттік нүктесінде
|
|
|
[  ] = [
] = [  ] =
] =  = 1,3 *
= 1,3 *  M.
M.
Күміс иондарының концентрациялары тепе-тең болғанда,  жету үшін қажет
жету үшін қажет 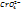 иондарының концентрациясын есептеуге болады. Ол тең болады:[
иондарының концентрациясын есептеуге болады. Ол тең болады:[ 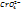 ] =
] =  /[
/[  ] = 1.1 *
] = 1.1 *  /(1,3 *
/(1,3 *  )= 6.2 *
)= 6.2 *  M.
M.
Күміс хроматының тұнбасының мұндай концентрациясының көзбен көруге болмайды. Күміс хроматы тұнбасын көзбен көру үшін анализденетін ерітіндісіне 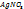 ерітіндісінің бір тамшысын артық тамызып титрлесе болғаны индикатор түсін байқай аламыз.
ерітіндісінің бір тамшысын артық тамызып титрлесе болғаны индикатор түсін байқай аламыз.
Бұл әдісте индикатор калий хроматы болып табылады. Хроматпен титрлеу бейтарап немесе әлсіз сілтілік ортада, ерітіндінің рН 6.5-10.5 аралығында болғанда жүргізіледі. Сілтілік ортада гидрохромат ионмен тепе-теңдікте болатын хромат иондары басымырақ, алдынғысының түзілуі қышқылдау аймақта мына теңдеуге сәйкес басталады:
 +
+ 

pH  6.5 болғанда индикатордың сезгіштігі төмендейді, ал рН
6.5 болғанда индикатордың сезгіштігі төмендейді, ал рН  10.5 болса тұнбаға түсіп, анализ нәтижелерін дұрыс көрсетпейтін күміс гидроксидтері және оксидтері түзілуі мүмкін. Бұрын аталғандай Мор әдісімен хлоридтер және бромидтер анықталады. Иодиттер мен тиоцианаттарды бұл әдіс бойынша титрлеу олардың адсорбциялануына байланысты тәжірибеде мүмкін емес. Бұл жағдайда эквиваленттік нүктесін анықтау қиын.
10.5 болса тұнбаға түсіп, анализ нәтижелерін дұрыс көрсетпейтін күміс гидроксидтері және оксидтері түзілуі мүмкін. Бұрын аталғандай Мор әдісімен хлоридтер және бромидтер анықталады. Иодиттер мен тиоцианаттарды бұл әдіс бойынша титрлеу олардың адсорбциялануына байланысты тәжірибеде мүмкін емес. Бұл жағдайда эквиваленттік нүктесін анықтау қиын.
48.Фольгард тәсіліне сипаттама,жүру жағдайы, қолданылатын индикатор.
|
|
|
Күмістің тиоцианат-ионымен әрекеттесу реакциясын есепке алып, галогенид –иондарды анықтау үшін кері титрлеу әдісін қолданылады. Галогенидтердің (хлорид не бромид) анализденетін ертіндісіне күміс нитратынның титрленген ерітіндісінің артық мөлшерін қосады,тұнбаға түспеген күміс иондарын темір (III) иондары бар тиоционат ионымен титрлеймиз.
Индикатор –темір (III) тиоционат комплексі.
Пайдаланатын темір реакциясы 10-5 М тиоцианатты анықтауға мүмкіндік туғызады. Эквиваленттік нүктеде иондар концентрациясы тең болады.
[Ag+]=[SCN-]=√EKAgSCN =√1,1*10-2 = 1,05*10-6 M
Тиоцианаттың мұндай концентрациясында темірдің тиоцианаттық комплексінің бояуын анықтау мүмкін емес. Калий тиоциатының артық тамшысынан анық қызғылт сары бояу пайда болады.
|
|
|
Фольгард әдісі, күміс ионымен нашар еритін қосылыстар түзетін, мысалы: оксалаттар, фосфаттар жіне басқалар сияқты аниондарды титрлеуге мүмкіндік туғызады. Титрлеуді қышқыл ортада өткізеді, бұл әдістің елеулі құндылығы болып табылады.
Дата добавления: 2016-01-03; просмотров: 1; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!
