Представители риккетсий и их роль в патологии.
Раздел 1.Общая микробиология.
1. Медицинская микробиология. Предмет, методы, задачи.
Медицинская микробиология (от греч. micros - малый, bios - жизнь, logos - учение) - наука, изучающая возбудителей инфекционных заболеваний человека и представителей собственной микрофлоры организма (морфологию, физиологию, экологию, биологические и экологические свойства, взаимоотношения с другими формами жизни), разрабатывает методы их культивирования и идентификации, диагностики, профилактики и лечения.
Предметом изучения медицинской микробиологии являются патогенные (болезнетворные) и условно-патогенные (в том числе и нормальная микрофлора организма человека) микробы.
Задачи:
1) Выявить возбудителей инфекционных болезней
2) Установить этиологическую роль м/о в норме и при патологии
3) Контроль за чувствительностью м/о к антибиотикам и др.препаратам
4) Разработка методов диагностики, специфической профилактики(вакцины), лечения(леч.сыворотки) инфекционных заболеваний
5) Микробиологический контроль окр. среды, продуктов питания, соблюдения режимов стерилизации, надзор за источниками инфекции в мед-х учреждениях.
Методы направлены на изучение свойств микробов, обусловливающих их патогенное действие, и процессы, которые возникают под их влиянием в организме человека и животных.
К основным методам микробиологии относятся:
1. микроскопический - изучение морфологических и тинкториальных признаков м/о с использованием специальной микроскопической техники (световая иммерсионная, темнопольная, фазово-контрастная, люминесцентная, электронная) ВИДИМ: форму, вид, расположение.
|
|
|
2. Метод культивирования м/о – выделение чистой культуры микробов и изучение их биологических свойств, позволяющие провести идентификацию.
-бактериологический
-вирусологический
3. серологический –применение иммунологических реакций для идентификации м/о по антигенной структуре, выявление антител к возбудителям в биологических жидкостях организма больного (чаще в сыворотке крови; от лат. serum - сыворотка); ИФА, РИФ, РИА
4. аллергологический – метод изучения инфекционно аллергии ГЗТ (клеточного иммунитета) –хр.паразит.-х инф-х. Оценка аллергических феноменов, возникающих в организме человека (на коже, слизистых оболочках или в крови) под действием компонентов или цельных клеток микроба-возбудителя; Не применяется в вирусологии
5. биологический - моделирование инфекционных процессов на лабораторных животных или куриных эмбрионах;
6. молекулярно-генетический – идентификация м/о по генетической структуре-изучение состава микробных нуклеиновых кислот с помощью ПЦР- полимеразной цепной реакции.
|
|
|
7. Экспресс методы диагностики – для установления наличия возбудителя в исследуемом материале (сыворотка крови, моча, слюна, с/м жидкость, мокрота) без выделения чистой культуры
-меченые серологические реакции- ИФА, РИФ, РИА- для выявления антигена возбудителя в биол.материале
-ПЦР- выявление фрагментов нуклеиновых кислот: РНК и ДНК
2. Начальный период развития микробиологии (А. Левенгук и др.)
Историю развития микробиологии можно разделить на пять этапов:
1. Эвристический - до изобретения микроскопов, связан с логическими и методическими приемами. (Гиппократ, Варрон и др.- предположения о природе заразных болезней) Фракасторо был одним из основоположников науки о причинах, условиях и механизмах формирования инфекционных заболеваний и способах их профилактики.
2. Морфологический – Левенгук (голлад-й) сконструировал «микроскоп», позволивший увеличивать рассматриваемые предметы в 300 раз, увидел «анималькулюсы». - в 1675 г. впервые описал простейших, в 1683г. ― основные формы бактерий: кокки, палочковидные и извитые. Он повсюду обнаруживал этих маленьких «зверушек»: в дождевой воде, испражнениях, зубном налете - и пришел к выводу, что окружающий мир густо заселен микробами. Однако тогда это был как интересный факт, который не имеет существенного практического значения.
|
|
|
3. Физиологический
Л. Пастер открыл:
1) природу брожения-вызывают м/о;
2) анаэробиоз;
3) опроверг теорию самозарождения-стерильный бульон в колбе с изогнутой S-образной трубкой не прорастают м/о;
4) обосновал принцип стерилизации- заложил основы дезинфекции, асептики и антисептики ;
5) разработал принцип вакцинации и способы получения вакцин
Роберт Кох (1843—1910) предложил окраску бактерий, микрофотосъемку, способ получения чистых культур, а также знаменитую триаду, получившую название триада Генле—Коха:
1) чтобы микроб обнаруживался только у больного и не обнаруживался у здоровых людей и бальных другими болезнями;
2) должна быть получена чистая культура микроба;
3) микроб должен вызвать аналогичное заболевание при заражении животных.
НО иногда трудно воспроизвести болезнь у животных, так как нет модели (например, ВИЧ-инфекция); нередко возбудитель обнаруживается у здоровых лиц (носительство).
4. Иммунологический - был создан ряд теорий иммунитета: гуморальная теория П. Эрлиха, фагоцитарная теория И. И. Мечникова- учение о невосприимчивости (иммунитете), разработав теорию фагоцитоза и обосновав клеточную теорию иммунитета, теория идиотипических взаимодействий Н. Ерне, гипофизарно-гипоталамо-адреналовая теория регуляции иммунитета П. Ф. Здродовского и др.
- Р. Кох открыл такую форму реагирования иммунной системы, как ГЗТ; Ш. Рише, Ж. Портье, Г. П. Сахаров описали ГНТ; обе эти формы реагирования легли в основу учения об аллергии (К. Пирке, 1906).
- открыта толерантность к антигенам (П. Медовар, М. Гашек), а также иммунологическая память (Ф. Бернет и др.).
-изучение лимфоцитов, их роли в иммунитете, кооперативным взаимоотношениям между Т- и В-лф и фагоцитирующими клетками, киллерная функция лимфоцитов и т. д.
-изучена структура иммуноглобулинов (Р Портер и Д. Эдельман), открыты интерферон (А. Айзекс и Ж. Линдеман), интерлейкины (ИЛ) и другие иммуномодуляторы.
|
|
|
Иммунология в середине XX в. оформилась как самостоятельная наука, имеющая свои цели и задачи в области медицины, свою структуру и классификацию
5. Молекулярно-генетический - Достижения обеспечили успехи в борьбе с инфекционными болезнями и открыли новые пути и методы диагностики и терапии неинфекционных болезней, связанных с нарушениями в иммунной системе. Так как:
-была расшифрована молекулярная структура многих бактерий и вирусов, строение и состав их генома, структура АГ и АТ, факторов патогенности бактерий и вирусов, а также факторов иммунной защиты (комплемент, интерферон, иммуномодуляторы и др.).
-Генная инженерия позволила получать вакцинные (живые, синтетические, генно-инженерные) (против геп. В, ВИЧ-инфекции) и диагностические препараты на основе моноклональных АТ
-Открыты и используются иммуномодуляторы эндогенного и экзогенного происхождения для коррекции иммунного статуса.
-Разрабатывается иммуногенетика, целью которой является генопрофилактика и генотерапия иммунодефицитов. Генодиагностика – ПЦР
-Изучены системы гистосовместимости (НLA-системы), трансплантологии при решении проблемы преодоления иммунологической несовместимости при пересадках органов и тканей, а также в проблеме несовместимости матери и плода в акушерстве и гинекологии.
- Создано большое количество противовирусных и антибактериальных препаратов.
3. Работы Л. Пастера и Р. Коха. Их значение в становлении и развитии микробиологии.
Луи Пастер сделал ряд открытий во многих областях науки, что позволило ему стать основоположником : микробиологии, биотехнологии, дезинфектологии, стереохимии. Он открыл:
1) природу брожения (молочнокислое, спиртовое, уксусное) — это биологическое явление, которое вызывается микробами, их ферментами.
2) анаэробиоз; а группа микробов получила название анаэробов.
3) опроверг бытовавшую в его времена теорию самозарождения; Он доказал, что если стерильный бульон оставить в открытой колбе, то он прорастет, но если стерильный бульон поместить в колбу, которая сообщается с воздухом через спиралью изогнутую стеклянную трубку, то бульон не прорастет, так как бактерии с частицами пыли из воздуха будут осаждаться на изогнутых частях спиральной трубки и не попадут в бульон.
4) обосновал принцип стерилизации; Пастеризация-это прогревание при 120-140°С с целью уничтожения бактерий, которая послужила основанием для разработки принципов асептики и дезинфекции.
5) разработал принцип вакцинации и способы получения вакцин против куриной холеры, сибирской язвы и бешенства-антирабическая, он делает очень важный вывод, что ослабленные (аттенуированные) микробы, введенные в организм, создают в нем иммунитет против последующих заражений вирулентными микробами.
6) Он доказал, что при выращивании грибов усваиваются лишь определенные стереоизомеры.
Роберт Кох (1843—1910) предложил окраску бактерий-анилиновые красители, микрофотосъемку, способ получения чистых культур, а также знаменитую триаду, получившую название триада Генле—Коха: для доказательства роли микроба в возникновении специфической болезни необходимо три условия:
1) чтобы микроб обнаруживался только у больного и не обнаруживался у здоровых людей и бальных другими болезнями;
2) должна быть получена чистая культура микроба;
3) микроб должен вызвать аналогичное заболевание при заражении животных.
Но в наше время иногда трудно воспроизвести болезнь у животных, так как нет модели (например, ВИЧ-инфекция); нередко возбудитель обнаруживается у здоровых лиц (носительство).
Р.Коху удалось культивировать и описать возбудителя сибирской язвы, стафилококка, возбудителей раневых инфекций и столбняка, возбудителя туберкулеза (палочка Коха) и туберкулина, который нашел применение в диагностике этой инфекции, холерного вибриона и пути его передачи, открыл возбудителей возвратного тифа, трипаносомоза и других инфекций.
4. Основные принципы систематики бактерий. Таксономические категории. Критерии вида.
В основу таксономии микроорганизмов положены их генетическое родство, морфологические, физиологические, биохимические, антигенные и молекулярно-биологические свойства
| 2 формы: -Неклеточные формы - это вирусы и прионы. -Клеточные формы – бактерии, грибы, простейшие. | Классификация: Царство (Эукариоты, прокариоты, вирусы), Отдел у прокариот (Скотобактерии, цианобактерии), Класс скотобактерий (бактерии, рикеттсии, мягкотелые), Порядок (Спирохеты,Актиномицеты), Семейство, Род (1 слово), Вид (2 слова). |
Вид — это совокупность особей, объединенных по близким свойствам, но отличающихся от других представителей рода.
Подвид – разновидность внутри одного вида, они отличаются по физиологическим (biovar), морфологическим (morphovar) или по антигенным (serovar) свойствам.
Чистая культура – это совокупность однородных микроорганизмов, выделенных на питательной среде, характеризующихся сходными морфологическими, тинкториальными (отношение к красителям), культуральными, биохимическими и антигенными свойствами
В микробиологии существуют также более мелкие таксономические единицы, чем вид:
Штамм- это чистая культура микроорганизмов, выделенных из определенного источника и отличающихся от других представителей вида. Разные штаммы одного и того же вида бактерий могут отличаться друг от друга по целому ряду свойств, например, по чувствительности к антибиотикам, способности к синтезу токсинов, ферментов и др
Клон –это совокупность потомков, выращенных из единственной клетки м/о – чистая культура.
Критерии вида:
а) морфологический -световая и иммерсионная микроскопия (установить род и семейство);
б) тинкториальные свойства – отношение к разным красителям ГРАМ+ и - (способность окрашиваться и расположение: поодиночке, группами, в цепочку); (установить род и семейство);
в) культуральный –метод культивирования (бактериологич и вирусологич) (установить род и семейство);
1)тип дыхания – аэробный, факультатив.анаэроб
2)тип питания:
нетребовательны к питательным средам- МПА и МПБ- автотрофы;
требовательные к питательным средам – гетеротрофы -элективные пит.среды- кровяной и сывороточный МПА
3)оптимальная температура в термостате (в основном 37; для возб-ля чумы-28, кампилобактерии-42)
4) Время культивирования в основном 18-24 часа; в-ль туберкулеза-месяц и более, в-ль бруцеллеза – около месяца, в-ль туляремии – 2 недели, Legionella pneumonia – 3-5 дней, Bordetella pertusis (коколюш)- 3-4 дня
5)Характер роста колоний:
на твердых питательных средах все образуют *S-колонии- округлой формы, гладкая поверхность, ровный край, *Исключение в-ли туберкулеза, чумы и сибирской язвы- Rформы: округлой или неопределенной формы, неровные края, шероховатая поверхность,
*Proteus vulgaris не дает изолированных колоний, у них H-форма роста-сплошным налетом в виде пленки из-за высокой подвижности- методика Щукевича.
*микоплазмы- яичная глазунья-требовательны, не можем культивировать
6)пигментообразования колоний – пигменты защищают от УФ лучей
Стафилококки- белый, желтый, золотистый
Красные пигменты—актиномицеты,
желтые и оранжевые – микобактерий туберкулеза, сарцины, стафилококки
зеленая – синегнойная палочка при рН 7,2-7,4
бело-голубоватый- vibro cholericae
Коричневые - bacteroidus melanogenius
Коричневая не только колония, но и вся питательная среда-Legionella pneumophilae
г) биохимический - дифф-диагностические среды, спец реактивы (установить вид)
-сахаролитические и протеолитические свойства патогенных видов
НАПРИМЕР-E.coli:
-реакция на сероводород(отриц-я) на каталазную активность(отриц-я)
-и на индол(полож-я),
-диф.диаг. среды-Гисса, Ресселя(расщепление лактозы до кислоты и газа, изменение цвета всей среды),
-по сахаралитической активности – изменение короткого пестрого ряда- E.coli ферментирует всё с образованием газа и кислоты(красные+ пузырьки), кроме сахарозы(желтая пробирка)
д)серологический (антигенная структура); (установить вид)- РА реакция агглютинации, в котором участвует целая клетка-агглютинин, полож.результат нуж-ся в подтверждении
меч.серологич – структуру АГ-ПЦР
е)по чувствительности к фагам (установить вид)-реакция фаголизиса, монофагами
ж)биологический (вирулентность) – заражение лаб животных (установить вид)
з)генетический– ПЦР, ИФА (установить вид)
5. Морфология бактерий. Основные формы, постоянные и непостоянные структуры бактериальной клетки.
Основные формы бактерий: кокковидные, палочковидные, извитые.
1) Сферические формы, или кокки- шаровидные d=до 1 мкм, которые по взаимному расположению делятся на микрококки, диплококки, стрептококки, тетракокки, сарцины и стафилококки.
Микрококки - отдельно расположенные клетки- деление в одной плоскости, расхождение клеток.
Диплококки или парные кокки, располагаются парами (пневмококк, гонококк, менингококк), так как клетки после деления не расходятся. Пневмококк (возбудитель пневмонии) имеет с противоположных сторон ланцетовидную форму, а гонококк (возбудитель гонореи) и менингококк (возбудитель эпидемического менингита) имеют форму кофейных зерен, обращенных вогнутой поверхностью друг к другу.
Стрептококки - клетки округлой или вытянутой формы, составляющие цепочку вследствие деления клеток в одной плоскости и сохранения связи между ними в месте деления.
Сарцины располагаются в виде пакетов из 8 кокков и более, так как они образуются при делении клетки в трех взаимно перпендикулярных плоскостях.
Стафилококки - кокки, расположенные в виде грозди винограда в результате деления в разных плоскостях.
2) Палочковидные бактерииразличаются по размерам, форме концов клетки и взаимному расположению клеток. Длина - до 10 мкм, толщина - до 2 мкм. Палочки могут быть правильной (кишечная палочка и др.) и неправильной булавовидной (коринебактерии) формы. К наиболее мелким палочковидным бактериям относятся риккетсии.
Концы палочек могут быть как бы обрезанными (сибиреязвенная бацилла), закругленными (кишечная палочка), заостренными (фузобактерии) или в виде утолщения как булавка (коринебактерии дифтерии).
Слегка изогнутые палочки называются вибрионами – 1 изгиб, не превышает четверть оборота (холерный вибрион).
Ветвящиеся - палочковидные бактерии, которые могут иметь разветвление в форме латинской буквы Y, встречающиеся у бифидобактерий, у актиномицетов
Большинство палочковидных бактерий располагается беспорядочно, так как после деления клетки расходятся. Если после деления клетки остаются связанными общими фрагментами клеточной стенки и не расходятся, то они располагаются под углом друг к другу (коринебактерии дифтерии) или образуют цепочку (сибиреязвенная бацилла).
3) Извитые формы- спиралевидные бактерии, которые бывают двух видов:
-Спириллы имеют вид извитых клеток с крупными завитками, большой диаметр (возбудитель содоку (болезнь укуса крыс), а также кампилобактерии и хеликобактерии) как штопор
-Спирохеты представляют тонкие длинные извитые бактерии, с более мелкими завитками до 30 шт, и характером движения. Treponema, Borrelia, Leptospira.
Постоянные структурные элементы бактерий: клеточная стенка, рибосома, цитоплазматическая мембрана, нуклеоид, мезасома.
Бактериальную клетку окружает оболочка, состоящая из клеточной стенки и цитоплазматической мембраны. Под оболочкой находится протоплазма, состоящая из цитоплазмы с включениями и наследственного аппарата - аналога ядра, называемого НУКЛЕОИДОМ. Он расположен в центральной зоне бактерий в виде двунитевой ДНК как клубок, не имеет ядерной оболочки, ядрышка и основных белков (гистонов). У большинства бактерий - одна хромосома, замкнутая в кольцо молекула ДНК. Есть внехромосомные факторы наследственности - плазмиды, представляющие собой ковалентно замкнутые кольца ДНК.
Генетические изменения могут привести к дефектам и к появлению в результате этого «шероховатых» колоний R-форм.
КЛЕТОЧНАЯ СТЕНКА - прочная, упругая структура, придающая бактерии определенную форму. Она участвует в процессе деления клетки и транспорте метаболитов, имеет рецепторы для бактериофагов, бактериоцинов и различных веществ. Наиболее толстая клеточная стенка у грам+. Толщина клеточной стенки грамм- около 15-20 нм, у грам+ 50 нм и более.
Основу клеточной стенки бактерий составляет пептидогликан.
В клеточной стенке грамм+ бактерий содержатся полисахариды, липиды-билипидный слой, белки. Основным компонентом является многослойный пептидогликан (муреин, мукопептид), составляющий 40—90% массы клеточной стенки + ковалентно связанные тейхоевые кислоты (из глицерола и рибитола), соединенных фосфатными мостиками. Форму и прочность бактериям придает жесткая волокнистая структура многослойного, с поперечными пептидными сшивками пептидогликана. Пептидогликан представлен параллельно расположенными молекулами гликана. состоящего из повторяющихся остатков N-ацетилглюкозамина и N-ацетилмурамовой кислоты, соединенных гликозидной связью. Эти связи разрывает лизоцим, являющийся ацетилмурамидазой. Гликановые молекулы соединены через N-ацетилмурамовую кислоту поперечной пептидной связью из четырех аминокислот (тетрапептида).
Способность грамм+ бактерий при окраске по Граму удерживать генциановый фиолетовый в комплексе с йодом (сине-фиолеговая окраска бактерий) связана со свойством многослойного пептидогликана взаимодействовать с красителем. Кроме этого, последующая обработка мазка бактерий спиртом вызывает суживание пор в пептидогликане и тем самым задерживает краситель в клеточной стенке.
У грамм- Пептидогликан в клеточной стенке представлен 1-2 слоями, кнаружи от которого расположен слой липопротеина, соединенный с пептидогликаном через ДАП. За ним следует наружная мембрана клеточной стенки.Тетрапептиды состоят из чередующихся L- и D-аминокислот, например: L-аланин — D-глугаминовая кислота — мезо-ди-амино-пимелиновая кислота — D-аланин. У Е. соli пептидные цепи соединены друг с другом через D-аланин одной цепи и мезо-диаминопимели новую кислоту — другой. Состав и строение пептидном части стабильны.
Грамм- бактерии после воздействия спиртом утрачивают краситель, что обусловлено меньшим количеством пептидогликана, они обесцвечиваются спиртом и при обработке фуксином или сафранином приобретают красный цвет.
ЦИТОПЛАЗМАТИЧЕСКАЯ МЕМБРАНА при электронной микроскопии представляет собой трехслойную мембрану.
Наружная мембрана представлена ЛПС, ФЛ и белками. Внутренний слой ее представлен ФЛ. Белки матрикса наружной мембраны образуют поры, через которые проходят вода и мелкие гидрофильные молекулы. Между наружной и цитоплазматической мембраной находится периплазматическое пространство, содержащая ферменты (протеазы, липазы, фосфатазы.)
ЛПС наружной мембраны состоит из трех фрагментов:
• липида А —обуславливает токсичность т.к. эндотоксин может вызвать шок. у грамм- одинакова
• ядра, или коровой части , относительно консервативной олигосахаридной структуры;
• высоковариабельной О-специфической цепи ПСХда –олигосахаридные последовательности. обусловливают серогруппу, серовар определенного штамма бактерий – О-АГ.
Есть рибосомы – немембранные органоиды , участвующие в синтезе белка, на основе мРНК.
В цитоплазме имеются различные включения в виде гранул гликогена, полисахаридов, β-оксимасляной кислоты и волютин. Они накапливаются при избытке питательных веществ в окружающей среде и выполняют роль запасных веществ для питания и энергетических потребностей. Волютин обладает сродством к основным красителям и легко выявляется с помощью специальных методов окраски (по Нейссеру) в виде метахроматических гранул.
Факультативные (непостоянные) структуры: форма (кокки, палочки, извитые), подвижность (жгутики, аксиальные нити), капсула, споры.
*Жгутики бактерий определяют подвижность бактериальной клетки (только у палочковидных). Это тонкие нити, берущие начало от цитоплазматической мембраны, длиннее клетки, толщина 12-20 нм, длина 3-15 мкм. 3 части: спиралевидные нити, крюк и базальные тельца, со стерженем со специальными дисками. Дисками жгутики прикреплены к цитоплазматической мембране и клеточной стенке.
Жгутики состоят из белка – флагеллина это- АГ - так называемый Н-антиген. Субъединицы флагеллина закручены в виде спирали.
Число жгутиков: от 1-(монотрих) у холерного вибриона, до десятка и сотен, отходящих по периметру бактерии (перитрих), у кишечной палочки, протея и др. Лофотрихи имеют пучок жгутиков на одном из концов клетки-кампилобактерии. Амфитрихи имеют по одному жгутику или пучку жгутиков на противоположных концах клетки- спириллы.
*Аксиальные нити у спирохет
*Ворсинки, или пили (фимбрии) - нитевидные образования, более тонкие и короткие, чем жгутики. Пили отходят от поверхности клетки и состоят из белка пилина. Пили общего типа отвечают за прикрепления к субстрату, питание и водно-солевой обмен. Многие пили являются рецепторами для бактериофагов.
*Споры (у семейства Bacillacia и у вирулентных и у невирулентных) во внешней среде- своеобразная форма покоящихся бактерий у грамм+ рода Bacillus, у которых размер споры не превышает диаметр клетки, называются бациллами - возбудитель Сибирской язвы Bacillus anthracis(в центре спора)
Если размер споры превышает диаметр клетки, как форма веретена, называются род клостридии: Clostridium botulinum – ботулизма(теннисные ракетки), Clostridium perfringens-газовой анаэробной инфекции(веретено), Сlostridium tetani-столбняка(палочки), и еще Cl. novyi, Cl.histolyiicum, Cl. Septicum.
Споры кислотоустойчивы, поэтому окрашиваются по методу Циля-Нельсена в красный, а вегетативная клетка - в синий цвет.
Спора долго может сохраняться из-за наличия многослойной оболочки, низкого содержания воды и вялых процессов метаболизма. В почве, например, возбудители сибирской язвы и столбняка могут сохраняться десятки лет.
*Капсула (внутри макроорганизма)– только у патогенных м/о, в основном -трехслойный полисахарид или полипептид- у сибиреязвенной бациллы. Ее функции: делает оболочку клетки (состоящей из клеточной стенки и ЦПМ) более плотной и прочной, предохраняет бактерии от воздействия бактерицидных факторов, обеспечивает адгезию на различных субстратах, может содержать запасы питательных веществ.
Классические капсулообразующие полисахаридной природы: St rep .pneumonia, Klebsiella pneumoniae, Cl . perfringens -газов.анаэроб. инфекции, Y . pestis -чумы, Bordetella pertussis-коклюша.
Капсулированные бактерии могут превращаться в бескапсульные варианты и, поскольку первые образуют мукоидные или гладкие (S), а бескапсульные — шероховатые (R) колонии, это явление известно, как S- и R-диссоциация. Капсула и слизистый слой не препятствуют поступлению и выходу различных веществ из бактериальной клетки, а также плохо удерживают красители.
Окраска капсул бактерий. Для облегчения микроскопирования капсулы можно сделать видимыми, проведя негативную окраску мазка по Бурри-Гинсу- тушь создает темный фон вокруг капсулы.
6. Основные характеристики светового микроскопа (разрешающая способность, общее увеличение). Принцип иммерсионного микроскопа.
Световой микроскоп – ϶ᴛο оптическая система, состоящая из конденсора, объектива и окуляра. Пучок света от источника освещения собирается в конденсоре, направляется на объект; пройдя через объект, лучи света попадают в систему линз объектива, они строят первичное изображение, которое увеличивается с помощью линз окуляра.
Разрешающая способность – ϶ᴛο минимальное расстояние между двумя точками, при котором они еще раздельно изображаются данной оптической системой.
Общее увеличение это произведение увеличения объектива на увеличение окуляра.
Иммерсионная микроскопия (от лат. погружение) — метод микроскопического исследования малых объектов с помощью погружения объектива светового микроскопа в среду с высоким коэффициентом преломления, расположенную между микроскопическим препаратом и объективом.
Методика: настраивается максимальное освещение, поднимая до отказа конденсор, полностью открывая диафрагму, нужно установить плоское зеркало; затем повернуть револьвер и поставить объектив с малым увеличением (х 8), опустить его на расстоянии около 0,5 см от предметного столика. Смотря в окуляр, вращать зеркало до тех пор, пока не установиться предварительное освещение.
Вращая револьвер установить иммерсионный объектив х 90 и, смотря с боку, осторожно опускать его с помощью макрометрического винта до соприкосновения с маслом. Провести окончательную фокусировку препарата микрометрическим винтом, вращая его в пределах только одного оборота. Нельзя допускать соприкосновения объектива с препаратом, т.к. это может повлечь поломку покровного стекла (свободное расстояние иммерсионного объектива до1 мм).
При микроскопировании обратить внимание на форму (кокки, палочки, извитые), цвет (сине-фиолетового- грамм+ и розового цвета грамм-, кислотоустойчивые и др.) и расположение бактерий (парами, в цепочку и др.). По окончании работы микроскоп необходимо привести в порядок: приподнять тубус микроскопа, снять препарат, вытереть чистой тряпочкой масло с объектива, поставить объектив с малым увеличением, опустить конденсор, полностью открыть диафрагму.
7. Особенности фазово-контрастной и темнопольной микроскопии.
Фазово-контрастное устройство переводит фазовые изменения световых волн, проходящих через объект в амплитудные. Фазово-контрастная микроскопия позволяет наблюдать живые объекты, которые имеют коэффициенты преломления, близкие к коэффициентам преломления среды. Как обычно происходит увеличение изображения объекта, однако прозрачные объекты видны более четко- живые прозрачные объекты становятся контрастными и видными в поле зрения.
Можно изучить форму, размеры, взаимное расположение клеток, их подвижность, размножение, прорастание спор микроорганизмов.
Спирохеты- трепонемы имеют форму спиралевидных палочек размером до 20 мкм,
Лептоспиры - тонкие спирохеты размером до 24 мкм. с изогнутыми концами, от каждого полюса клетки по одной фибрилле отходит. Число завитков 20—40
Наблюдается подвижность трихомонад, микоплазмы
Темнопольная микроскопия основана на освещении объекта косыми лучами света (эффект Тиндаля). При таком освещении лучи не попадают в объектив, поэтому поле зрения выглядит темным. Если в исследуемом препарате содержатся клетки микроорганизмов, то косые лучи отражаются от их поверхности, отклоняются от своего первоначального направления и попадают в объектив. На интенсивно черном фоне видны сияющие объекты. Такое освещение препарата достигается использованием специального темнопольного конденсора.
Можно увидеть объекты величиной сотой доли микрометра, контуры клеток, но не дает возможности рассмотреть их внутреннюю структуру.
Спирохеты- трепонемы имеют форму спиралевидных палочек размером до 20 мкм.
Лептоспиры - тонкие спирохеты размером до 24 мкм. с изогнутыми концами, от каждого полюса клетки по одной фибрилле отходит. Число завитков 20—40.
8. Основные характеристики электронного микроскопа (разрешающая способность, общее увеличение). Особенности люминесцентной микроскопии
Электронная микроскопия позволяет наблюдать объекты, размеры которых лежат за пределами разрешающей способности светового микроскопа (0,2 мкм). Электронный микроскоп применяется для изучения вирусов, бактериофагов, тонкого строения различных микроорганизмов (жгутиков, микрокапсул, цитоплазматическую мембрану бактерий), макромолекулярных структур и других субмикроскопических объектов.
Наружная мембрана бактерий имеет вид волнообразной трехслойной структуры
В-лимфоциты имеют шероховатую поверхность, на которой определяются маркеры CD 19—22 и некоторые другие.
Объект облучается пучком электронов, генерируемым специальным электронным прожектором. Полученное изображение проецируется на люминесцентный экран с помощью системы линз. Увеличение электронного микроскопа может достигать миллиона и даже более раз.
Разрешающей способность –это способность прибора отобразить раздельно два мелких максимально близко расположенных объекта. Ниже предела разрешения эти объекты будут восприниматься как один объект. Предел разрешения составляет на практике около 0,5 нм, тогда как для светового микроскопа он равен 200 нм, поскольку у электронов длина волны намного меньше, чем у видимого света.
Люминесцентная микроскопия (флюоресценция)- это такое явление, когда некоторые вещества под влиянием падающего на них света испускают лучи с другой (обычно большей) длиной волны. Кроме того, вещества, имеющие определенный цвет при обычном освещении, при освещении УФЛ приобретают совершенно иной цвет. Объект, не видимый в УФ свете, может приобрести яркий блеск после обработки его флуорохромом (акридин оранжевый, флуоресцеин, родамин и др.). В таком препарате люминесцирующие объекты светятся различным цветом в темном поле зрения. Сила их света бывает различной, но чаще всего она невелика, поэтому люминесцентную микроскопию следует проводить в затемненном помещении.
Особенность: препарат рассматривается в излучаемом им свете. Химический состав клеток и тканей влияет на качество люминесценции т.к. это гистохимическое исследование.
При первичной флуоресценции в самом объекте находятся вещества, способные флуоресцировать.
Вторичная флуоресценция – наведенная, возникает при специальной обработке объекта веществами, способными флуоресцировать.
Ее преимуществами являются:
1) цветное изображение;
2) высокая степень контрастности самосветящихся объектов на черном фоне;
3) возможность исследования как прозрачных, так и непрозрачных живых объектов;
4) возможность исследования различных жизненных процессов в динамике их развития;
5) обнаружение и установление локализации отдельных микробов и вирусов;
6) развитие тончайших методов цито- и гистохимии и экспресс-диагностика.
9. Этапы приготовления мазка для иммерсионной микроскопии.
Приготовление окрашенного препарата состоит из следующих этапов: а) приготовление мазка, б) высушивание, в) фиксация, г) окраска.
а) Обезжиренное предметное стекло и бактериологическую петлю прожигают в пламени горелки. Пробирку с изучаемой культурой держат между указательным и большим пальцами левой руки. Петлю берут правой рукой, мизинцем правой руки прижимают пробку пробирки к ладони. Если мазок готовится с жидкой питательной среды, то каплю культуры наносят петлей на предметное стекло. Если мазок делают из культуры с агара, то петлю с культурой вносят на предметное стекло и добавляют каплю физиологического раствора, в котором эмульгируют внесенный материал. Петлю обжигают в пламени горелки. Мазок должен быть тонким, равномерно растертым, округлой формы, размером 1,5-2смІ.
б) высушивание мазка производится на воздухе или для ускорения предметное стекло с мазком, обращённым кверху, можно подержать в струе теплого воздуха высоко над пламенем горелки, но не вносить в огонь.
в) после высушивания производят фиксацию (прикрепление к стеклу) препарата. Для этого стекло с мазком, обращённым кверху, медленно проводят через пламя 3-4 раза. При этом микробы погибают, приклеиваются к стеклу и не смываются при дальнейшей обработке.
г) после охлаждения стекла производится окраска препарата простым или сложным методами:
-простыми методами, когда окрашивается вся клетка и используется только один краситель (водный фуксин Пфейффера или метиленовая синька Леффлера)
-сложными методами, когда определяются клеточные структуры (методы Грама, Циля-Нильсена)
После окраски мазок промывают водой, высушивают фильтровальной бумагой и микроскопируют под иммерсией.
10. Определение подвижности бактерий методами «раздавленной» и «висячей» капли.
(Микроскопические методы) Жгутики являются органами движения бактерий, состоят из белка флагеллина. По количеству и характеру расположения жгутиков различают бактерии: монотрихи, лофотрихи, амфитрихи и перитрихи. Жгутики обладают антигенными свойствами (Н-антиген) и дают возможность бактериям перемещаться в жидкой среде.
О наличии жгутиков можно судить по характеру движения бактерий в «раздавленной» и «висящей» каплях при опущенном конденсоре и частично прикрытой диафрагме микроскопа.
Метод «раздавленной капли». Культуру в изотоническом растворе хлорида натрия наносят на предметное стекло и сверху накладывают покровное. Капля материала должна быть такой величины, чтобы она заполняла все пространство между покровным и предметным стеклом и не выступала за пределы покровного. Препарат рассматривают с иммерсионной системой и слегка опущенным конденсором.
Метод «висячей капли». Необходимо иметь предметное стекло с лупочкой. Каплю культуры наносят на покровное стекло. Сверху накладывают предметное стекло с лупочкой посредине, края которого предварительно обмазаны вазелином. Затем предметное стекло слегка прижимают к покровному, и препарат переворачивают покровным стеклом кверху. Получается герметично закрытая камера, в которой капля долго не высыхает.
Оценка результата: неподвижные микробы в препаратах «раздавленной» и «висячей» капли двигаются хаотично, подвижные – проходят с одинаковой скоростью большие пространства, иногда через все поле зрения «вращаясь» вокруг своей оси.
Способность к движению можно определять также после внесения культуры бактерий уколом в столбик полужидкого агара (подвижные виды растут по всей толще среды, неподвижные - по уколу) или посевом бактерий в водный конденсат скошенного столбика агара (подвижные виды переплывают из конденсата на поверхность среды и колонизируют её), либо определяют способность бактерий давать «феномен роения».
11.Различия в структуре грамм+ и грамм- бактерий. Протопласты, сферопласты и L-формы бактерий.
В клеточной стенке грамм+ бактерий содержатся полисахариды, липиды-билипидный слой, белки. Основным компонентом является многослойный пептидогликан (муреин, мукопептид), составляющий 40—90% массы клеточной стенки + ковалентно связанные тейхоевые кислоты (из глицерола и рибитола), соединенных фосфатными мостиками. Форму и прочность бактериям придает жесткая волокнистая структура многослойного, с поперечными пептидными сшивками пептидогликана. Пептидогликан представлен параллельно расположенными молекулами гликана. состоящего из повторяющихся остатков N-ацетилглюкозамина и N-ацетилмурамовой кислоты, соединенных гликозидной связью. Эти связи разрывает лизоцим, являющийся ацетилмурамидазой. Гликановые молекулы соединены через N-ацетилмурамовую кислоту поперечной пептидной связью из четырех аминокислот (тетрапептида).
Способность грамм+ бактерий при окраске по Граму удерживать генциановый фиолетовый в комплексе с йодом (сине-фиолеговая окраска бактерий) связана со свойством многослойного пептидогликана взаимодействовать с красителем. Кроме этого, последующая обработка мазка бактерий спиртом вызывает суживание пор в пептидогликане и тем самым задерживает краситель в клеточной стенке.
У грамм- Пептидогликан в клеточной стенке представлен 1-2 слоями, кнаружи от которого расположен слой липопротеина, соединенный с пептидогликаном через ДАП. За ним следует наружная мембрана клеточной стенки.Тетрапептиды состоят из чередующихся L- и D-аминокислот, например: L-аланин — D-глугаминовая кислота — мезо-ди-амино-пимелиновая кислота — D-аланин. У Е. соli пептидные цепи соединены друг с другом через D-аланин одной цепи и мезо-диаминопимели новую кислоту — другой. Состав и строение пептидном части стабильны.
Грамм- бактерии после воздействия спиртом утрачивают краситель, что обусловлено меньшим количеством пептидогликана, они обесцвечиваются спиртом и при обработке фуксином или сафранином приобретают красный цвет.
При нарушении синтеза клеточной стенки бактерий под влиянием лизоцима, пенициллина, защитных факторов организма и других соединений образуются клетки с измененной (часто шаровидной) формой: протопласты - бактерии, полностью лишенные клеточной стенки; сферопласты - бактерии с частично сохранившейся клеточной стенкой. После удаления ингибитора клеточной стенки такие измененные бактерии могут реверсировать, т.е. приобретать полноценную клеточную стенку и восстанавливать исходную форму.
Бактерии сферо или протопластного типа, утратившие способность к синтезу пептидогликана под влиянием антибиотиков или других факторов и способные размножаться, называются L-формами (от названия Института им. Д. Листера). L-формы могут возникать и в результате мутаций. Они представляют собой осмотически чувствительные, шаровидные, колбовидные клетки различной величины, в том числе и проходящие через бактериальные фильтры. Нестабильные L-формы при удалении фактора, приведшего к изменениям бактерий, могут реверсировать, возвращаясь в исходную бактериальную клетку. L-формы могут образовывать многие возбудители инфекционных болезней, они обладают относительно высокой жизнеспособностью и выраженной способностью к репродукции. Исключительное значение L-трансформации патогенных бактерий заключается в том, что она является частой причиной перехода острых форм заболеваний в хронические и их обострений.
12. Окраска по методу Грама. Назначение, основная краска, протрава, обесцвечивающий фактор, дополнительная краска, механизм.
Метод Грама применяется для выявления грамм+ и грамм- бактерий
Ход работы
 1.На фиксированный мазок накладывают фильтровальную бумагу, пропитанную генцианвиолетом и наносят каплю воды на 2 минуты.
1.На фиксированный мазок накладывают фильтровальную бумагу, пропитанную генцианвиолетом и наносят каплю воды на 2 минуты.
| Методические указания Генцианвиалет основная окраска. | Ориентировочные данные
|
| 2.Бумагу сбрасывают и, не промывая водой, наливают раствор Люголя на 1 минуту. | Р-р Люголя - протрава: усиливает действие осн. краски у грамм+ бактерий. Спирт– фактор обесцвечивающий. | |
| 3.Препарат обесцвечивают 3-5 каплями спирта в течении 30 секунд до прекращения отхождения фиолетовых струек краски. | ||
| 4.Промывают водой. |
Водный фуксин – дополнительная краска | |
| 5.Докрашивают водным фуксином Пфейффера в течении 1-2 минут. | ||
| 6.Промывают водой, высушивают фильтровальной бумагой и микроскопируют под иммерсией. | Грамм+бактерии (кокки) синефиолетового цвета, грамм- (палочковидные формы) розового цвета | |
Механизм: Способность грамм+ бактерий при окраске по Граму удерживать комплекс генцианвиолета с йодом связана со свойствами многослойного пептидогликана. Обработка спиртом вызывает сужение пор пептидогликана и тем самым задерживает краску.
Наоборот, грамм- бактерии после воздействия спиртом утрачивают краситель, обесцвечиваются и окрашиваются фуксином в красный цвет вследствие меньшего содержания пептидогликана, у них наиболее выражен липополисахаридный слой.
13. Окраска по Циль-Нильсону. Назначение, основная краска, протрава, обесцвечивающий фактор, дополнительная краска, механизм.
Назначение: для окраски кислотоустойчивых бактерий ( M . tuberculosis , M . leprae ).
МЕХАНИЗМ: Кислотоустойчивость связана с наличием в клеточной стенке и цитоплазме бактерий повышенного количества липидов, воска и оксикислот - миколовой кислоты. Карболовая кислота разрыхляет клеточную стенку и тем самым повышает тинкториальные свойства, высокая концентрация красителя и нагревание усиливают реакцию взаимодействия клетки с красителями. При обработке препарата серной кислотой некислотоустойчивые бактерии обесцвечиваются и окрашиваются метиленовым синим в голубой цвет.
Методика окраски:
| Ход работы | Ориентировочные данные |
| 1.На фиксированный мазок накладывают белую фильтровальную бумагу и наливают фуксин Циля. Препарат 2-3 раза подогревают, держа высоко над пламенем до появления паров и каждый раз отставляя препарат в сторону для охлаждения. | Карболовый фуксин-основная краска; прогревание – протрава. Наблюдать за появлением паров, глядя на мазок сбоку, а не сверху. |
| 2.Дают препарату остыть, бумагу сбрасывают и препарат промывают водой. | |
| 3.Препарат обесцвечивают в 5% растворе серной кислоты. | Серная кислота - обесцвечивающий фактор. |
| 4.Промывают водой. |
Синька Леффлера – доп-я краска. |
| 5.Докрашивают синькой Леффлера 3-5 минут. | |
| 6.Промывают водой, высушивают, смотрят под иммерсией. | Кислотоустойчивые бактерии рубиново – красного цвета, а остальная микрофлора – синего цвета. |
14. Окраска по способу Ожешко и Нейссера. Назначение. основная краска, протрава, обесцвечивающий фактор, дополнительная краска, механизм. Основные этапы. Механизм.
Окраска по способу Ожешки
Назначение: для выявления спор. Этапы окраски:
1) на нефиксированный мазок наносят 0,5% раствор соляной кислоты и подогревают на пламени спиртовки 2-3 минуты;
2) кислоту сливают, препарат промывают водой, высушивают и фиксируют над пламенем ;
3) окрашивают по Циль-Нильсену.
Споры бактерий окрашиваются в красный цвет, а вегетативные формы в синий
Окраска по Нейссеру
Назначение: для выявления зерен волютина у возбудителей дифтерии (С. diphtheria), у них зерна волютина распалагаются на концах палочек .ЭТАПЫ:
1) фиксированный мазок окрашивают ацетатом синьки Нейссера ( основная окраска) в течение 2-3 мин.
2) наносят раствора Люголя (протрава) на 10-30 секунд;
3) промывают препарат водой;
4)окрашивают везувином (дополнительная окраска) в теч. 0,5-1 мин.
5) промывают препарат водой, высушить и микроскопируют.
МЕХАНИЗМ: Зерна волютина представляют собой соединения, имеющие в отличие от цитоплазмы щелочную реакцию, и поэтому избирательно воспринимают ацетат синьки, окрашиваясь в темно-синий цвет. Цитоплазма клетки, обладающая кислой реакцией, воспринимает щелочной краситель везувин и окрашивается в желтый цвет
15. Актиномицеты. Таксономия. Особенности строения. Общие признаки с бактериями и грибами. Патогенные представители, вызываемые заболевания.
| Таксономия. Царство :прокариоты Отдел: скотобактерии Класс: бактерии Порядок: Actinomycetales Семейство: Actinomycetaceae Род: Actinomyces и Nocardia. Вид: A . bovis , A . israili возбудители актиномикоза и нокардиоза Nocardia asteroides, Nocardia brasitiensis - патогенные | Особенности строения : Грамм+ бактерии. -Нет капсулы, жгутиков, ворсинок. Есть включения. -Имеют вид длинных и ветвящихся несептированных нитей (длина до 600 мкм, толщина до 2 мкм). - Встречаются тонкие, прямые или слегка изогнутые палочки или кокковидные формы, они образуются при фрагментации мицелия. -В составе пептидогликана КС обнаружены сахара (галактоза, арабиноза, ксилоза), миколовые кислоты и много жирных кислот. -Размножаются спорами, поперечным делением, почкованием. Споры не обладают термоустойчивостью, но выдерживают высушивание. -Являются представителями нормальной микрофлоры организма человека. -Продуцируют антибиотики. |
| Актиномицеты — бактерии, так как: · Состоят из одной клетки · Грамм+, полиморфны · имеют нуклеоид, а не истинное ядро. · содержат в клеточной стенке пептидогликан, а не хитин и целлюлозу, которые имеют грибы; · чувствительны к бактериофагам и АБ, а не к противогрибковым препаратам; · хорошо растут в слабо щелочной среде, а грибы — в кислой. | Общие признаки с грибами: форма ветвящейся нити-гифы, которые, переплетаясь, как и плесневые грибы, образуют видимый глазом мицелий: Субстратный мицелий формируется в результате врастания клеток в питательную среду. воздушный мицелий образуется на поверхности среды. На концах воздушного мицелия актиномицеты образуют спороносцы. Размножаются как путем фрагментации мицелия, так и путем образования экзоспор (стрептомицеты) на воздушном мицелии. |
Представители актиномицетов и их роль в патологии. Для человека патогенны очень немногие виды актиномицетов ― возбудители актиномикоза и нокардиоза.
Представители рода Actinomyces — свободноживущие микроорганизмы, обитают в почве богатой перегноем, на растениях, в воде. Некоторые присутствуют в ротовой полости, зубном налете, лакунах миндалин, в слюнных железах, на слизистой оболочке ЖКТ, обнаруживаются в камнях желчевыводящих и мочевых путей.
Актиномикоз (во всех странах )-это первично-хроническая антропо-зоонозная инфекция с длительным прогрессирующим течением и возможностью рецидивов. A. Israeli -эндогенное развитие заболевания в результате перехода актиномицетов из сапрофитического состояния в паразитическое при ИДС, воспалительных заболеваниях слизистых полости рта, респираторного тракта и ЖКТ.
Возможно также экзогенное инфицирование при заносе воз-ля из окружающей среды в ротовую полость.
Инкубационный период – до нескольких лет. В месте внедрения инфекции развивается воспалительный очаг и образуется гранулема —очень плотный и почти безболезненный инфильтрат, состоящий из макрофагов и актиномицетов. Гранулема прорастает в окружающие ткани, в результате чего в процесс вовлекается кожа: она становится цианотично-багровой. Когда гранулема нагнаивается, ее центр подвергается некротическому распаду, а при вскрытии абсцесса вначале появляется флюктуация, затем образуются длительно незаживающие свищи. Из свищей выделяется гной, в к-м содержатся друзы — белые или желтые гранулы, диаметром до 2 мм. Затем происходит фиброз (рубцевание) гранулемы. В образовании нагноений играет роль вторичная, преимущественно стафилококковая, инфекция.
Для диагностики используют бактериоскопический, бактериологический, серологический и аллергологический методы. Обычно диагноз ставят бактериоскопически по обнаружению в нативном исследуемом материале друз актиномицетов, имеющих вид мелких желтоватых или серовато-белых зернышек с зеленоватым отливом. Видны сплетения тонких гиф с пигментироваными зернами, по периферии от этого клубка мицелия отходят радиально в виде лучей гифы с колбовидными утолщениями на концах. По Граму споры окрашиваются в темно-фиолетовый, мицелий — в фиолетовый, а друзы — в розовый цвет. По Цилю—Нельсону мицелий окрашивается в синий, а споры — в красный цвет.
Окончательный диагноз устанавливают на основании выделения возбудителя. Для подавления роста сопутствующей микрофлоры гной и мокроту перед посевом центрифугируют в растворе пенициллина и стрептомицина, затем отмывают изотоническим раствором NaCJ для удаления антибиотиков. Засевают на питательные среды (сахарный агар, среда Сабуро и др.) и культивируют в аэробных и анаэробных условиях. Выделяют и идентифицируют чистую культуру по общепринятой схеме.
У выделенных культур определяют способность сворачивать и пептонизировать молоко. Выделение анаэробных видов подтверждает диагноз актиномикоза.
Для серодиагностики ставят PCК с актинолизатом. НО положительные результаты могут отмечаться при раке легкого и тяжелых нагноительных процессах. Применение в качестве АГ вместо актинолизата внеклеточных белков актиномицетов повышает чувствительность РСК. Этот же АГ можно использовать и для постановки РНГА. Аллергическую пробу проводят с актинолизатом. Диагностическое значение имеют лишь положительные и резко-положительные пробы. При висцеральном актиномикозе алтергическая проба часто отрицательная.
Лечение – применение пенициллина, тетрациклина, эритромицина, клиндамицина. Специфическая профилактика не разработана. Неспецифическая профилактика – направлена на повышение иммунного статуса, важно соблюдать гигиену полости рта, своевременно лечить зубы, воспалительные заболевания миндалин и слизистых оболочек.
Нокардиозы — оппортунистические инфекции человека, вызываемые нокардиями (Nocardia asteroides, Nocardia brasitiensis)., которые характеризуются преимущественным поражением легких и подкожной клетчатки с развитием гнойно-гранулематозного воспаления.
Патогенез. Возбудитель захватывается альвеолярными макрофагами, в цитоплазме которых он сохраняет жизнеспособность, блокируя слияние фагосомы с лизосомами и ингибируя синтез лизосомальных ферментов. Персистенция возбудителя ведет к развитию воспаления с формированием множественных сливных абсцессов и гранулем.(ЛЕГОЧНАЯ ФОРМА) Воспаление органов средостения, мягких тканей грудной клетки и др.
Инфекции ПОДКОЖНОЙ клетчатки развиваются при попадании в рану возбудителя и характеризуются развитием гнойного воспаления неглубоких пустул в месте проникновения возбудителя. У иммунодефицитных лиц возможно развитие диссеминированных инфекций.
Микробиологическая диагностика. Материалом для исследования служат мокрота, гной, биоптаты тканей. Для диагностики используют бактериоскопический и бактериологический методы. Обычно диагноз ставят бактериоскопически по обнаружению в исследуемом материале несептированных гиф. Окончательный диагноз устанавливают на основании выделения возбудителя.
Лечение -применять сульфаниламиды или их комбинации с гентамииином или левомицетином. Специфическая профилактика не разработана. Неспецифическая профилактика направлена на повышение иммунного статуса
16. Спирохеты. Таксономия. Особенности строения. Общие признаки с бактериями и простейшими. Патогенные представители. Вызываемые заболевания.
| Царство :прокариоты Отдел: скотобактерии Класс: бактерии Порядок: Spirochaetales Семейство: Spirochaetaceae, Leptospiraceae -Род: Treponema Вид : T. pallidum- сифилиса , T. carateum, T. denticola, T. minutum, T. vincentii, T. scoliodontum, T. refringens - Род : Borrelia Вид : B. recurrentis- возвратоного тифа , B. burgdorferi, B. persica, B. hispanica, B. duttoni - Род : Leptospira Вид : L. interrogans- лептоспироза , L. biflexa | Спирохеты: - Грам- извитые, тонкие, обладающие активной подвижностью микроорганизмы толщиной — до 0,6 мкм, длиной до 500 мкм. -Не образуют спор, нет капсулы. -Снаружи от ЦПМ находится тонкая и эластичная КС, состоящая из пептидогликанового слоя (мало) и наружной мембраны, между которыми расположены осевые фибриллы, в совокупности называемые аксиальные нити -состоят из белка флагеллина. Ак.нити - винтообразной формы м/о придавая клеткам вращательное, сгибательное и поступательное движение. -Есть жгутики |
Спирохеты состоят из цитоплазматического цилиндра (спирально закручен вокруг пучка осевых фибрилл), покрытого ЦПМ. Фибриллы отходят от субтерминальных прикрепительных дисков, расположенных на концах клетки. Один конец фибрилл прикреплен к субтерминальному прикрепительному диску — блефаропласту, а другой конец фибрилл свободен, поэтому фибриллы направлены навстречу друг другу. При движении спирохеты образуют петли, изгибы, которые называются вторичными завитками. Истинные жгутики крепятся в ЦПМ и отходят от нее радиально, а осевые фибриллы располагаются вдоль протоплазматического цилиндра и заключены во внешнюю оболочку (наружную мембрану).
Спирохеты в жидких средах совершают движения трех типов: быстрое вращательное вокруг длинной продольной оси, сгибательное и поступательное (штопорообразное, винтообразное). Они также способны скользить по твердому субстрату. Спирохеты отличаются друг от друга размерами клеток, количеством и характером завитков, числом фибрилл.
| Общие признаки с простейшими: · образуют цисты – при неблагоприятных условиях · отсутствует клеточная стенка · есть аксиальная нить, двигаются за счет ее сокращения – несколько типов движений · особое строение тела (множество волокон, фиксированных на полюсах) · вызывают заболевания приступообразного характера · Отличаются по количеству и амплитуде завитков. · Живут и в окружающей среде и в организме | Признаки бактерий (по морфологичким и тинкториальным) · Прокариоты грамм- · Спиралевидная форма · Размножаются путем деления |
Общие признаки спирохетозов:
– генерализованный характер;
– спирохетемия;
– рецидивирующее течение, обусловленное изменением антигенной структуры либо образованием покоящихся форм (L–форм, цист);
– экзантема (сыпь на коже);
– чувствительность спирохет к бензилпенициллину.
Представители спирохет и их роль в патологии: 3 Рода: Treponema, Borrelia, Leptospira.
1) Трепонемы (род Treponema) - извитые бактерии, имеющие 8-12 мелких завитков и 3-4 фибриллы. У Вызывают сифилис (Т. pallidum) и фрамбезию (Т. pertenue).
Сифилис— антропоноз, передается разными путями: половым, котактно-бытовым (через белье, посуду, зубные щетки, бритвенные приборы, сигареты, помаду, соски, молоко кормящей матери) через поврежденные кожу и слизистые, трансплацентарным(врожденный ранний и врожденный поздний сифилис) и трансфузионным («обезглавленный сифилис», начинается со второй стадии: появления сыпи и симптомов интоксикации через 2–3 месяца после гемотрансфузии инфицированной крови).
T. pallidum неустойчива во внешней среде: погибает при высыхании биологического материала, содержащего возбудителя, мгновенно — при 1000С; чувствительна к тяжелым металлам и дезинфектантам. Однако в донорской крови сохраняет инфекционную активность в течении суток, во влажной среде и тканях трупа — в течение 3 суток. В третичном периоде сифилиса возбудитель поражает нервную систему, поэтому препараты, используемые для лечения сифилиса должны проникать через ГЭБ.
При действии неблагоприятных факторов (обычно неправильный подбор дозы АБ) возбудитель сифилиса может образовывать покоящиеся формы: L–формы (формы с дефектами КС) или цисты (локализованные в стенке сосудов, свернутые в шар спирохеты, покрытые непроницаемой муциновой оболочкой) и в таком состоянии длительно персистировать (переживать) в организме. Клинически образование покоящихся форм ассоциируется с ремиссией- только обнаружение АТ, иногда ошибочно принимаемой за реконвалесценцию, прекращение приема антимикробных препаратов в таком случае ведет к эксцистированию трепонем и к рецидиву заболевания- с выявлением АГ.
2) Боррелии (род Borrelia) - это длинные извитые бактерии, имеющие 3-8 крупных завитков и 7-20 фибрилл. Возбудители болезни Лайма - B. burgdorferi и возвратного тифа- B. R ecurrentis , а также возбудители эндемических клещевых борелиозов (В. duttonii, В. persica, В. hispanica, В. latyschewii, В. caucasica)
B. R ecurrentis проникают в организм только через поврежденные кожу и слизистые. Распространяются трансмиссивным путем. Короткий инкубационный период (неделя). Эпидемический вшивый возвратный тиф — антропоноз. Bозбудитель распространяется платяной и головной вшами, при раздавливании вшей и втирании содержащей боррелий гемолимфы, при расчесывании укуса. Боррелии с кровью заносятся в желудок, и оттуда в полость тела (гемолимфу), где размножаются в вшах.
Для боррелий характерна высокая антигенная изменчивость: каждое новое поколение отличается структурой поверхностных АГ, что обусловливает волнообразный характер лихорадки при возвратном тифе. Первый лихорадочный приступ заканчивается образованием АТ против боррелий первой генерации. Под влиянием этих АТ большая часть борелий погибает, клинически наступает ремиссия. Часть боррелий изменяет АГ-е свойства и наступает новый приступ лихорадки. Всего наблюдается 7–8 лихорадочных волн. Выздоровление наступает, когда в крови появляется спектр антител, лизирующих все варианты боррелий. Эта особенность дала название заболеванию – возвратный тиф.
Эндемический среднеазиатский клещевой возвратный тиф — трансмиссивный зооноз. (Кавказ, Средняя Азия).Возбудителями являются многие виды боррелий. Резервуаром боррелий в природных очагах являются животные: разные виды грызунов (крысы, полевки, песчанки, ежи, барсуки), а также шакалы. Переносчиком являются паразитирующие на животных аргазовые клещи рода Ornithodorus, выделяющие возбудителя со слюной и испражнениями в течение всей их жизни. В природных очагах происходит постоянная циркуляция возбудителя от грызунов к клещам и обратно.
Человек заражается при укусах клеща или попадании испражнений клеща на поврежденную кожу. На месте инокуляции возбудителя образуется папула (первичный аффект). Заболевания чаще возникают в теплое время года во время активизации жизнедеятельности клещей. Население эндемичных по клещевому возвратному тифу районов приобретает невосприимчивость к циркулирующим возбудителям в результате бытовой иммунизации. В сыворотке крови местных жителей обнаруживаются антитела к боррелиям, распространенным в этом регионе.
Боррелиоз Лайма— клещевой боррелиоз лесов умеренного климатического пояса, занимает одно из первых мест среди природно-очаговых инфекций (весна-лето). Естественные хозяева B. burgdorferi — позвоночные животные, чаще грызуны, переносчики — иксодовые клещи. У клещей возбудитель локализуется в кишечнике, в полости тела, слюнных железах и гонадах и может передаваться трансовариально.
В организм человека B. burgdorferi попадаетсо слюной клеща при укусе. На месте укуса образуется пятно — двухцветная кольцевидная эритема с темно окрашенным периферическим контуром, оно увел-ся («ползучая эритема») . При отсутствии своевременного лечения развиваются хронические формы с многосистемными поражениями: часто поражаются кожные покровы, суставы (артриты) и нервная система (могут развиваться параличи с летальным исходом).
3)Лептоспиры «водная лихорадка» (род Leptospira) - это извитые бактерии (5-8 мелких завитков), как закрученная веревка. Они имеют 2 осевые фибриллы. Концы клеток изогнуты крючком и имеют утолщения. Лептоспиры образуют вторичные завитки, в результате чего приобретают S- образную форму. Патогенным представителем лептоспир является L. interrogans. попадают в организм с водой или пищей, что сопровождается кровоизлияниями и желтухой.
Лептоспироз- острое природно-очаговое зоонозное заболевание. Больной человек выделяет возбудителя, но эпидемического значения не имеет. Резервуаром являются животные (млекопитающие, земноводные, пресмыкающиеся и птицы), которые переносят заболевание в бессимптомной форме и длительное время с мочой выделяют лептоспиры. Чаще это грызуны, КРС, свиньи, собаки. Попав в воду, почву, лептоспиры сохраняют жизнеспособность в течение 2–3 нед. В пищевых продуктах (молоко, масло, хлеб) выживают несколько дней.
Заражение человека в природных очагах происходит главным образом алиментарным путем (через контаминированные воду или пищевые продукты), а также контактно-бытовым (при купании в контаминированных водоемах, уходе за инфицированными животными, контакте с растительностью).
Лептоспиры обладают высокой инвазивной способностью, они могут проникать через неповрежденную кожу и слизистые оболочки ротовой полости, носа, глаза, ЖКТ. На месте внедрения возбудителя первичного аффекта не возникает. Затем лептоспиры проникают в кровь и разносятся в различные ткани и органы. Там происходит их размножение и поражение мышц, особенно икроножных, почек, печени, нервной системы. Различают тяжелые желтушные формы лептоспироза, ассоциированные с гепатитом и гломерулонефритом (болезнь Васильева-Вейля) и субклинические безжелтушные формы. Тяжесть заболевания зависти от реактивности макроорганизма. После перенесенного заболевания развивается длительная невосприимчивость к данному серовару лептоспир. Однако иммунитет типоспецифический, поэтому возможно повторное заражение другим сероваром лептоспир.
17. Особенности строения риккетсий. Общие признаки с бактериями и вирусами, патогенные представители. Вызываемые заболевания.
| Царство :прокариоты Отдел: скотобактерии Класс: Риккетсии Порядок: Rickettsiales Семейство: Rickettsiaceae, Ehrlichiaceae Род: Rickettsia, Orientia, Bartonella. Вид:- группа сыпного тифа (R. Typhi, R. prowazekii -эпидемический сыпной тиф,) - группа клещевых риккетсиозов (R. conorii, R. akari, R. sibirica -клещевой риккетсиоз, R. rickettsii -пятнистую лихорадку Скалистых гор, R. australis, R. japonica, R. honei) Bartonella quintana ― возбудитель волынской лихорадки, Сoxiella burnetii ― возбудитель Q-лихорадки. | Риккетсии: · Грам- палочковидные мелкие до 4 мкм бактерии. · Нуклеопротеиды при окраске по Романовскому-Гимзе представлены зернами (от 1 до 4) при этом риккетсии -красные, а инфицированные клетки – синие. · Риккетсии обладают независимым от клетки-хозяина метаболизмом, но они получают от него макроэргические соединения для размножения. · Нет капсулы, жгутиков, спор · могут иметь включения. · Обладают полиморфизмом: ü кокковидные однозернистые и палочковидные двухзернистые - при интенсивном размножении риккетсий в клетках; ü удлиненные палочки трех-четырехзернистые - при медленном размножении риккетсий; ü нитевидные многозернистые— на начальных стадиях и в фазу замедленного роста. · Размножаются простым делением, дроблением, образуя микрокапсулу. · Обитают в организме членистоногих (вши, блохи, клещи), которые являются для них хозяевами или переносчиками. Могут передаваться трансовариально. | |
| Общие признаки с вирусами: · Высокое содержание липидов и низкое – углеводов · Облигатные (абсолютные) внутриклеточные паразиты · невозможность культивирования на искусственных питат-х средах МОЖНО: в желточном мешке куриного эмбриона, в культурах клеток млекопитающих (там некоторые виды риккетсий образуют включения), реже — в организме лабораторных животных (морских свинок, белых мышей). | Общие признаки с бактериями: · Строение клеточной стенки · Наличие ДНК и РНК · Размножение бинарным делением (удваиваются только через 8-12 часов) внутри клеток хозяина | |
Риккетсии чувствительны к действию неблагоприятных физических или химических факторов, некоторых АБ. Однако в высохших фекалиях вшей риккетсии могут сохранять инфекционность 3 месяца.
1) являются облигатными внутриклеточными паразитами, что связано с особенностями энергетического обмена: они не способны синтезировать НАД («энергетические паразиты» клеток-эукариотов). Паразитируют в ретикулоэндотелиальных клетках, клетках эндотелия сосудов. Место размножения (в цитоплазме и/или ядре клеток) является видовым признаком риккетсий.
2) жизненный цикл риккетсий складывается из двух стадий: вегетативной и покоящейся (малые формы, элементарные тельца). Вегетативные формы риккетсий активно размножаются путем бинарного деления. В покоящейся стадии риккетсии имеют меньшие размеры и дополнительную оболочку.
3) ЦПМ риккетсий отличается высокой проницаемостью, что является результатом их приспособления к паразитическому образу жизни.
Представители риккетсий и их роль в патологии.
Риккетсиозы— трансмиссивные инфекции. У человека риккетсии вызывают эпидемический (вшивый) сыпной тиф (Rickettsia prowazekii), клещевой риккетсиоз (R. sibirica), пятнистую лихорадку Скалистых гор (R. rickettsii) и другие риккетсиозы.
Эпидемический вшивый сыпной тиф. Возбудитель R. prowazekii (1913)— антропоноз. Источник инфекции — человек, больной сыпным тифом или болезнью Брилля-Цинссера, который заразен с последних 2–3 дней инкубационного периода. Передача инфекции осуществляется трансмиссивно через платяных, реже — головных вшей. Вошь, насосавшись крови больного, приобретает красный цвет (кровяная имбибиция вши) и через 3–4 часа становится заразной. Теоретически вошь способна передавать инфекцию в течение своей жизни (вошь живет 40–45 дней), но практически заразительный период вши значительно короче, так как через 2 нед после инфицирования она погибает от риккетсиозной инфекции.
Риккетсии, попавшие при сосании крови в желудок, размножаются в клетках эпителия желудка или тонкой кишки вши. Пораженные клетки разрушаются, возбудитель выделяется с испражнениями вши. При самом укусе вши заражения человека не происходит, так как возбудитель в слюнных железах отсутствует. Необходимо втирание экскрементов или раздавливание кишечника вши и попадание содержимого кишечника в ранки от укусов или в расчесы и ссадины на коже. Слюна вшей вызывает жжение и зуд, при расчесывании мест укуса риккетсии поступают в организм, при этом также открываются ворота для вторичной инфекции. Описаны случаи аэрогенного заражения людей сыпным тифом при вдыхании пыли с высохшими испражнениями, содержащими риккетсий.
В организме человека риккетсии адгезируются на эндотелии сосудов, проникают в эндотелиоциты и размножаются. В течение инкубационного периода (12–14 дней) происходит накопление возбудителя. Сильнейший эндотоксин риккетсий проявляет действие при их жизни, после гибели интоксикацию не вызывает. При разрушении эндотелиоцитов риккетсии поступают в кровь и повреждают интактные эндотелиальные клетки- капилляры-, на стенках которых возникают специфические узелки-гранулемы, развиваются васкулиты. Образование тромбов приводит к нарушению микроциркуляции. Наиболее выраженные изменения капилляров происходят в ЦНС, особенно в головном мозге, что приводит к сильным головным болям. Из-за поражения сосудов кожи появляется розеолезно-петехиальная сыпь.
Болезнь Брилля-Циннсера—рецидив эпидемического сыпного тифа. При недостаточно напряженном иммунитете риккетсии в виде покоящихся малых форм могут длительно персистировать в клетках РЭС. При снижении резистентности организма носителя возможна эндогенная активация покоящихся форм: малые формы переходят в вегетативные. Присоединение в этот период переносчика-вши может способствовать распространению свежих случаев сыпного тифа.
Эндемический крысиный сыпной тиф— природно-очаговый зооноз. Резервуаром возбудителей являются крысы, переносчики — блохи, вши, клещи. Пути заражения людей: трансмиссивный, воздушно-капельный, алиментарный.
Лабораторное подтверждение риккетсиозов возможно лишь на второй неделе болезни-с появлением АТ – РИФ, РИА, ИФА. При этом обязательно должны исследоваться «парные» сыворотки, взятые в начале болезни и через 7—14 дней и позже от начала болезни.
Лечение- антибиотики тетрациклинового ряда. Препараты пролонгированного действия (доксициклин, миноциклин). хлорамфеникола.
Профилактика. Неспецифические меры профилактики риккетсиозов сводятся к уничтожению переносчиков (вшей, блох, клещей) наиболее эффективным способом (дезинсекция) или к устранению условий для контакта с ними (периодические осмотры на педикулез, на носительство клещей, ношение клещезащитной одежды и др.). Специфические меры профилактики - путем проведения вакцинаций. Разработаны живые и инактивированные вакцины против сыпного тифа, инактивированная вакцина против пятнистой лихорадки Скалистых гор.
Возбудитель пятнистой лихорадки Скалистых гор (R. ricketsii). Весна-лето в Америке. Инкубационный период 6—8 дней. Острое начало, клинические проявления обусловлены генерализованным панваскулитом с первичным нарушением функций эндотелиальных клеток кровеносной системы и последующим развитием патологических явлений за счет дисбаланса эйкозаноидов. каскада коагуляции—антикоагуляции крови и нарушениями в системе комплемента.
Для диагностики типичного заболевания характерна триада признаков: указание на укус или контакт с клещами, макуло-папулезная сыпь, захватывающая ладони и подошвы, лихорадочное состояние с высокой температурой. Первичный аффект на месте укуса клеща, как правило, не развивается. Окончательный диагноз подкрепляется серологическим обнаружением специфических антител в РСК, РНИФ и лр. Этиотропное Лечение антибиотиками широкого спектра действия (тетрациклины, доксициклин).
18. Особенности строения хламидий. Общие признаки с бактериями и вирусами, патогенные представители. Вызываемые заболевания.
| Царство :прокариоты Отдел: скотобактерии Класс: Риккетсии Порядок: Chlamydiales Семейство: Chlamydiaceae Род: Chlamydia, Chlamydophila Вид: Chlamydia trachomatis ― воз-ль трахомы, паратрахомы, лимфогранулематоза, Chlamydophila psittaci ― воз-ль орнитоза, пситтакоз, Chlamydophila pneumoniae ― воз-ль пневмонии. | - облигатные внутриклеточные кокковидные грамм- бактерии
-Полиморфные: имеют шаровидную, овоидную или палочковидную формы.
-Размеры 0,2-1,5 мкм.
-Капсул, спор, жгутиков не образуют.
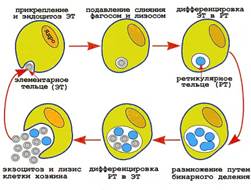
-Морфология зависит от стадии их внутриклеточного цикла развития, который характеризуется превращением небольшого шаровидного элементарного образования в крупное инициальное тельце с бинарным делением. 2 фазы в цикле развития: элементарные тельца ЭТ— внеклеточная, инфекционная форма и ретикулярные тельца РТ — внутриклеточные.
|
Элементарные тельца являются внеклеточной (покоящейся) формой – сох-ся до 3-х часов: мелкие сферические образования с толстой клеточной стенкой, окрашиваются по Романовскому-Гимзе в красный (пурпурный) цвет, метаболически неактивны, неспособны к делению, нечувствительны к антибиотикам. ЭТ попадают в клетку путем эндоцитоза. В клетке формируется вакуоль, внутри которой ЭТ увеличиваются в размерах и превращаются в РТ.
Ретикулярные тельца являются внутриклеточной (вегетативной) формой. Они крупнее ЭТ в несколько раз, имеют тонкую клеточную стенку, окрашиваются по Романовскому-Гимзе в голубой или фиолетовый цвет, метаболически активны, способны к бинарному делению, чувствительны к антибиотикам. Внутри клеток РТ делятся и затем превращаются в ЭТ, которые выходят из клеток путем экзоцитоза или лизиса клетки. Вышедшие из клетки ЭТ инфицируют другие клетки, в результате чего цикл развития хламидий повторяется.
| Общие признаки хламидий с вирусами: 1. абсолютные внутриклеточные паразиты, размножаются в цитоплазме кл. 2. имеют ограниченные метаболические возможности – «энергетические паразиты» - не способны к синтезу АТФ и НАДФ. Хламидии получают АТФ из клеток хозяина.. 3. На питательных средах хламидии не растут. Особенности культивирования – в желточном мешке куриных эмбрионов и тканевых культур. | Общие признаки хламидий с бактериями:
|
Хламидии не являются представителями нормальной микрофлоры, их обнаружение в чувствительных эпителиальных клетках (конъюнктивы, бронхов, бронхиол, легких и мочеполовой системы) хозяина всегда говорит об инфекционном процессе. Отсутствие симптомов обусловлено временным равновесием между паразитом и хозяином в условиях, ограничивающих размножение хламидий. Хламидии поглощаются периферическими моноцитами и распространяются в организме. Инфицированные моноциты оседают в тканях (в суставах, в сосудах и в области сердца) и превращаются в тканевые макрофаги, которые могут жить в течение нескольких месяцев, а находящиеся в них хламидии становятся антигенным стимулятором. Организм пытается защититься от содержащих м/ы макрофагов и инкапсулирует их. Это приводит к возникновению гранулем, которые в конечном итоге фиброматозно изменяют здоровую ткань. Периодически хламидии или их фрагменты высвобождаются из клетки и вызывают образование антител, независимо от того, определяется или нет хламидийный антиген во входных воротах инфекции. Скудность клинических симптомов при хламидиозах способствует затяжному или рецидивирующему течению инфекций, создает трудности в установлении клинического диагноза и проведении адекватной этиотропной терапии.
Хламидии способны поражать человека и животных.
C. trachomatis и C. pneumoniae — возбудители антропонозных заболеваний.
C. psittaci поражает птиц и млекопитающих, реже — вызывает респираторные инфекции у человека,
C. abortus вызывает аборты у овец и работающих с ними беременных женщин,
C. felis — конъюнктивиты у домашних кошек и человека.
Хламидийная инфекция у человека характеризуется полиморфизмом клинических проявлений и может протекать с поражением различных органов и систем: органов зрения(трахома, конъюнктивит), дыхания, мочеполовой системы, мочевыводящих и желчевыводящих путей, печени, лимфоузлов, ЦНС, суставов, сердечно-сосудистой системы . Хламидиоз часто сопровождается развитием иммунопатологических реакций и состояний.
У инфицированных C. trachomatis и C. pneumoniae инфекционный процесс имеет латентный характер. При заболеваниях, вызванных C. psittaci, наблюдается гематогенный тип распространения, поражаются различные внутренние органы (печень, селезенка, ЦНС). При венерической лимфогранулеме распространение хламидий происходит лимфогенно. C. trachomatis гематогенно и лимфагенно распространяется.
Трахома (в Африке) - хронический керато-конъюнктивит, характеризуется поражением роговицы и конъюнктивы с образованием фолликулов (трахоматозных зерен), наблюдается рубцевание конъюнктивы, хряща век и наступает слепота.
Паховый венерический лимфогранулематоз (тропика и субтропика) Цикличен: через 1,5–2 недели после заражения на месте внедрения возбудителя образуется единичный пузырек, который переходит в эрозию и язву, затем наступает генерализация процесса и развитие спаечного процесса промежности.
Урогенитальные хламидиозы у женщин—(первично-хронический) Причина воспалительных заболеваний половых путей, нарушение репродуктивной функции и здоровья новорожденного. C. trachomatis —передается половым путем, транспланцентарно, интранатально-при родах. Инкубационный период 6–14 дней. Протекают бессимптомно, инфицированные лица сохраняют хламидий длительное время. Факторы риска: молодой возраст, низкий социально-экономический статус, большое количество половых партнеров, прием оральных контрацептивов с высоким содержанием эстрогена, использование внутриматочных контрацептивов, АБ, стероидных гормонов, аборты, беременность вне брака, возраст менее 20 лет, оперативные вмешательства на гениталиях. АТ обнаруживаются у 20–40 % женщин
Урогенитальные хламидиозы у мужчин проявляются хроническими вялотекущими уретритами, осложняются болезнью Рейтера и эпидидимитом. Приводит к нарушению репродуктивной функции у мужчин, вплоть до развития вторичного бесплодия.
Болезнь Рейтера (1916) — тяжелый системный хламидиоз (уретрит + артрит + конъюнктивит), развивается в результате генерализации процесса после острой инфекции мочеполовой системы у молодых лиц с ИДС. Инкубационный период 1–2 недели. Заболевание начинается с уретрита (болезненность при мочеиспускании и проявляется лишь в изменениях мочи при лабораторном исследовании). Гематогенно разносятся по организму и поражают другие органы и системы. Через 1–2 недели — несколько месяцев появляется артрит (коленного сустава и др.). Ухудшается самочувствие больного, температура тела повышается, развивается коньюнктивит, поражение кожи на половом члене и слизистой оболочки полости рта с язвочками. На коже появляются красные пятна, которые покрываются толстой коркой, поражаются ногти (утолщение, ломкость). Болезнь плохо поддается лечению-хронич теч.
*Эндоцервицит(часто) (воспаление шейки матки) –бессимптомно или шейка может выглядеть отечной, с гипертрофической эрозией и гнойно-слизистыми выделениями из канала. Часто наблюдается картина «фолликулярного» цервицита. Резервуар половой передачи и неонатальной инфекции.
*Эндометрит: плазматические клетки, инфильтрация лейкоцитами и обнаружение C. trachomatis. Является промежуточной ступенью распространения из шейки и влагалища в маточные трубы.
*Острый сальпингит (воспаление маточных труб) является самым серьезным осложнением.
*Острый уретральный синдром характеризуется дизурией, частым мочеиспусканием, пиурией при отсутствии бактериурии. C. trachomatis.
Синдром Фитц-Хью-Куртиса — острый перигепатит, спайка между передней поверхностью печени и диафрагмой, боли в правом верхнем квадранте живота.
Влияние хламидий на репродуктивную функцию женщин – существует связь между выкидышами, бесплодиями и хламидиозами у детей (конъюнктивиты, пневмонии (воз-кап.), гастроэнтериты, Гранулярный хламидийный цистит у девочек - кон-быт ) с хламидийной инфекцией у беременных.
Орнитоз(пситтакоз) — зоонозный хламидиоз, передающийся от зараженных птиц: голубей, попугаев, канареек. Воздушно-пылевым путем при вдыхании пыли, содержащей хламидии. Обычно развивается хроническая пневмония, к-я сопровождается повышением температуры и астматическим бронхитом.
Длительное лечение хламидиозов антибиотиками, не проникающими в клетку, снижает барьерную функцию эпителия, усиливает патогенность ассоциаций кандиды-хламидии, вызывает дисбактериоз (чаще кандидозный), способствует активации уреаплазм, вызывая микст-инфекции, но инициатором воспаления являются хламидии. Поэтому урогенитальный хламидиоз часто распространяется вместе с другими заболеваниями, передаваемыми половым путем (гонореей, микоплазмозом, уреаплазмозом), что следует учитывать при диагностике и лечении. Для лечения и экстренной профилактики предпочтение отдается суммамеду (азитромицину), так как он проникает внутриклеточно.
19. Морфология и структура микоплазм, патогенные представители. Вызываемые заболевания.
| Царство: прокариоты Отдел: скотобактерии Класс: Mollycutes Порядок: Mycoplasmatales Семейство: Mycoplasmataceae Род: Mycoplasma, Ureaplasma; Acholeoplasma. Вид: Mycoplasma pneumoniae ― воз-ль пневмонии, Ureaplasma urealyticum, hominis – воз-ль урогенитальных воспалительных процессов, бесплодия, (уретриты, циститы, гломерулонефриты) Mycoplasma hominis ― усл-патог. (уретриты, пиелонефриты, простатиты, кольпиты, эндоцервициты,сальпингиты, оофориты) M. arthritidis Ревматоидный артрит | М. hominis отличается от U. urealyticum морфологией колоний, метаболизмом и чувств-тью к АБ. Микоплазма — аэробный м/о, превращающий аргинин в орнитин с освобождением аммиака. Уреаплазма — микроаэрофильный организм, превращающий мочевину в аммиак. |
• Грам- мелкие бактерии. Есть нуклеоид- с малым размером генома, рибосомы есть
• Нет клеточной стенки, нет капсулы, нет спор.
• Вместо клеточной стенки содержат 3 слоя липопротеидную ЦПМ (с стеролами- ХС)
• Образуют колонии в виде яичницы-глазуньи: гомогенный приподнятый центр и ажурные края.
• Делятся бинарным делением, почкованием, нитевидная форма может образовывать псевдомицелий (как грибы).
• Амебоидное движение, могут быть псевдоподии или жгутики (как простейшие).
• Размеры 0,15-0,3 мкм
• Полиморфны: имеют форму круглых, овальных или нитевидных, колбовидных образований при фазово-контрастной микроскопии
• Высокая чувствительностьк механическим, физическим (изменения осмотического давления, рн среды, повышение температуры, действие УФО), и химическим (действие дезинфектантов) фак-м;
• Во внешней среде микоплазмы быстро погибают, поэтому экзогенное заражение микоплазмами происходит при близком и длительном контакте воздушно-капельным или половым путем; уреаплазмами — при половом контакте; возможны эндогенные инфекции.
• Отличается от вирусов ростом в бесклеточных средах. Обладают ограниченными биосинтетическими способностями, и их приходится длительно культивировать на бесклеточных питательных изотонических и гипертонических сложных средах, обогащенных липидами, белками, предшественниками нуклеиновых кислот.
• Энергию микоплазмы получают, ферментируя углеводы или аминокислоты.
• Первичная резистентность к b–лактамным антибиотикам (пенициллинам и цефалоспоринам);
• Антигенная мимикрия: микоплазмы имеют общие АГ с антигенами клеток хозяина либо включают их в свою мембрану в результате межклеточных взаимодействий; следствием этого является развитие иммунопатологических процессов.
В инфицированных тканях микоплазмы паразитируют на мембранах эпителтальных эукариотических клеток и способны персистировать на них долгое время. Тесный контакт осуществляется с помощью особых концевых структур липопротеиновой природы. При этом липидные компоненты мембран микоплазм диффундируют в мембрану клетки, а ХС клетки макроорганизма поступает в мембрану микоплазм. Заканчивается этот процесс либо откреплением микоплазм от клетки либо поглощением их клеткой путем фагоцитоза. Фагоцитированные микоплазмы размножаются внутриклеточно, длительно персистируют в организме в составе фагоцитирующих клеток, заносятся из первичного очага в разные органы. Малотоксичные продукты обмена микоплазм оказывают неблагоприятное воздействие на мембраны пораженных клеток только в силу тесного контакта с микоплазмами; Микоплазмы стимулируют пролиферацию окружающих их клеток макроорганизма, оказывают непрямое повреждающее действие на ткани и повышают чувствительность клеток к вирусам (вирусы интенсивно размножаются именно в делящихся клетках). Поэтому нередки сочетания микоплазмоза с респираторными вирусными инфекциями.
Увеличение числа иммунодефицитных лиц, нарушение экологических взаимоотношений хозяина и его микрофлоры в результате применения антибиотиков широкого спектра действия, длительное применение гормональных контрацептивов увеличивают риск развития микоплазмозов.
Большинство микоплазм и уреаплазм являются безвредными комменсалами слизистых оболочек глаз, полости рта, дыхательных, пищеварительных и мочеполовых путей человека. Для микоплазмозов характерен клинический полиморфизм: респираторные инфекции, урогенитальные инфекции, артриты, сложные воспалительные синдромы, иммунопатологические расстройства. Микоплазмы выделены при сепсисе, абсцессе мозга, играют вспомогательную роль в патогенезе вирусного лейкоза. Возможно хроническое или латентное течение.
Респираторные инфекции, вызываемые M. pneumoniae (фарингиты, пневмонии), широко распространены во всех странах мира. Больной человек заразен во всех стадиях заболевания, начиная с инкубационного периода до 2 месяцев после перенесенного заболевания. Больше тяжело страдают дети: генерализация процесса с развитием патологических очагов в других внутренних органах. У взрослых иногда наблюдаются бессимптомные формы микоплазмоза.
Ревматоидный артрит (M. fermentes, M. artritidis, M. pneumoniae) и болезнь Рейтера (M. hominis, M. Artritidis), взаимодействующие с мембраной клеток синовиальной оболочки суставов и иммунокомпетентных клеток, оказывая на них повреждающее действие. Далее действует аутоиммунный компонент, активация реакций клеточного и гуморального иммунитета и процессы, связанные с образованием ИК.
U. urealiticum (из-за уреазной активности), вызывает острые и хронические воспалительные процессы урогенитальной сферы. Они активизируются во время беременности и могут быть причиной преждевременных родов и спонтанных абортов.
Влияние микоплазм и уреаплазм на репродуктивную функцию – спорно. Наиболее часто встречающиеся в половых путях микоплазмы (M. hominis, M. fermentans, M. primatum, M. genitalium и U. urealyticum). Часто встречаются микст-инфекции (уреплазмоз, хламидиоз, гонорея, трихомоноз). Описано также воздействие уреаплазм на сперматогенез и сперматозоиды: уреаплазмы адсорбируются на поверхности сперматозоидов, изменяют их подвижность и морфологию.
Степень колонизации связана с количеством половых партнеров, возрастом, уровнем образования и доходов, семейным положением. Инфицирование плода микоплазмами и уреаплазмами может происходить внутриуробно (через околоплодные воды восходящим путем из цервикального канала, гематогенным путем) это приводит к преждевременным родам выкидышам, мертворождениям. Воздействие микоплазм на хромосомный аппарат инфицированных клеток может приводить к аномалиям развития. А также при прохождении новорожденного через родовые пути.
У недоношенных новорожденных: поражаются органы дыхания (врожденная пневмония), нервная система, часто наблюдается гипотрофия. Колонизация влагалища и носоглотки, прямой кишки уреаплазмой отмечается у новорожденных девочек. В течение первого года жизни процент колонизации прогрессивно снижается и в препубертатном периоде встречается редко. После периода полового созревания колонизация нарастает вместе с частотой половых контактов.
При лечении микоплазмозов и уреаплазмозов следует помнить, что микоплазмы обладают естественной резистентностью к β–лактамным антибиотикам и другим лекарственным препаратам, подавляющим синтез КС (из-за ее отсутствия у возбудителя).
20. Морфология простейших их классификация патогенные представители
Простейшие – эукариотические одноклеточные микроорганизмы, составляющие подцарство Protozoa царства животных (Animalia). Простейшие включают три патогенных для человека типа (Sarcomastigophora, Apicomplexa, Ciliophora).
· Размеры простейших от 5 до 30 мкм.
· Снаружи простейшие окружены мембраной (пелликулой) – аналогом ЦПМ клеток животных.
· Некоторые имеют опорные фибриллы.
· Цитоплазма и ядро соответствуют по строению эукариотическим клеткам: цитоплазма состоит из ЭП ретикул, митохондрий, лизосом, многочисленных рибосом и др.; ядро имеет ядрышко и ядерную оболочку.
· Передвигаются простейшие посредством жгутиков, ресничек и путем образования псевдоподий.
· Простейшие могут питаться в результате фагоцитоза или образования особых структур.
· При неблагоприятных условиях образуют цисты – покоящиеся стадии, устойчивые к изменению температуры, влажности и др.
· Простейшие окрашиваются по Романовскому-Гимзе (ядро – красного, цитоплазма – синего цвета).
Тип Sarcomastigophora .
Подтип Mastigophora (жгутиконосцы) :
· трипаносому – возбудителя африканского трипаносомоза (сонная болезнь);
· лейшмании – возбудителей кожной и висцеральной форм лейшманиозов;
· трихомонады, передающиеся половым путем и паразитирующие в толстой кишке человека;
· лямблию – возбудителя лямблиоза.
Эти простейшие характеризуются наличием жгутиков: один – у лейшмании, четыре свободных жгутика и короткая ундулирующая мембрана – у трихомонад.
К подтипу Sarcodina (саркодовые) относится дизентерийная амеба – возбудитель амебной дизентерии человека. Морфологически сходна с ней непатогенная кишечная амеба. Эти простейшие передвигаются путем образования псевдоподий. Питательные вещества захватываются и погружаются в цитоплазму клеток. Половой путь размножения у амеб отсутствует. При неблагоприятных условиях они образуют цисту.
Тип Apicomplexa . В классе Sporozoa (споровики) патогенными представителями являются возбудители токсоплазмоза, кокцидиоза, саркоцистоза и малярии. Жизненный цикл возбудителей малярии характеризуется чередованием полового размножения (в организме комаров Anopheles) и бесполого (в клетках тканей и эритроцитах человека они размножаются путем множественного деления). Токсоплазмы имеют форму полулуний. Токсоплазмозом человек заражается от животных. Токсоплазмы могут передаваться через плаценту и поражать центральную нервную систему и глаза плода.
Тип Ciliophora. Патогенный представитель – возбудитель балантидиаза – поражает толстый кишечник человека. Балантидии имеют многочисленные реснички и поэтому подвижны.
21. Питание бактерий. Механизмы транспорта питательных веществ в бактериальную клетку.
Поступление питательных веществ внутрь бактериальной клетки происходит разными способами, которому способствует ряд факторов: разница в концентрации веществ, величина молекул, их растворимость в воде или липидах, рН среды, проницаемость клеточных мембран и т. д.
Различают следующие типы переноса питательных веществ из внешней среды в бактериальную клетку:
1 Пассивный перенос (по градиенту концентрации без затрат энергии):
- простая диффузия;
- облегченная диффузия.
2 Активный перенос (против градиента концентрации с затратой энергии с помощью пермеаз):
- активный транспорт;
- транслокация радикалов.
Поступив в клетку, питательные вещества вступают в биохимические реакции, в результате которых образуются как источники энергии, так и структурные компоненты клетки.
| 1. Пассивная диффузия (осмос) - это поступление питательных веществ из окружающей среды через клеточную стенку и ЦПМ в результате разницы концентраций питательных веществ в теле бактериальной клетки и в питательной среде (по градиенту концентрации). При этом концентрация вещества вне клетки выше, чем внутри клетки. Переносимое вещество не взаимодействует с компонентами клеточной мембраны. Процесс осуществляется без затрат энергии. | Внешняя среда ЦПМ Цитоплазма
Поступают газы, вода и некоторые ионы натрия. | ||||
| 2. Облегченная диффузия. – это транспорт веществ через клеточную мембрану с помощью белка-переносчика (паромщика) - транслоказы. На внутренней поверхности мембраны происходит диссоциация комплекса и транспортируемое вещество высвобождается в цитоплазму, а паромщик-пермеаза вновь принимает первоначальное положение. При этом концентрация вещества в среде превышает его концентрацию в клетке, то есть перенос осуществляется по градиенту концентрации. Процесс идет без затрат энергии. |
Перенос глицерина. | ||||
| 3. Активный транспорт - осуществляется также с помощью белков - переносчиков – пермеаз, но с затратой энергии. Энергия необходима для модификации белка-переносчика на внутренней стороне мембраны. Активный транспорт направлен против градиента концентрации и позволяет создать значительную концентрацию вещества внутри клетки при его небольшом количестве в питательной среде. Пермеаза на внешней стороне цито плазматической мембраны связывается специфически с молекулой субстрата и с помощью АТФ транспортирует ее к внутренней стороне мембраны. На внутренней поверхности мембраны пермеаза высвобождает субстрат в цитоплазму. |
Схема поступает основное количество питательных веществ в виде небольших молекул - аминокислоты, некоторые сахара, органические кислоты. | ||||
| 4. Транслокация радикалов. Сущность этого механизма состоит в переносе питательного вещества внутрь клетки против градиента концентрации с помощью пермеаз в химически измененной форме с затратой энергии АТФ. При этом в процессе переноса происходит химическая модификация переносимого вещества. |
переносятся пурины, пиримидины, некоторые сахара- крупные молекулы питательных веществ. | ||||
22. Классификация бактерий по типам питания (аутотрофы, гетеротрофы, сапрофиты, облигатные и факультативные паразиты) и источникам энергии (фототрофы и хемотрофы). Примеры.
Дата добавления: 2022-11-11; просмотров: 24; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!