Записать в тетрадь реакции гидролиза и омыления .
ХИМИЯ 10 кл.
30.03.22.
Тема урока: СЛОЖНЫЕ ЭФИРЫ, ЖИРЫ, МЫЛА.
Раздел: Органическая химия.
Цели: Получение сложных эфиров реакцией этерификации. Сложные эфиры в природе, их значение. Применение сложных эфиров на основе свойств.
Жиры как сложные эфиры. Классификация жиров. Химические свойства жиров: гидролиз и гидрирование жидких жиров. Применение жиров на основе свойств.Мыла.
Систематизировать знания о сложных эфирах, их строении, нахождении в природе и свойствах. Сформировать представление о жирах, их составе, свойствах и применении. Ознакомить с солями жиров – мылами.
Задачи:
Образовательные:
познакомить учащихся с жирами, их строением и классификацией;
изучить получение и химические свойства жиров;
познакомить с функциями жиров в организме человека;
познакомить с применением сложных эфиров и жиров.
Развивающие:
развить умения применять ИКТ;
продолжить развитие умений анализировать;
развивать логическое мышление, практические умения и
умения прогнозировать.
Воспитательные:
создание эффекта необычности для мотивации обучения;
воспитание бережного отношения к природе.
Тип урока: комбинированный урок.
Структура урока
АКТУАЛИЗАЦИЯ И МОТИВАЦИЯ ОПОРНЫХ ЗНАНИЙ
Вопрос: Какие химические соединения отвечают за запах любых ароматизаторов?
3 ЭТАП – ИЗУЧЕНИЕ НОВОГО МАТЕРИАЛА .
Сложные эфиры являются составной частью эфирных масел (известно около 3000 эф.м. – апельсиновое, лавандовое, розовое и т. д.)
|
|
|
Эфиры низших карбоновых кислот и низших одноатомных спиртов имеют приятный запах цветов, ягод и фруктов. Эфиры высших одноосновных кислот и высших одноатомных спиртов – основа природных восков. Например, пчелиный воск содержит сложный эфир пальмитиновой кислоты и мирицилового спирта (мирицилпальмитат): CH 3 ( CH 2 )14– CO – O –( CH 2 )29 CH 3
Что такое сложные эфиры?
Запись в тетради.
Сложные эфиры — это вещества, которые образуются в результате взаимодействия органических или кислородсодержащих неорганических кислот со спиртами (реакции этерификации).
Общая формула сложных эфиров одноатомных спиртов и одноосновных карбоновых кислот:
R-COO-R, где R и R1 углеводородные радикалы, исключение – эфиры муравьиной кислоты
H–COO–R1.
2. Сложные эфиры в природе. Запись в тетради.
Сложные эфиры – функциональные производные карбоновых кислот, в молекулах которых гидроксильная группа (-ОН) замещена на остаток спирта (-OR)
Сложные эфиры карбоновых кислот – соединения с общей формулой
R–COOR', где R и R' – углеводородные радикалы.
Сложные эфиры – жидкости, обладающие приятными фруктовыми запахами. В воде они растворяются очень мало, но хорошо растворимы в спиртах. Сложные эфиры очень распространены в природе. Их наличием обусловлены приятные запахи цветов и фруктов. Они даже могут находиться в коре некоторых деревьев.
|
|
|
Запах жасмина - бензилпропаноат, хризантемы – сложный эфир фенилэтилового спирта и муравьиной кислоты. Сложные эфиры, которые имеют цветочные запахи, это чаще всего производные ароматических кислот или ароматических спиртов. А вот сложные эфиры, которые входят в состав известных вам фруктов имеют довольно простой состав.
Эфиры высших одноосновных кислот и высших одноатомных спиртов – основа природных восков. Воски не растворяются в воде. Их можно формовать в нагретом состоянии. Примерами животных восков могут служить пчелиный воск, а также ворвань (спермацет), содержащийся в черепной коробке кашалота (кашалотовый воск). Пчелиный воск содержит сложный эфир пальмитиновой кислоты и мирицилового спирта (мирицилпальмитат): CH3(CH2)14–CO–O–(CH2)29CH3.
3. Физические свойства сложных эфиров. Запись в тетради.
 Физические свойства сложных эфиров:
Физические свойства сложных эфиров:
¾ Летучие, бесцветные жидкости
¾ Плохо растворимы в воде
¾ Чаще с приятным запахом
¾ Легче воды
|
|
|
4. Название сложных эфиров.

Запись в тетради.
Название сложных эфиров:
Краткие названия сложных эфиров строятся по названию радикала (R') в остатке спирта и названию группы RCOO- в остатке кислоты.
Например, этиловый эфир уксусной кислоты CH3COOC2H5 называется этилацетат.
5. Получение сложных эфиров. Демонстрация видеофрагмента:https://youtu.be/BijrJyqECXk
В пробирку налить 2 мл изоамилового (изопентилового) спирта, 2 мл уксусной кислоты и 0,5 мл концентрированной серной кислоты. Закрыть пробирку газоотводной трубкой и нагреть на водяной ба не в течение нескольких минут. После охлаждения добавить в пробирку несколько миллилитров воды. При этом, образуется слой изоамилового эфира уксус ной кислоты (изоамилацетата) с характерным запахом грушевой эссенции.
Вопросы(устно ):
¾ Как называется взаимодействие кислот со спиртами? Напишите уравнение реакции изоамилового спирта с уксусной кислотой.
¾ Для чего в реакционную смесь, содержащую спирт и карбоновую кислоту, добавляют концентрированную серную кислоту?
¾ Как вы думаете, где находят применение сложные эфиры?
¾ Как могут быть получены сложные эфиры?
Cложные эфиры могут быть получены при взаимодействии карбоновых кислот со спиртами (реакция этерификации). Катализаторами являются минеральные кислоты.
|
|
|
Записать в тетрадь реакцию этерификации.
6. Основные свойства сложных эфиров.
Обратный процесс – расщепление сложного эфира при действии воды с образованием карбоновой кислоты и спирта – называют гидролизом сложного эфира.
Гидролиз в присутствии щелочи протекает необратимо (т.к. образующийся отрицательно заряженный карбоксилат - анион RCOO– не вступает в реакцию с нуклеофильным реагентом – спиртом).
Эта реакция называется омылением сложного эфира.
Записать в тетрадь реакции гидролиза и омыления .
7. Применение сложных эфиров.
Применение сложных эфиров очень разнообразно
Их применяют в промышленности в качестве растворителей и промежуточных продуктов при синтезе различных органических соединений. Сложные эфиры с приятным запахом используют в парфюмерии и пищевой промышленности. Сложные эфиры часто служат исходными веществами в производстве многих фармацевтических препаратов.
8. Жиры, как сложные эфиры.
Важнейшими представителями сложных эфиров являются жиры.
При нагревании жиров с водой в щелочной среде французский ученый Э. Шеврель установил, что жиры расщепляются и образуются глицерин и различные карбоновые кислоты. Французский ученый М.Бертло в 1854 г. осуществил обратный процесс: при нагревании глицерина с высшими карбоновыми кислотами он получил жиры и воду.
На основании этих экспериментов сделали вывод, что
Запись в тетрадь.
Жиры – это сложные эфиры трехатомного спирта глицерина и высших карбоновых кислот, общая формула которых ?
 Жиры, как это не удивительно, относятся к сложным эфирам. В их образовании участвуют стеариновая кислота С17Н35СООН (или близкие к ней по составу и строению другие жирные кислоты) и трехатомный спирт глицерин С3Н5(ОН)3. Вот как выглядит схема молекулы такого эфира:
Жиры, как это не удивительно, относятся к сложным эфирам. В их образовании участвуют стеариновая кислота С17Н35СООН (или близкие к ней по составу и строению другие жирные кислоты) и трехатомный спирт глицерин С3Н5(ОН)3. Вот как выглядит схема молекулы такого эфира:
Н2С- О –С(О)С17Н35
|
НС- О –С(О)С17Н35
|
Н2С- О –С(О)С17Н35 тристеарин, эфир глицерина и стеариновой кислоты, тристеарат глицерина.
Жиры имеют сложное строение – это подтверждает модель молекулы тристеарата.
9. Классификация жиров.
Наиболее важные ВКК, входящие в состав жиров:
| Насыщенные кислоты | Ненасыщенные кислоты | ||
| Эмпирическая формула ВКК | Название кислоты (кислотного остатка) | Эмпирическая формула ВКК | Название кислоты (кислотного остатка) |
| С15Н31СООН | Пальмитиновая (пальмитат) | С17Н33СООН | Олеиновая (олеат) |
| С17Н35СООН | Стеариновая (стеарат) | С17Н31СООН | Линолевая (линолеат) |
| С17Н29СООН | Линоленовая | ||
10. Физические свойства жиров. https://youtu.be/Xs-N_fzqPTc
Запись в тетрадь.
По физическим свойствам жиры – твердые вещества или вязкие жидкости.
Жиры в воде не растворяются, но растворяются в органических растворителях (бензиле, бензоле, гексане...). Поэтому их можно извлечь экстракцией из измельченных семян растений или из животных продуктов этими растворителями при нагревании.
11. Основные химические свойства жиров.
https://youtu.be/P9xOj6fOnps
Переписать слайд (ХИМ. СВ.) в тетрадь.

Для жиров, содержащих остатки ненасыщенных карбоновых кислот, характерны все реакции непредельных соединений.
Наиболее важная реакция присоединения, имеющая практическое значение – это гидрирование жидких жиров. Эта реакция лежит в основе получения маргарина (твердого жира) из растительного масла.
Все жиры, как и другие сложные эфиры, подвергаются гидролизу.
Гидролиз жиров протекает и в нашем организме: когда в органы пищеварения поступают жиры, то под влиянием ферментов они гидролизуются с образованием глицерина и карбоновых кислот. Продукты гидролиза всасываются ворсинками кишечника, а затем синтезируется жир, но уже свойственный данному организму. В дальнейшем они гидролизуются и постепенно окисляются до углекислого газа и воды. При окислении жиров в организме выделяется большое количество энергии. Для людей, занятых тяжелым физическим трудом, затраченную энергию проще всего компенсировать жирной пищей. Жиры поставляют в ткани организма жирорастворимые витамины и другие биологические активные вещества.
В зависимости от условий гидролиз бывает:
¾ Водный (без катализатора, при высоких температуре и давлении).
¾ Кислотный (в присутствии кислоты в качестве катализатора).
¾ Ферментативный (происходит в живых организмах).
¾ Щелочной (под действием щелочей).
Гидролиз сложных эфиров – обратимая реакция. Для смещения равновесия в сторону продуктов реакции его проводят в щелочной среде (в присутствии щелочей или карбонатов щелочных металлов, например, карбоната натрия).
Гидролиз жиров в щелочной среде называют омылением жиров, т.к. образуются соли карбоновых кислот, которые называют мылами.
Применение жиров.
Применение жиров .
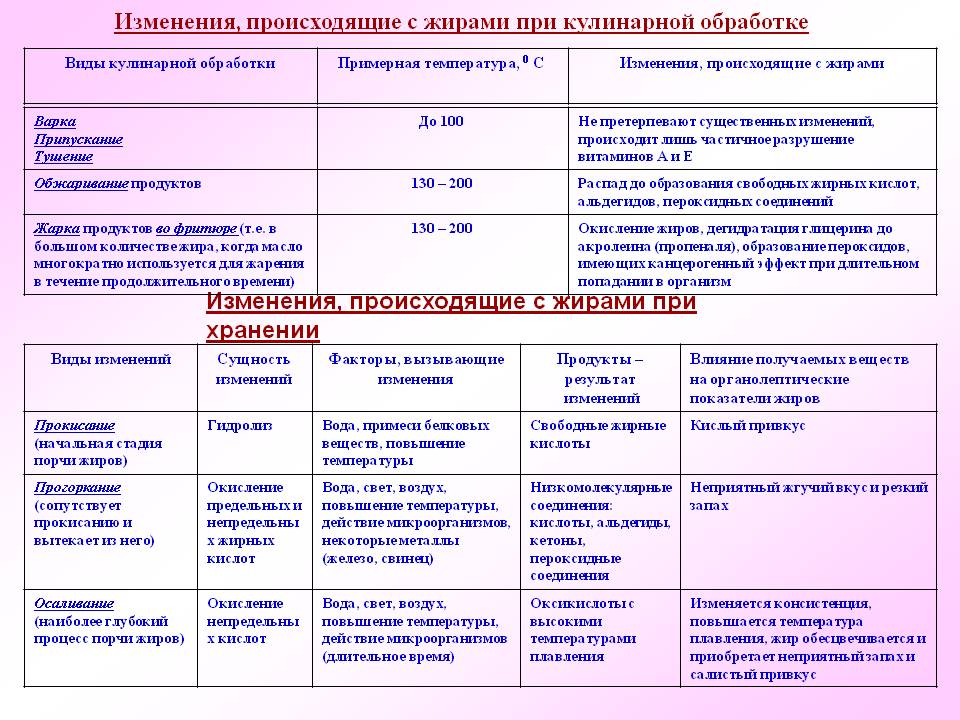
Многие жиры при стоянии на воздухе прогоркают – приобретают неприятные запах и вкус, так как при этом образуются кетоны и альдегиды. Такой процесс стимулируется железом, поэтому нельзя оставлять масло в сковороде до следующего дня. Для предотвращения его применяют антиоксиданты.
Прокисание жира связано с гидролизом его. Кислый вкус обусловлен появлением карбоновых кислот.
Весьма важными являются реакции полимеризации масел. По этому признаку растительные масла делят на высыхающие, полувысыхающие и невысыхающие. Высыхающие в тонком слое образуют блестящие тонкие пленки. На этом основано использование этих масел для приготовления лаков и красок (льняное). К полу высыхающим относятся, например, подсолнечное, а к невысыхающим относится оливковое, содержащее мало непредельных кислот.
Биологическая роль жиров.
Жиры имеют большое практическое значение и выполняют в нашем организме несколько функций:
¾ Энергетическая (при полном расщеплении 1 г жира до СО2 и Н2О освобождается 38,9 кДж энергии).
¾ Структурная (жиры – важный компонент каждой клетки).
¾ Защитная (жиры накапливаются в подкожных тканях и тканях, окружающих внутренние органы).
¾ Жиры обладают низкой теплопроводностью и предохраняют организм от переохлаждения. Поэтому северяне, употребляют много животных жиров.
14. Мыла. Запись в тетрадь .
Дата добавления: 2022-07-02; просмотров: 109; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!
