Модель атома водорода по Бору.
ФИЗИКА, ГРУППА № 36, 15.02.2022 г.
Занятие № 62
Тема: Повторение программного материала по теме «Квантовая физика».
Цель : повторение основных понятий, законов и формул квантовой физики.
План:
1. Квантовая физика.
2. Фотоэффект. Законы фотоэффекта.
3. Строение атома. Квантовые постулаты Бора.
4. Физика атомного ядра.
5. Элементарные частицы.
Теоретический материал для самостоятельного изучения
1. Квантовая физика.
Квантовая физика - раздел теоретической физики, в котором изучаются квантово-механические и квантово-полевые системы и законы их движения.
В начале 20-го века в физике произошла величайшая революция. Попытки объяснить наблюдаемые на опытах закономерности распределения энергии в спектрах теплового излучения оказались несостоятельными. Законы электромагнетизма Максвелла неожиданно «забастовали». Согласно теории Максвелла, колеблющиеся электрические заряды испускают электромагнитные волны. Тогда излучение нагретых тел может быть объяснено колебаниями электрических зарядов в молекулах вещества. При этом плотность излучаемой энергии должна увеличиваться с частотой. Однако опыт показывает, что при больших частотах плотность энергии становится малой, о чем свидетельствует характер спектра электромагнитного излучения.
Противоречия между опытом и практикой были разрешены немецким физиком Максом Планком.
|
|
|
Гипотеза Макса Планка: атомы испускают электромагнитную энергию не непрерывно, а отдельными порциями – квантами. Энергия Е каждой порции прямо пропорциональна частоте ν излучения света:
E = hν.
Коэффициент пропорциональности получил название постоянной Планка, и она равна:
h = 6,63 ∙ 10-34 Дж∙с
После открытия Планка начала развиваться самая современная и глубокая физическая теория – квантовая физика.
2. Фотоэффект. Основные законы фотоэффекта.
Фотоэффект.
Квантовым законам подчиняется поведение всех микрочастиц. Но впервые квантовые свойства материи были обнаружены именно при исследовании излучения и поглощения света.
В 1886 году немецкий физик Густав Людвиг Герц обнаружил явление электризации металлов при их освещении.
Фотоэлектрический эффект был открыт в 1887 году немецким физиком Г. Герцем и в 1888–1890 годах экспериментально исследован А. Г. Столетовым. Наиболее полное исследование явления фотоэффекта было выполнено Ф. Ленардом в 1900 г. К этому времени уже был открыт электрон (1897 г., Дж. Томсон), и стало ясно, что фотоэффект (или точнее – внешний фотоэффект) состоит в вырывании электронов из вещества под действием падающего на него света.
|
|
|
Фотоэффект — это испускание (вырывание) электронов из вещества под действием падающего на него света.
Фотоэффектом называется явление взаимодействия электромагнитного излучения с веществом, в результате которого энергия излучения передается электронам вещества.
Схема экспериментальной установки для исследования фотоэффекта изображена на рис.
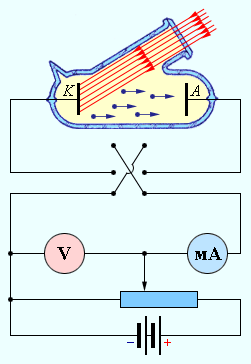
В экспериментах использовался стеклянный вакуумный баллон с двумя металлическими электродами, поверхность которых была тщательно очищена. К электродам прикладывалось некоторое напряжение U, полярность которого можно было изменять с помощью двойного ключа. Один из электродов (катод K) через кварцевое окошко освещался монохроматическим светом некоторой длины волны λ. При неизменном световом потоке снималась зависимость силы фототока I от приложенного напряжения.
На рис. ниже изображены типичные кривые такой зависимости, полученные при двух значениях интенсивности светового потока, падающего на катод.
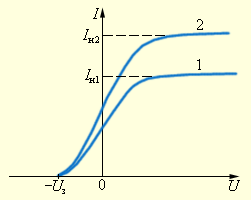
Зависимость силы фототока от приложенного напряжения. Кривая 2 соответствует большей интенсивности светового потока. Iн1 и Iн2 – токи насыщения, Uз – запирающий потенциал или задерживающее напряжение.
|
|
|
Кривые показывают, что при достаточно больших положительных напряжениях на аноде A фототок достигает насыщения, так как все электроны, вырванные светом из катода, достигают анода. Тщательные измерения показали, что ток насыщения Iн прямо пропорционален интенсивности падающего света. Когда напряжение на аноде отрицательно, электрическое поле между катодом и анодом тормозит электроны. Анода могут достичь только те электроны, кинетическая энергия которых превышает |eU|. Если напряжение на аноде меньше, чем –Uз, фототок прекращается. Измеряя Uз, можно определить максимальную кинетическую энергию фотоэлектронов:
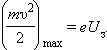
Величина Uз оказалась независящей от интенсивности падающего светового потока.
Задерживающее напряжение - минимальное обратное напряжение между анодом и катодом, при котором фототок равен нулю.
Задерживающее напряжение U3 зависит от максимальной кинетической энергии, которую имеют вырванные светом электроны.
Основные законы фотоэффекта.
Законы фотоэффекта были установлены в 1888 году профессором московского университета Александром Григорьевичем Столетовым.
Первый закон фотоэффекта Столетова звучит так: фототок насыщения пропорционален световому потоку, падающему на катод. Объясняется этот закон тем фактом, что фототок — это движение электронов, выбитых из катода в результате фотоэффекта. При нулевом напряжении выбитые электроны летят во все стороны, и некоторые достигают анода — возникает ток. При повышении напряжения все больше электронов достигают анода, ток растет, но только до тех пор, пока до анода не будут долетать все выбитые электроны.
|
|
|
Число фотоэлектронов, вырываемых светом из катода за 1 с, прямо пропорционально интенсивности света.
Второй закон фотоэффекта Столетова гласит, что кинетическая энергия фотоэлектронов не зависит от интенсивности падающего света, а зависит от его частоты и возрастает с частотой.
Если частота света меньше определенной для данного вещества минимальной частоты νmin, то фотоэффекта не происходит.
Объяснить этот закон в рамках классической электродинамики невозможно, его смогли объяснить только с разработкой квантовой теории фотоэффекта.
Объяснение фотоэффекта было дано в 1905 г. Эйнштейном, развившим идеи Планка о прерывистом испускании света. В экспериментальных законах фотоэффекта Эйнштейн увидел убедительное доказательство того, что свет имеет прерывистую структуру и поглощается отдельными порциями.
Энергия Е каждой порции излучения в полном соответствии с гипотезой Планка пропорциональна частоте:
Е = hν,
где h — постоянная Планка.
При фотоэффекте, согласно законам сохранения, часть этой энергии пойдет на то, чтобы сорвать электрон с орбиты (работа выхода A), а остаток электрон получит в виде кинетической энергии. Таким образом, получаем формулу, объясняющую второй и третий законы фотоэффекта:
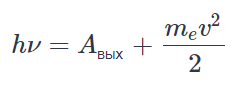
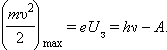
Эту формулу принято называть уравнением Эйнштейна для фотоэффекта.
Третий закон фотоэффекта.
Для каждого вещества фотоэффект наблюдается лишь в том случае, если частота ν света больше некоторого минимального значения νmin. Ведь, чтобы вырвать электрон из металла даже без сообщения ему кинетической энергии, нужно совершить работу выхода А. Следовательно, энергия кванта должна быть больше этой работы:
hν > А
Предельную частоту νmin и предельную длину волны λmах называют красной границей фотоэффекта. Они выражаются так:
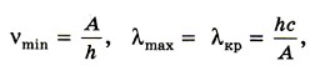
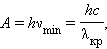
|
где c – скорость света, λкр – длина волны, соответствующая красной границе фотоэффекта. λmах(λкр) — максимальная длина волны, при которой фотоэффект еще наблюдается. Это название появилось по аналогии со световыми волнами, так как максимальная длина волны видимого света соответствует красному цвету.
3. Строение атома. Квантовые постулаты Бора.
Модель Томсона.
1896 году Хендрик Лоренц создал электронную теорию о том, что электроны являются частью атома. Эту гипотезу в 1897 году подтвердили эксперименты Джозефа Джона Томсона. Им был сформулирован вывод о том, что существуют частицы с наименьшим отрицательным зарядом - электроны и они являются частью атомов.
Электрон – наименьшая электроотрицательная заряжённая элементарная частица.
Масса покоя электрона me = 9,1·10-31кг.
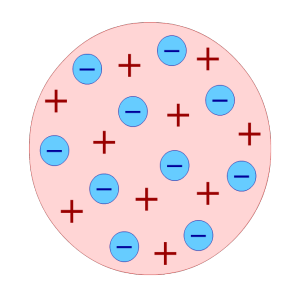
По мысли Томсона, положительный заряд занимает весь объём атома и распределён он в этом сферическом объёме равномерно. У более сложных атомов в положительно заряжённом шаре есть несколько электронов, так что атом подобен кексу, в котором роль изюма играют электроны. Распространённый термин этой модели - «Пудинг с изюмом».
Планетарная модель атома.
Резерфорд пришел к мысли о существовании атомного ядра.
Атомное ядро — тело малых размеров, в котором сконцентрирована почти вся масса и весь положительный заряд атома.
На основе своих опытов Резерфорд создал планетарную модель атома.
Опыты Резерфорда приводили к радикальным выводам и сомнениям ученых. Используя классическое представление о движении микрочастиц, он предлагает планетарную модель атома. Ее смысл заключался в том, что центр атома состоит из положительно заряженного ядра, которое является основной частью массы элементарной частицы. Атом считается нейтральным. При наличии кулоновских сил вокруг ядра по орбиталям вращаются электроны. Электроны всегда находятся в состоянии движения.
Орбиталь – область наиболее вероятного местонахождения электрона в атоме (атомная орбиталь) или в молекуле (молекулярная орбиталь).
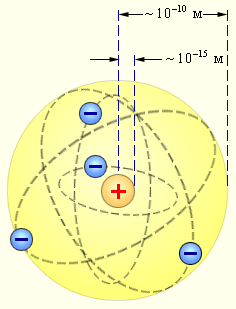
Электроны движутся вокруг ядра, подобно тому как планеты обращаются вокруг Солнца.
Такой характер движения электронов определяется действием кулоновских сил притяжения со стороны ядра.
Планетарная модель атома Резерфорда: в целом атом нейтрален, в центре атома расположено положительно заряженное ядро, в котором сосредоточена почти вся масса атома. Число внутриатомных электронов, как и заряд ядра, равны порядковому номеру элемента в периодической системе Д. И. Менделеева.
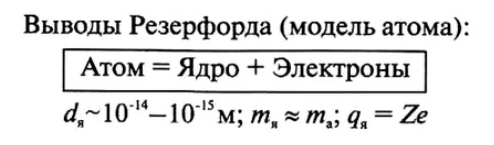
Постулаты Бора.
Первый постулат Бора (постулат стационарных состояний) гласит: атомная система может находится только в особых стационарных или квантовых состояниях, каждому из которых соответствует определенная энергия En. В стационарных состояниях атом не излучает.
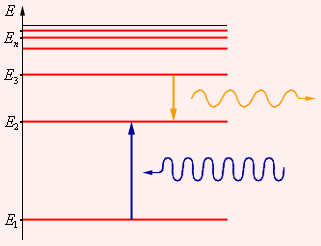
Второй постулат Бора (правило частот) формулируется следующим образом: при переходе атома из одного стационарного состояния с энергией En в другое стационарное состояние с энергией Em излучается или поглощается квант, энергия которого равна разности энергий стационарных состояний:
|
где h – постоянная Планка. Отсюда можно выразить частоту излучения:
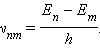
|
Модель атома водорода по Бору.
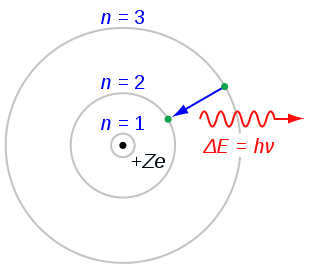
| Боровская модель водородоподобного атома (Z — заряд ядра), где отрицательно заряженный электрон заключен в атомной оболочке, окружающей малое, положительно заряженное атомное ядро. Переход электрона с орбиты на орбиту сопровождается излучением или поглощением кванта электромагнитной энергии (hν). |
Свои постулаты Н. Бор применил для построения теории строения простейшего атома (атома водорода).
Согласно этой теории Бор смог вычислить для атома водорода:
- возможные радиусы орбит электрона и размеры атома
- энергии стационарных состояний атома
- частоты излучаемых и поглощаемых электромагнитных волн.
4. Физика атомного ядра.
- Радиоактивность - явление испускания атомами невидимых проникающих излучений
- Атомы радиоактивных веществ испускают три вида излучений различной физической природы
- Альфа-лучи - поток ионов гелия;
- Бета- лучи - поток электронов;
- Гамма-лучи - поток квантов жесткого рентгеновского излучения
a - частица – ядро атома гелия. a- лучи обладают наименьшей проникающей способностью. Слой бумаги толщиной около 0,1 мм для них уже не прозрачен. Слабо отклоняются в магнитном поле.
У a- частицы на каждый из двух элементарных зарядов приходится две атомные единицы массы. Резерфорд доказал, что при радиоактивном a - распаде образуется гелий.
β - частицы представляют собой электроны, движущиеся со скоростями, очень близкими к скорости света. Они сильно отклоняются как в магнитном, так и в электрическом поле. β – лучи гораздо меньше поглощаются при прохождении через вещество. Алюминиевая пластинка полностью их задерживает только при толщине в несколько миллиметров.
g - лучи представляют собой электромагнитные волны. По своим свойствам очень сильно напоминают рентгеновские, но только их проникающая способность гораздо больше, чем у рентгеновских лучей. Не отклоняются магнитным полем. Обладают наибольшей проникающей способностью. Слой свинца толщиной в 1 см не является для них непреодолимой преградой. При прохождении g – лучей через такой слой свинца их интенсивность убывает лишь вдвое.
a – распадом называется самопроизвольный распад атомного ядра на a – частицу (ядро атома гелия) и ядро-продукт. Продукт a – распада оказывается смещенным на две клетки к началу периодической системы Менделеева.
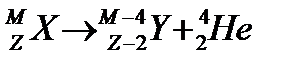
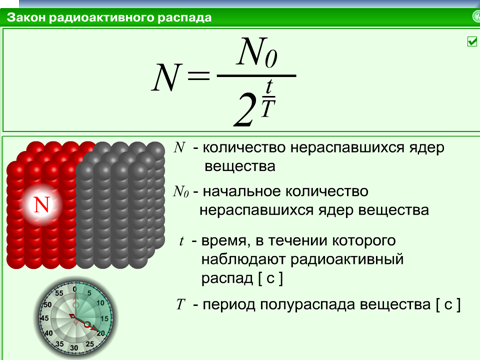
g – излучение не сопровождается изменением заряда; масса же ядра меняется ничтожно мало.

- Ядерная реакция – это процесс взаимодействия атомного ядра с другим ядром или элементарной частицей, сопровождающийся изменением состава и структуры ядра и выделением вторичных частиц или γ-квантов.
- Первая ядерная реакция была осуществлена Э. Резерфордом в 1919 году в опытах по обнаружению протонов в продуктах распада ядер

Устройство, в котором поддерживается управляемая реакция деления ядер, называется ядерным (или атомным) реактором.
5. Элементарные частицы.
Физика элементарных частиц — это в первую очередь физика реакций между этими частицами.
Элементарные частицы – материальные объекты, которые нельзя разделить на составные части. В соответствии с этим определением к элементарным частицам не могут быть отнесены молекулы, атомы и атомные ядра, которые поддаются делению на составные части – атом делится на ядро и орбитальные электроны, ядро – на нуклоны. В то же время нуклоны, состоящие из более мелких и фундаментальных частиц – кварков, нельзя разделить на эти кварки. Поэтому нуклоны относят к элементарным частицам. Учитывая то обстоятельство, что нуклон и другие адроны имеют сложную внутреннюю структуру, состоящую из более фундаментальных частиц – кварков, более целесообразно адроны называть не элементарными частицами, а просто частицами.
Частицы имеют размеры меньшие, чем атомные ядра. Размеры ядер 10 -13 − 10-12 см. Наиболее “крупные” частицы (к ним относятся и нуклоны) состоят из кварков (двух или трёх) и называются адронами. Их размеры ≈ 10-13 см. Существуют также бесструктурные (на современном уровне знаний) точечноподобные (< 10-17 см) частицы, которые называют фундаментальными. Это кварки, лептоны, фотон и некоторые другие. Всего известно несколько сот частиц. Это в подавляющем большинстве адроны.
Чем меньше масса элементарной частицы, тем больше места она занимает. Именно по этой причине электроны, которые в 2000 раз легче протона, занимают гораздо больше места по сравнению с ядром атома.
Нейтроны и протоны относятся к группе так называемых адронов (частиц, подверженных сильному взаимодействию), а если быть ещё точнее, барионов.
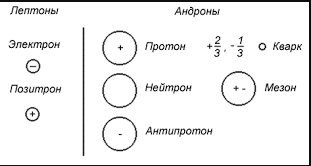
Адроны можно разделить на группы:
Барионов, которые состоят из трёх кварков
Мезонов, которые состоят из пары: частица-античастица
Фермионы и Бозон.
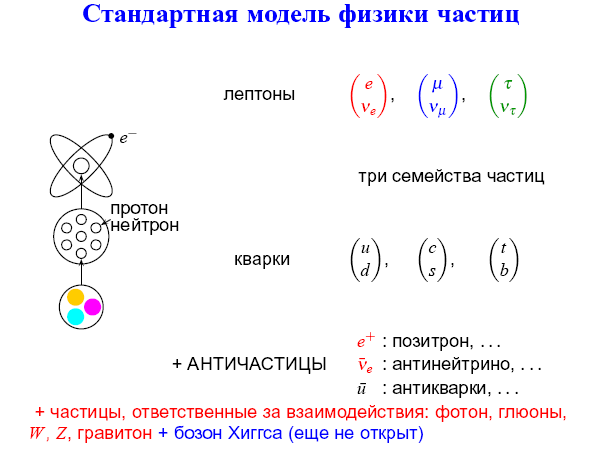
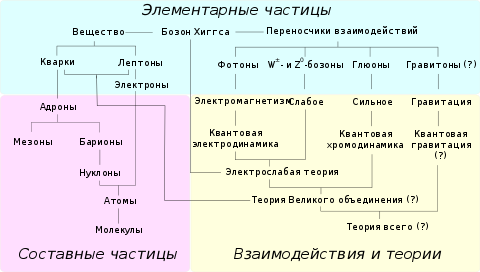
Достаточно давно учёными была придумана удобная и лаконичная форма представления элементарных частиц, названная стандартной моделью. Оказывается, все элементарные частицы делятся на фермионы, из которых и состоит вся материя, и бозоны, которые переносят различные виды взаимодействий между фермионами.
Разница между этими группами очень наглядна. Дело в том, что фермионам для выживания по законам квантового мира необходимо некоторое пространство, а для бозонов почти не важно наличие свободного места.
Основная литература по теме урока:
1) Учебник «Физика 11» Г.Я. Мякишев, Б.Б. Буховцев, В.М. Чаругин, М. «Просвещение»
2) интернет ресурсы
Домашнее задание: повторить ранее изученный материал, сделать краткий конспект.
Задание скидывать в группу
36 гр. https://vk.com/club194179937
Дата добавления: 2022-06-11; просмотров: 19; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!
