II. Решение теоретических задач.
Урок ____________
Тема: Решение задач на уравнение теплового баланса. Агрегатные (фазовые) переходы.
Цель урока:
1. Обобщить знания по теме: “Тепловые явления” на примере теоретического и практического решения задачи на тепловой баланс.
2. Проверить: знания по теме: “Тепловые явления”, умение решать задачи на тепловой баланс, навыки выполнения лабораторных опытов.
Задачи урока: Привить навыки обращения с физическими измерительными приборами.
Ход урока
I. Обобщающая беседа по теме: “Тепловые явления”.
В любой замкнутой системе соблюдается закон сохранения полной энергии. E=W+U+Q
Любые процессы, в которых изменяется внутренняя энергия, называются тепловыми. К ним относятся нагревание и охлаждение, испарение и конденсация, плавление и кристаллизация.
Количество теплоты при нагревании или охлаждении тела рассчитывается по формуле
Q= cm 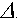 T ,
T ,
где с - удельная теплоемкость вещества, которая зависит от его свойств и находится экспериментально, m - масса, 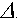 Т - изменение температуры.
Т - изменение температуры.
В процессе плавления количество теплоты, потребляемое телом, вычисляется с учетом того, что данное явление сопровождаются разрушением межмолекулярных связей. В этом случае вся энергия, полученная телом, уходит на это. Q= m 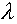 , где m - масса вещества,
, где m - масса вещества, 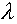 - удельная теплота плавления (кристаллизации), зависящая от свойств веществ, определяется с помощью эксперимента. Этот процесс всегда происходит при температуре плавления, и т.к. она постоянна, то
- удельная теплота плавления (кристаллизации), зависящая от свойств веществ, определяется с помощью эксперимента. Этот процесс всегда происходит при температуре плавления, и т.к. она постоянна, то 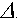 Т = 0.
Т = 0.
|
|
|
При кипении все количество теплоты, подводимое к телу, затрачивается, также как и в процессе плавления на разрыв межмолекулярных связей, но для этого требуется несколько меньшая энергия, чем при плавлении. Изменение температуры не происходит. Следовательно, и количество теплоты тоже потребуется другое.
Q = m L,
где m - масса тела,
L- удельная теплота парообразования, определяемая взаимодействием молекул в жидкости (экспериментально).
Если в системе присутствует нагреватель, работающий на топливе, то количество теплоты, выделяемое сгорающим топливом Q = mтq, где mт – масса топлива, q –удельная теплота сгорания данного топлива (определяется экспериментально).
В замкнутой теплоизолированной системе обмен энергией между телами происходит без потери тепла, т.е. теплообмен с окружающей средой не происходит. Таким образом, уравнение теплового баланса для такой системы запишется
Q = 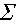 Q i ,
Q i ,
где Q - количество теплоты, выделяемое в системе,
Qi - количество теплоты, которое поглощается телами, составляющими эту систему.
Чтобы это стало более понятно, предлагаю решить несколько задач:
1. В ванну влито 80 л воды при температуре 10° С. Сколько литров воды при 100° С нужно прибавить в ванну, чтобы температура смеси была 25° С.
|
|
|
2. Какое количество теплоты потребовалось для получения дистиллированной воды объемом 5 л, если вода в дистиллятор поступила при температуре 14° С? (Потерями энергии пренебречь).
3. Сколько льда, взятого при 0° С, расплавится, если ему сообщить такое количество теплоты, которое выделится при конденсации водяного пара, масса которого равна 8 кг, а температура равна 100° С, при нормальном атмосферном давлении.
4. Сколько спирта нужно сжечь для того, чтобы нагреть 100 г воды, взятой при температуре 0° С, и испарить ее. Внешними потерями энергии пренебречь.
II. Решение теоретических задач.
Рассмотрим решение последней задачи практически и теоретически.
Задача 1:Сколько спирта нужно сжечь для того, чтобы нагреть 100 г воды, взятой при температуре 0° С, и испарить ее. Внешними потерями энергии пренебречь.
| Дано: mв =100 г = 0,1 кг; t1 = 0° С; t2 = 100° С; c = 4200 Дж/кг*°С; q = 29 МДж/кг; r = 29·106 Дж/ кг. m с - ? | Решение: Количество теплоты, выделяемое при сгорании спирта, полностью затрачивается на нагревание, плавление и испарение воды: 1. Qу = Q1 + Q2, где Qс - теплота, выделяемая при сгорании спирта, Q1 –кол-во теплоты, требуемое для нагревания воды от 0° С до температуры кипения, Q2 - кол-во теплоты, требующееся для превращения воды в пар. 2. Кол-во теплоты, выделяемое при сгорании спирта Qс = mсq 3. Кол-во теплоты, требуемое для нагревания воды Q1 = m c (t2 - t1) 4. Кол-во теплоты, требуемое для испарения воды Q2 = mпr 5. С учетом всех формул записываем уравнение теплового баланса mсq = mв cв (tкип - tпл) + mп r |
Из выражения теплового баланса можно найти массу спирта, требующуюся для данного процесса.
|
|
|
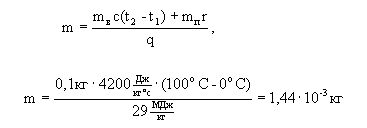
Ответ: для этого процесса потребуется сжечь примерно10 г спирта.
III. Эту же задачу предлагается решить экспериментально и сравнить результаты.
Оборудование: штатив с кольцом, лапкой и муфтами; термометр; спиртовка; спички; внутренний стакан от калориметра; весы лабораторные с разновесами; измерительный цилиндр.
Цель опыта: определить массу спирта, сгоревшего при нагревании и парообразовании воды.
Ход работы:
1. Определить массу спиртовки со спиртом до начала опыта.
2. С помощью мензурки и весов отмерить 100 г воды и влить во внутренний стакан калориметра.
3. Измерить температуру воды (убедиться, что ее температура 0 ° С).
4. Нагреть и испарить воду.
5. Определить массу спиртовки со спиртом по окончании опыта.
|
|
|
6. Найти массу сгоревшего спирта.
7. Сравнить результаты, полученные теоретически и практически, и вычислить коэффициент полезного действия данной тепловой установки.
Дано: mт = 0.1 кг; m пр - опр.эксперимент. 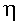 - ?
- ?
Решение:
1. КПД тепловой установки равен отношению количества теплоты, полезного (нужного для нагревания и испарения воды), и количества теплоты, затраченного (выделившегося при сгорании спирта).
2. Qп = mтq - полезное кол-во теплоты, рассчитанное теоретически.
3. Qз = mпрq - затраченное кол-во теплоты, определенное экспериментально.
4. Подставив выражения 2 и 3 в 1, получим:

Даже при максимальном уменьшении потерь тепла, КПД практически не может быть более 60%, т.к. полностью изолировать систему (вода - спирт) не удается.
В атмосфере Земли происходят подобные явления. Вы знаете, что испарение может происходить при любой температуре. Благодаря этому, осуществляется круговорот воды в природе.
Но в природе конденсация воды происходит не только непосредственно в атмосфере Земли, но и вблизи ее поверхности. Это такие явления, как роса, иней и туман
Дата добавления: 2022-06-11; просмотров: 43; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!
