ЗАДАЧИ ДЛЯ САМОСТОЯТЕЛЬНОГО РЕШЕНИЯ
Краткие теоретические сведения
Насыщенным называют пар, находящийся в динамическом равновесии со своей жидкостью. Это означает, во-первых, что число молекул, вылетающих из жидкости, равно в среднем числу молекул, возвращающихся из пара в жидкость за то же время, и, во-вторых, что насыщенный пар – это пар, имеющий наибольшую плотность при данной температуре.
Пар, давление и плотность которого меньше давления и плотности насыщенного пара при данной температуре, называют ненасыщенным.
Пар, который все время является насыщенным, не подчиняется газовым законам (Бойля-Мариотта, Гей-Люссака, Шарля), потому что при переходе из одного состояния в другое масса насыщенного пара изменяется. Масса насыщенного пара mн.п. зависит от температуры и для двух различных состояний не может иметь одинакового значения. Указанным законам подчиняется ненасыщенный пар, если его масса остается постоянной. Эти законы можно применять и к процессам перехода насыщенного пара в ненасыщенный и наоборот, если при этом масса пара не изменяется.
В каждом состоянии насыщенного пара его параметры связаны между собой уравнением Менделеева-Клапейрона.
Давление насыщенного пара с ростом температуры растет быстрее, чем давление идеального газа, так как при этом не только увеличивается скорость молекул, но и возрастает их концентрация, потому что продолжается испарение жидкости, находящейся в том же сосуде, что и пар.
|
|
|
При решении задач можно использовать справочные таблицы, в которых приводятся давление и плотность насыщенного пара при данной температуре.
Превратить ненасыщенный водяной пар, находящийся в сосуде, в насыщенный можно путем его сжатия, вставив в сосуд поршень и опуская его, или путем охлаждения. В процессе охлаждения при некоторой температуре на стенках сосуда вследствие конденсации появятся капельки воды. Это означает, что пар стал насыщенным.
Ненасыщенный пар, отделенный от жидкости, переходит в насыщенный, если его изотермически сжимать или изохорно охлаждать. В процессе изотермического сжатия ненасыщенного пара его давление и плотность возрастают до тех пор, пока пар не станет насыщенным. Дальнейшее уменьшение объема сопровождается конденсацией, давление и плотность пара остаются при этом неизменными, равными давлению и плотности насыщенного пара при данной температуре.
Температуру, при которой ненасыщенный пар становится насыщенным в результате изохорного охлаждения, называют точкой росы.
При охлаждении пара ниже точки росы начинается конденсация пара в жидкость.
Насыщенный пар можно превратить в ненасыщенный путем изотермического расширения или изохорного нагревания.
|
|
|
Согласно закону Дальтона давление воздуха, содержащего водяной пар, складывается из давления сухого воздуха рс и давления паров воды рп, т. е. атмосферное давление равно:
 .
.
Воздух, содержащий водяной пар, называют влажным. Влажный воздух или сухой можно определить, вычислив относительную влажность.
Относительной влажностью 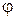 называют отношение парциального давления р водяного пара (упругости водяного пара), содержащегося в воздухе при данной температуре, к давлению
называют отношение парциального давления р водяного пара (упругости водяного пара), содержащегося в воздухе при данной температуре, к давлению  насыщенного водяного пара при той же температуре, выраженное в процентах:
насыщенного водяного пара при той же температуре, выраженное в процентах:
 . (3.1)
. (3.1)
В некоторых задачах нужно находить либо массу водяного пара, содержащегося в заданном объеме воздуха, либо массу воды, которую нужно испарить, чтобы довести влажность до некоторого требуемого значения. Относительную влажность можно определить, используя понятие абсолютной влажности.
Абсолютной влажностью ρ называется величина, равная массе водяного пара, содержащегося в 1 м3 воздуха. Иначе говоря, абсолютная влажность – это плотность водяного пара, находящегося в воздухе.
|
|
|
Относительную влажность можно определить как отношение абсолютной влажности ρ к плотности 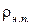 насыщенного водяного пара при данной температуре, выраженное в процентах:
насыщенного водяного пара при данной температуре, выраженное в процентах:
 . (3.2)
. (3.2)
Оба определения ((3.1) и (3.2)) эквивалентны, потому что отношение давлений равно отношению плотностей. Это легко доказать. Используя уравнение Менделеева-Клапейрона, выразим плотность идеального газа при давлении р и температуре Т:
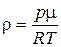 . (3.3)
. (3.3)
Считая, что водяной пар ведет себя подобно идеальному газу, на основании этой формулы получим
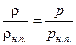 .
.
Поэтому при расчетах можно использовать как выражение (3.1), так и выражение (3.2).
Кипение – это интенсивное парообразование, которое происходит при нагревании жидкости не только с поверхности, но и внутри неё. Пузырьки пара возникают вследствие испарения жидкости внутрь мельчайших пузырьков газа, имеющихся на дне и стенках сосуда. Пузырьки газа наполняются насыщенным паром, давление которого с повышением температуры увеличивается. Когда давление внутри пузырька становится немного больше внешнего давления, которое равно сумме атмосферного и гидростатического давлений, пузырек всплывает на поверхность и лопается.
|
|
|
Давление насыщенного пара зависит от температуры. Поэтому температура кипения зависит от внешнего давления. С уменьшением внешнего давления температура кипения понижается, с увеличением – повышается. Температуры кипения различных жидкостей неодинаковы, так как давления насыщенных паров при одной и той же температуре отличаются друг от друга.
Алгоритм решения задач
Задачи на пары и влажность по своему решению принципиально почти не отличаются от задач на идеальные газы. Тем не менее, они вызывают у учащихся серьезные затруднения, связанные с неумением пользоваться уравнением газового состояния и попыткой искать решение путем логических рассуждений, что во многих случаях требует большой сообразительности. Особенно это относится к тем задачам, где вместо плотности насыщенного пара дается его давление.
Новым при решении задач на влажность является широкое использование таблиц упругости и плотности водяных паров и применение формулы относительной влажности. Из таблиц можно взять дополнительные данные к тем, которые известны по условию задачи, и составить вспомогательные уравнения, позволяющие вместе с уравнением состояния и законом Дальтона определить искомую величину.
Анализируя условие задачи, всегда полезно иметь в виду следующее. Если задана температура насыщенного пара, то его давление и плотность при этой температуре можно найти в таблицах, т. е. их можно считать известными. Если же заданы температура и давление (плотность) ненасыщенного пара, то его плотность (давление) определяется из уравнения Менделеева-Клапейрона без таблиц.
Давление насыщенных паров при температуре кипения жидкости равно атмосферному. Например, при температуре кипения воды (373 К) давление ее насыщенных паров равно нормальному атмосферному давлению (101 кПа).
Если известна температура ненасыщенного пара Т1 и точка росы Тр, то с помощью таблиц можно определить абсолютную и относительную влажность воздуха при температуре Т1, так как при температуре Тр это же количество пара будет полностью насыщать занимаемый объем. В общем случае порядок решения задач на влажность можно рекомендовать такой:
а) установить число состояний газа, рассматриваемых в условии задачи, обратив особое внимание на то, дается чистый пар жидкости или смесь пара с сухим воздухом;
б) для каждого состояния пара записать уравнение Менделеева-Клапейрона и формулу относительной влажности, если о последней что-либо сказано в условии. Составить уравнение Менделеева-Клапейрона для каждого состояния сухого воздуха (если дается смесь пара с воздухом). В тех случаях, когда при переходах из одного состояния в другое масса пара не меняется, вместо уравнения Менделеева-Клапейрона можно использовать сразу объединенный газовый закон. Вычисляя давление и плотность пара, следует всегда иметь в виду, что их значения не могут превышать значений этих величин для насыщенного пара при данной температуре.
С учетом (3.1) уравнение Менделеева-Клапейрона для пара можно записать в виде:
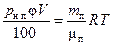 или
или  ,
,
где рн.п. – давление, которое создавал бы пар, если бы при температуре Т он был насыщенным; ρп– плотность пара;
в) записать все дополнительные условия, связывающие величины, входящие в составленные ранее уравнения и решить относительно искомой величины. Выписывая числовые значения заданных величин, нужно учесть сделанные выше замечания и использовать таблицу давления и плотности насыщенных паров при различных температурах.
Примеры решения задач
Задача 3.1. Вечером температура воздуха была t1 = 15 °С, относительная влажность φ = 80 %. Ночью температура воздуха понизилась до t2 = 8 °С. Была ли роса?
Решение. Насыщенный пар – это пар, имеющий максимальную плотность при данной температуре. Из соответствующей таблицы найдем, что при температуре 15 °С плотность насыщенного водяного пара ρн.п. 1 = 12,8 г/м3, а при 8 °С – ρн.п. 2 = 8,3 г/м3. Чтобы узнать, была ли роса, найдем плотность ρ1 водяного пара при температуре t1 и сравним ее с плотностью ρн.п. 2 насыщенного водяного пара при температуре t2. Если ρ1 < ρн.п. 2, то пар конденсироваться не будет (не будет росы). Если же ρ1 > ρн.п. 2, то роса будет, причем из каждого 1 м3 влажного воздуха сконденсируется масса пара, численно равная разности ρ1 – ρн.п. 2.
Так как относительная влажность  , то ρ1 = φ∙ρн.п. 1 / 100 % =
, то ρ1 = φ∙ρн.п. 1 / 100 % =
= 0,80·12,8 г/м3 = 10 г/м3. Сравнивая это значение с ρн.п. 2 = 8,3 г/м3, делаем вывод: роса была, причем из каждого 1 м3 воздуха сконденсировалось 1,7 г пара.
Задача 3.2 . Под колоколом насоса находится стакан, содержащий воду массой m = 0,2 кг. Насос откачивает воздух из-под колокола со скоростью и =
= 8·10– 4 м3/с. Через сколько времени вся вода испарится, если установившаяся под колоколом температура равна T = 280 К?
Решение. Если под колокол насоса поместить стакан с водой, то спустя некоторое время пространство под колоколом станет насыщенным водяными парами. При заданной температуре давление и плотность этого пара можно считать известными, поскольку их значения могут быть найдены в таблицах. Из таблицы зависимости давления насыщенного пара от температуры находим, что при 280 К давление пара  1 025 Па. Это значение определяет максимально возможное давление пара под колоколом при данной температуре.
1 025 Па. Это значение определяет максимально возможное давление пара под колоколом при данной температуре.
Когда насос начнет работать, пары из-под колокола будут удаляться, и их давление должно уменьшаться. Происходит это, однако, не сразу. Поскольку насыщенный водяной пар находится над водой, то на границе раздела пар–жидкость существует динамическое равновесие, уменьшение числа молекул пара, вызванное действием насоса, приводит к тому, что из жидкости начинает вылетать молекул больше, чем влетать в нее. Вследствие непрерывного испарения воды при работе насоса убыль молекул пара все время пополняется, в результате плотность пара, а, следовательно, и давление некоторое время почти не изменяются. Само собой разумеется, что температура пара должна при этом поддерживаться постоянной.
Как только вся вода испарится, давление под колоколом начнет падать. Процесс откачки пара из-под колокола насоса до полного испарения воды удобно схематически представить следующим образом.
В сосуде находится насыщенный водяной пар, масса которого равна массе воды в стакане и давление которого при работе насоса остается неизменным. Температура пара, а значит, и давление известны, и требуется определить время, необходимое для удаления пара из сосуда при заданной скорости откачки. Применяя к данному воображаемому состоянию насыщенного пара уравнение Менделеева-Клапейрона, можно определить объем пара, а затем и время, необходимое для его откачки, зная производительность насоса. Нетрудно заметить, что это время и будет равно искомому времени τ испарения воды под колоколом.
Предположим, водяной пар массой т при температуре Т насыщает пространство объемом V и производит давление  .
.
Тогда
 , (1)
, (1)
где µп = 1,8·10–2 кг/моль – молярная масса воды.
Если насос, откачивая пар, захватывает объем V0 за время τ0, то производительность насоса (скорость откачки) будет равна:
 , (2)
, (2)
и весь пар, находящийся в объеме V, насос откачает за время
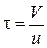 . (3)
. (3)
Это и есть время испарения всей воды.
Из уравнений (1) – (3) получим искомое время:
 ; τ ≈ 8,8 ч.
; τ ≈ 8,8 ч.
Задача 3.3 . В запаянной трубке объемом V = 0,4 л находится водяной пар под давлением рп = 8,5 кПа при температуре Тп = 423 К. Сколько росы выпадает на стенках трубки при охлаждении воды до температуры Тн.п. = 295 К? Давление насыщенных паров воды при температуре 295 К равно рн.п. = 2,6 кПа.
Решение. В задаче рассматривают два состояния пара в запаянной трубке – до и после охлаждения. В первом состоянии при 423 К пар был ненасыщенным (это вполне очевидно, так как даже при 373 К рн.п. = 101 кПа), поэтому при его изохорном охлаждении, начиная с некоторой температуры (точки росы), пар станет насыщенным и дальнейшее понижение температуры до 295 К вызовет его частичную конденсацию.
Происходит ли конденсация пара при изохорном понижении температуры от значения Т1 до Т2, если об этом не сказано в условии задачи, можно установить самим, зная плотность или давление пара. С помощью таблиц нужно только определить, будет ли точка росы Тр > Т2 или нет. В нашем примере это неравенство имеет место, следовательно, пар конденсируется.
Чтобы определить массу росы, выпавшей на стенках трубки, необходимо найти массу пара при каждой из заданных температур и вычесть из первого результата второй. Для нахождения масс удобно воспользоваться уравнением Менделеева-Клапейрона, составив его для каждого из двух состояний пара.
Обозначим параметры состояния пара до его охлаждения через рп, V, Тп и будем считать, что его масса равна тп. Тогда
 , (1)
, (1)
где  = 1,8·10–2 кг/моль – молярная масса воды.
= 1,8·10–2 кг/моль – молярная масса воды.
После охлаждения и конденсации, когда пар в трубке будет насыщенным, его масса станет равной mн.п., а параметры примут значения рн.п., V и Tн.п.. Для насыщенного пара
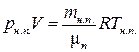 . (2)
. (2)
При составлении этого уравнения мы не учитывали объем, занимаемый каплями воды.
Для определения массы росы, выпавшей на стенках трубки, составляем вспомогательное уравнение:
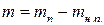 , (3)
, (3)
где m – искомая масса росы.
Решая уравнения (1) – (3) совместно и проводя вычисления, находим:
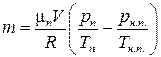 ; m ≈ 9,8 мг.
; m ≈ 9,8 мг.
Задача 3.4 . В комнате объемом V =150 м3 поддерживается температура Т1= 293 К, а точка росы равна Т2 = 283 К. Определите относительную влажность воздуха и количество водяных паров, содержащихся в комнате.
Решение. Если воздух в комнате содержит некоторое количество водяных паров, то при понижении температуры до точки росы эти пары становятся насыщенными. В тех случаях, когда задана точка росы, как, например, в этой задаче, можно рассмотреть два состояния пара в комнате: при данной температуре Т1 и температуре росы Т2. Каждое из этих состояний описывается уравнением Менделеева-Клапейрона и формулой относительной влажности. Давление насыщенных паров можно считать при этом известным, так как известна его температура (точка росы). Из таблиц зависимости давления насыщенного пара воды от температуры мы находим, что при 283 К оно равно р2н.п. = 1 225 Па, а при 293 К оно равно р1н.п. = 2 328 Па.
Допустим, что пар, находящийся в комнате объемом V, при температуре Т1 создает давление p1 и имеет массу тп; тогда
 , (1)
, (1)
где 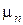 = 1,8·10–2 кг/моль – молярная масса воды.
= 1,8·10–2 кг/моль – молярная масса воды.
Если при этой температуре давление насыщенных паров равно р1н.п., то относительная влажность воздуха в комнате
 , (2)
, (2)
поскольку истинное давление паров в комнате р1. В случае понижения температуры до Т2 (точки росы) пар в комнате стал бы насыщенным и его давление было бы равно р2н.п.. Для этого состояния пара можно записать:
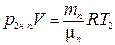 , (3)
, (3)
так как масса пара в комнате остается неизменной.
В уравнениях (1) – (3) содержатся три неизвестные величины – φ, тп, которые требуется определить, и давление p1. Решая уравнения совместно относительно искомых неизвестных, получим:
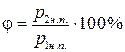 ;
;  ;
; 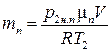 ;
;  .
.
Благоприятная для здоровья человека влажность – 40–60 %, т. е. при нормальной влажности в комнате объемом 150 м3 находится приблизительно 1,5 л воды.
Задача 3.5 . Влажный воздух объемом 1 м3 при относительной влажности φ = 60 %, температуре Т = 293 К и нормальном атмосферном давлении имеет массу m = 1,2004 кг. Определить давление насыщенного водяного пара при температуре Т.
Решение. Влажный воздух представляет смесь сухого воздуха и водяного пара. В условии задачи даны величины, характеризующие эту смесь в целом, и требуется определить параметр одного из газов, входящих в смесь, – давление насыщенного пара.
Для решения задачи нужно рассмотреть каждую компоненту газа в отдельности, составив для каждого из них уравнение состояния. Кроме того, необходимо учесть, что масса т и давление влажного воздуха р складываются соответственно из масс и давлений сухого воздуха и пара:
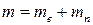 ; (1)
; (1)
 . (2)
. (2)
Рассмотрим сначала воздух без пара. Обозначим параметры состояния воздуха в заданном объеме через рв, V, Т, тогда
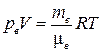 , (3)
, (3)
где 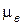 = 2,9·10–2 кг/моль – молярная масса сухого воздуха.
= 2,9·10–2 кг/моль – молярная масса сухого воздуха.
Пар, находящийся в этом же пространстве, имеет давление pп, объем V и температуру Т. Для него
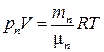 , (4)
, (4)
и, кроме того, нам дано:
 , (5)
, (5)
где рн.п. – искомое давление насыщенных паров при температуре Т.
Из уравнений (1) – (5) находим:
 ;
; 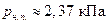 .
.
Задача 3.6 . В сосуде находится воздух, температура которого Т1 = 283 К и влажность φ1 = 60 %. Как изменится влажность воздуха и его давление, если воздух нагреть до температуры Т2 = 373 К и в три раза уменьшить объем? Начальное давление сухого воздуха p1 = 38,5 кПа, давление насыщенных паров воды при 283 К равно р1н = 1,2 кПа.
Решение. Нам даны два состояния смеси сухого воздуха с паром при разных температурах. Как видно из условия задачи, в процессе нагревания сосуда меняются все три параметра состояния и воздуха, и пара. Чтобы выбрать исходные уравнения для решения задачи, надо, прежде всего, установить, изменяется ли масса пара при его переходе во второе состояние или нет. Сделать это можно следующим образом. С помощью объединенного газового закона надо найти давление р2п пара при температуре Т2 = 373 К и сравнить его с давлением насыщенного пара при этой температуре, равным нормальному атмосферному давлению р2н = 101 кПа. Так как большего давления, чем р2н, пар при данной температуре иметь не может, то, если окажется, что р2п > р2н, это бyдeт означать, что происходила конденсация, если же р2п ≤ р2н, то при переходе во второе состояние масса пара не менялась – его недостаточно, чтобы создать давление р2н. Расчет показывает (предлагаем его сделать читателям), что в нашем примере
р2п < р2н, т. е. пар не конденсируется, и, следовательно, к параметрам пара применимо уравнение объединенного газового закона, так как масса газа остается одной и той же.
Допустим, что в начальном состоянии при температуре Т1 пар, находящийся во влажном воздухе, имел давление р1п и объем V1, а после нагревания сосуда до температуры Т2 эти параметры стали равными р2п и V2. Тогда согласно объединенному газовому закону должно быть:
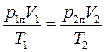 . (1)
. (1)
Относительная влажность воздуха до нагревания была равна:
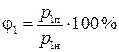 , (2)
, (2)
после нагревания она станет равной:
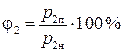 . (3)
. (3)
Ее изменение
 . (4)
. (4)
Под p1н и р2н здесь подразумевается давление насыщенного пара при температурах T1 и Т2.
Совместное решение уравнений (1) – (4) относительно ∆φ при условии, что 3V2 = V1, дает:
 ;
; 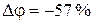 .
.
Знак «минус» обозначает, что φ2 < φ1, т. е. во втором состоянии относительная влажность воздуха уменьшилась.
Изменение ∆р полного давления влажного воздуха равно сумме изменений давлений сухого воздуха и пара:
 . (5)
. (5)
Так как масса воздуха не изменялась и воздух занимает тот же объем, что и пар, то для него должно быть
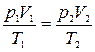 , (6)
, (6)
где р2 – давление сухого воздуха после нагревания сосуда.
Решая совместно уравнения (1), (2), (5) и (6) относительно искомого изменения давления ∆р, получим:
 ;
;  .
.
ЗАДАЧИ ДЛЯ САМОСТОЯТЕЛЬНОГО РЕШЕНИЯ
3.8. В 4 м3 воздуха при температуре 16 °С находится 40 г водяного пара. Найти относительную влажность.
3.11. Относительная влажность в комнате при температуре 16 °С составляет 65 %. Как изменится она при понижении температуры воздуха на 4 К, если парциальное давление водяного пара останется прежним?
3.13. Как изменится разность показаний сухого и влажного термометров психрометра при понижении температуры воздуха, если абсолютная влажность не изменяется? Объясните.
3.17. Относительная влажность воздуха при t1 = 30 °С равна φ1 = 80 %. Какова будет относительная влажность φ2, если этот воздух нагреть при постоянном объеме до t2 = 50 °С? Давление насыщенных паров воды при 30 °С р1 =
= 31,8 мм рт. ст., при 50 °С р2 = 92,5 мм рт. ст.
3.18. В сосуде объемом V = 100 л при температуре t = 27 °C находится воздух с относительной влажностью φ1 = 30 %. Какова станет относительная влажность φ2, если в сосуд внесли m = 1 г воды? Давление насыщенных паров воды при 27 °С р0 = 26,7 мм рт. ст.
ОТВЕТЫ
3.8. 74 %.
3.11. Увеличится на 19 %.
3.13. Уменьшится.
3.17. ≈ 29 %.
3.18. 70 %.
ТАБЛИЦЫ
Плотность жидкостей
| Вещество | кг/м3 | Вещество | кг/м3 | Вещество | кг/м3 |
| Ацетон Бензин Бензол Вода Вода морская | 780 710 880 1000 1030 | Глицерин Касторовое масло Керосин Масло машинное Нефть | 1260 960 800 900 800 | Ртуть Серная кислота Спирт Эфир | 13600 1800 790 720 |
Плотность газов при нормальных условиях (при 0 ºС и давлении 101 кПа)
| Вещество | кг/м3 | Вещество | кг/м3 | Вещество | кг/м3 |
| Азот Аммиак Водород Воздух | 1,25 0,77 0,09 1,293 | Гелий Кислород Метан | 0,18 1,43 0,72 | Природный газ Углекислый газ Хлор | 0,80 1,98 3,21 |
Тепловые свойства веществ
Твердые тела
| Вещество | Удельная теплоемкость, кДж/(кг∙К) | Температура плавления, °С | Удельная теплота плавления, кДж/кг | Температурный коэффициент линейного расширения, 10–5, К–1 |
| Алюминий | 0,88 | 660 | 380 | 2,3 |
| Железо | 0,5 | 1530 | 272 | 1,2 |
| Латунь | 0,39 | 900 | – | 1,9 |
| Лед | 2,1 | 0 | 330 | – |
| Медь | 0,38 | 1083 | 180 | 1,7 |
| Олово | 0,23 | 232 | 59 | 2,7 |
| Платина | 0,12 | 1770 | 113 | 0,89 |
| Пробка | 2,05 | – | – | – |
| Свинец | 0,13 | 327 | 25 | 2,9 |
| Серебро | 0,23 | 960 | 87 | 1,9 |
| Сталь | 0,46 | 1400 | 82 | 1,2 |
| Цинк | 0,39 | 420 | 117 | 2,9 |
Жидкости
| Вещество | Удельная теплоемкость, кДж/(кг∙К) | Температура кипения1, °С | Удельная теплота парообразования1, МДж/кг |
| Вода | 4,2 | 100 | 2,26 |
| Керосин | 2,1 | – | – |
| Ртуть | 0,12 | 357 | 0,29 |
| Спирт | 2,4 | 78 | 0,85 |
Газы
| Вещество | Удельная теплоемкость2, кДж/(кг∙К) | Температура конденсации1, °С |
| Азот | 1,05 | –196 |
| Водород | 14,3 | –253 |
| Воздух | 1,01 | – |
| Гелий | 5,29 | –269 |
| Кислород | 0,913 | –183 |
1 При нормальном давлении
2 При постоянном давлении
Дата добавления: 2022-06-11; просмотров: 224; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!
