V .Окисление многоатомных спиртов.
МНОГОАТОМНЫЕ СПИРТЫ.


Общая формула ряда гликолей СnН2n(ОН)2.
Этиленгликоль очень токсичен! Это сильный яд! Этиленгликоль вызывает длительное угрожающее жизни угнетение центральной нервной системы и поражение почек. Продуктами его превращения в организме являются щавелевая кислота и другие не менее ядовитые соединения. Он имеет спиртовой запах, в связи, с чем может быть принят за этиловый спирт и стать причиной тяжелых отравлений.

Получение этиленгликоля:
1. Щелочной гидролиз дигалогеналканов
При обработке дигалогенопроизводных углеводородов водным раствором щелочи также можно получить гликоли (лабораторный):

Реакция Вагнера-
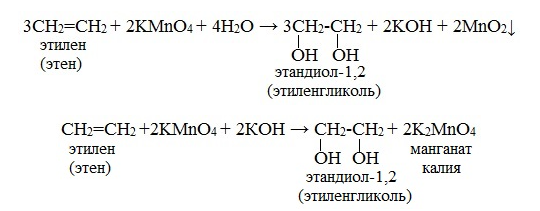
3. Промышленный способ. 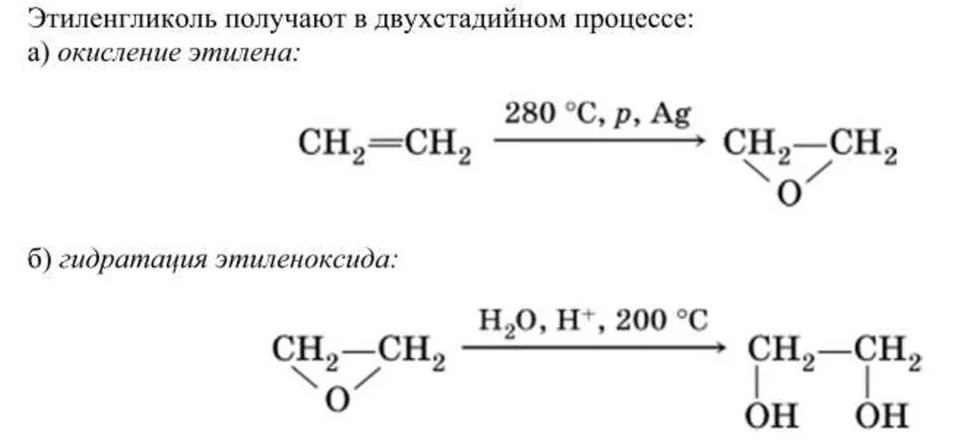
Глицерин – бесцветная, вязкая, сиропообразная жидкость, сладкая на вкус. Не ядовит. Глицерин не имеет запаха, его tпл = 180С, tкип = 2900С. Глицерин гигроскопичен, хорошо смешивается с водой и этанолом. На этом свойстве основано применение глицерина в косметической промышленности, где глицерин используется для увлажнения кожи.
 Абсолютно чистый безводный глицерин затвердевает при +180С, но получить его в твердом виде чрезвычайно сложно.
Абсолютно чистый безводный глицерин затвердевает при +180С, но получить его в твердом виде чрезвычайно сложно.
Глицерин широко распространен в живой природе. Он играет важную роль в процессах обмена в организмах животных, входит в состав большинства липидов – жиров и других веществ, содержащихся в животных и растительных тканях и выполняющих в живых организмах важнейшие функции. Благодаря этим свойствам глицерин является важным компонентов многих пищевых продуктов, кремов, косметических средств.
|
|
|
Этиленгликоль и глицерин, благодаря наличию гидроксильных групп, могут образовывать водородные связи с молекулами воды, этим объясняется их не ограниченная растворимость в воде.
Получение глицерина.
1.Промышленный способ- трехстадийный синтез из пропилена:
1 вариант:
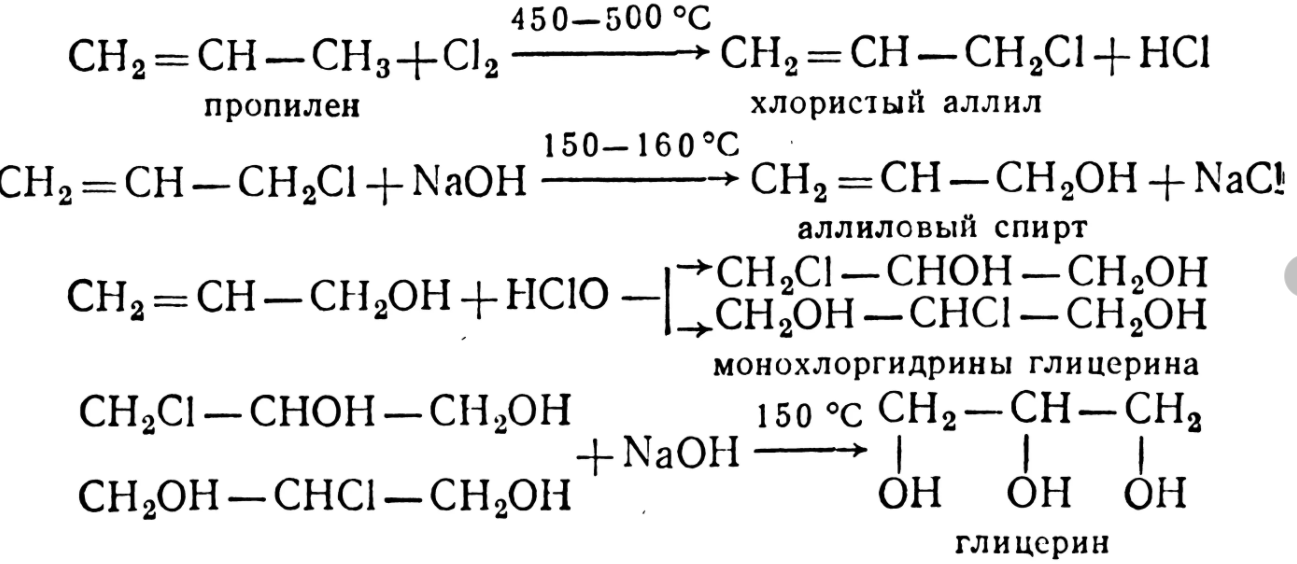
2 вариант:
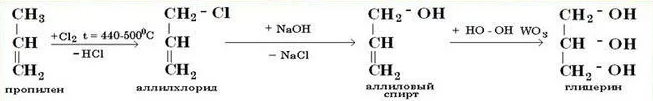
Гидролиз жиров:
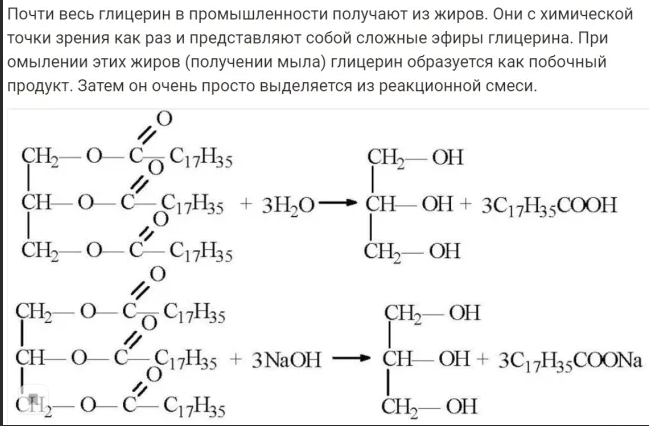
В общем виде:
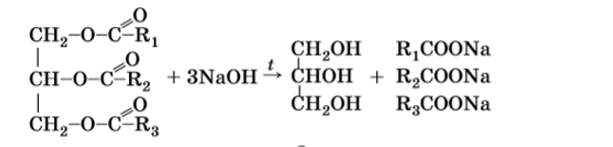
Лабораторный способ: щелочной гидролиз 1,2,3- трихлор (бром) пропана:

Химические свойства одноатомных спиртов.
I . Замещение атома водорода гидроксильной группы:
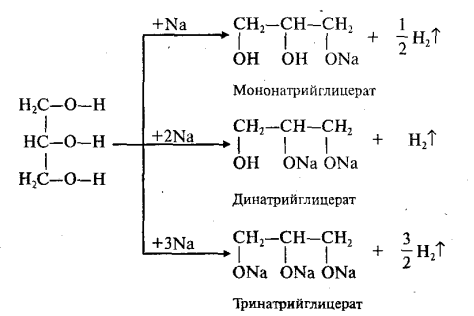
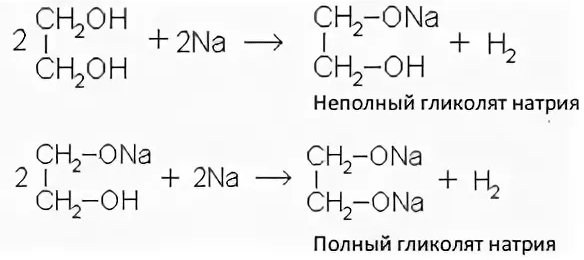 1. С активными металлами:
1. С активными металлами:
 2.Реакция этерификации- взаимодействие с высшими карбоновыми кислотами и кислородсодержащими неорганическими кислотами:
2.Реакция этерификации- взаимодействие с высшими карбоновыми кислотами и кислородсодержащими неорганическими кислотами: 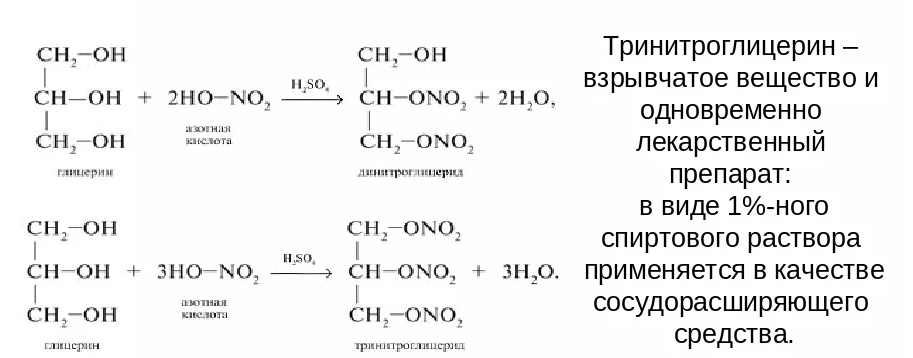
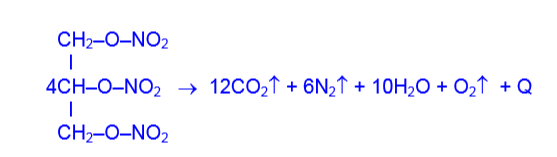

Взаимодействие с карбоновыми кислотами:

Качественная реакция- взаимодействие с гидроксидом меди ( II )

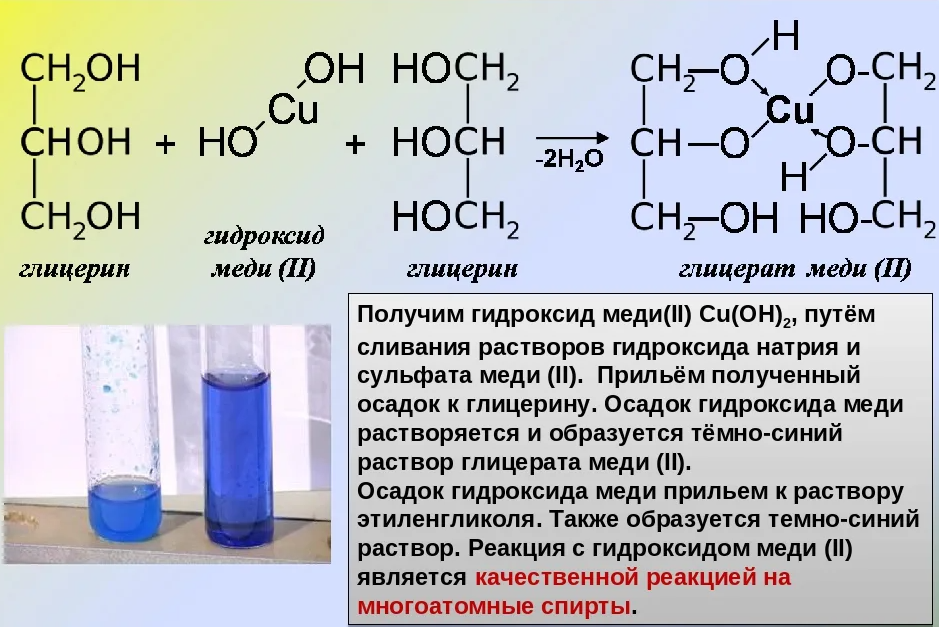
!!!! Такая реакция возможна, если гидроксильные группы находятся у соседних атомов углерода. Если они разделены хотя бы одним атомом углерода- такая реакция не пойдет!
|
|
|
II . Замещение гидроксильных групп.
Замещение гидроксильных групп на галоген:

III . Дегидратация:


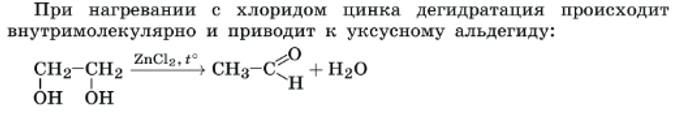
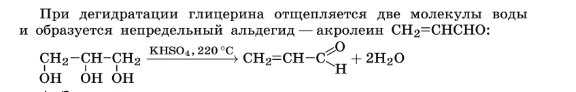
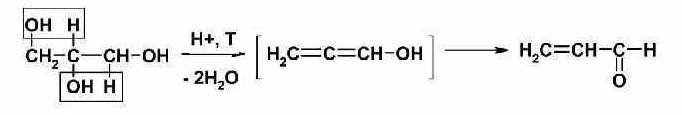
IV .Реакция поликонденсации:
Реакция поликонденсации характерна имеет большое практическое значение для этиленгликоля: 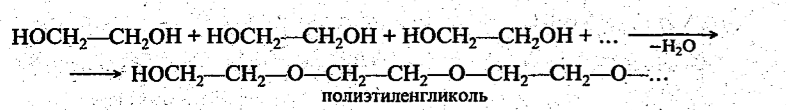
Сфера применения полиэтиленгликоля. Их используют в качестве как растворителей, так и стабилизаторов. В пищевой промышленности их используют в качестве пищевой добавки. В пеногасителях, подсластителей, в производстве БАДов. Этим веществом обрабатывают свежие овощи и фрукты, для лучшего хранения. Они образуют пленку, которая останавливает доступ воздуха к продуктам.
Получение лавсана:
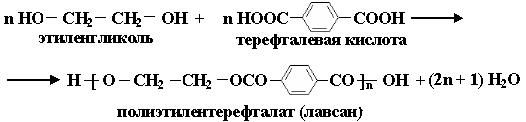

V .Окисление многоатомных спиртов.
Процесс окисления многоатомных спиртов происходит ступенчато. При этом первичные спиртовые группы превращаются в альдегидные, а вторичные- в кетонные:
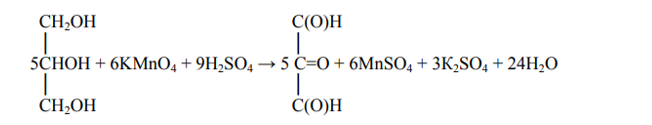
Возможно также окисление первичных спиртовых групп до карбоксильных:
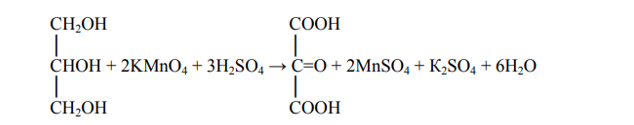
Окисление этиленгликоля:
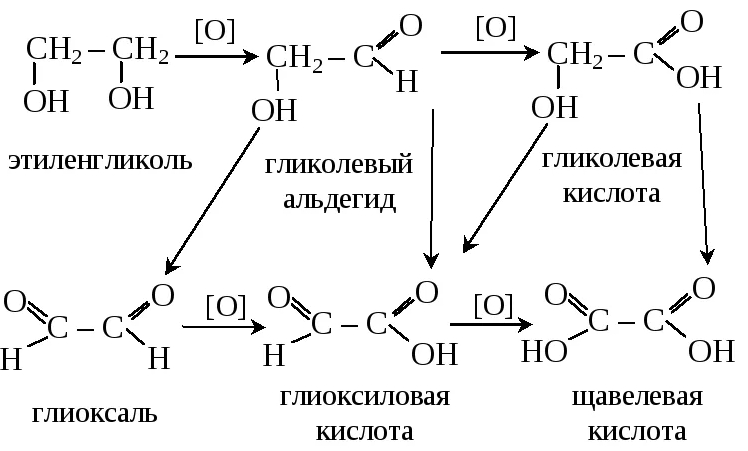
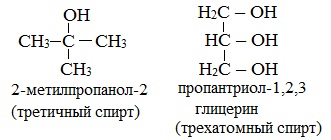
Какая разница между третичным и трехатомным спиртом?
Третичным называется спирт, в котором функциональная группа -ОН связана с третичным атомом углерода. Трехатомным называют спирт, в котором имеется три функциональных группы – ОН.
|
|
|
Дата добавления: 2022-01-22; просмотров: 45; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!
