I . Болезни поджелудочной железы.
ЛЕКЦИЯ № 1 4
ПАТОЛОГИЧЕСКАЯ ФИЗИОЛОГИЯ ОРГАНОВ ПИЩЕВАРЕНИЯ
(часть 1)
ЯЗВЕННАЯ БОЛЕЗНЬ ЖЕЛУДКА
И ДВЕНАДЦАТИПЕРСТНОЙ КИШКИ
(часть 2)
БОЛЕЗНИ ПОДЖЕЛУДОЧНОЙ ЖЕЛЕЗЫ И ПЕЧЕНИ
ПЛАН
1. Язвенная болезнь (ЯБ) как мировая проблема.
2. Этиология ЯБ (современные взгляды).
3. Патогенез ЯБ. Современные взгляды. Теория «едкого щелочного плевка».
4. Механизм образования пилоробульбарных язв.
5. Механизм образования медиогастральных язв.
6. Заболевания поджелудочной железы (панкреатит): этиология, патогенез.
7. Заболевания печени (гепатиты, гепатозы, цирроз): этиология.
8. Заболевания печени (гепатиты, гепатозы, цирроз): патогенез.
9. Взаимосвязь патологии печени с патологией других органов и систем.
Язвенное поражение гастродуоденальной зоны желудочно-кишечного тракта (ЖКТ) – широко распространённая патология. Язвенная болезнь (ЯБ) поражала население Земли ещё с древних времён, на что указывает изучение древнеегипетских мумий, у которых находили признаки данной болезни.
ЯБ – одно из наиболее распространённых заболеваний среди трудоспособного населения и составляет около 20-30% всех заболеваний ЖКТ, которые, в свою очередь, занимают третье место по распространённости в мире после заболеваний сердечно-сосудистой системы и онкологической патологии. Данной патологией в наше время в разных странах в течение жизни страдает от 3 до 20 % всего взрослого населения, а у 15 – 30 % больных ЯБ в течение 5-10 лет заболевания возникают различные осложнения, требующие хирургического вмешательства.
|
|
|
Этиология. В понимании этиологии язвенной болезни в последние годы произошли существенные изменения. Сформировался новый взгляд на этиологию данного заболевания в связи с открытием в 1983 г. австралийскими учёными Б.Маршаллом и Дж. Уоренном инфекции, названной позднее Helicobacter pylori (НР)( Нобелевская премия 2005года). Выяснение роли НР в этиологии и патогенезе хронического гастрита (ХГ), язвенной болезни (ЯБ), рака желудка (РЖ) и МАLT-лимфомы стало настоящей революцией в гастроэнтерологии.
По данным мультицентровых исследований в разных странах, до 60% общей популяции инфицировано НР начиная с детского возраста; с наличием НР связано более 90-96,3% ЯБ ДПК и более 60% ЯБЖ. Данное открытие изменило подход терапевтического лечения, к основополагающей формуле которого «Без кислоты - нет язвы», добавилось «Без НР-инфекции – нет язвы», что стало причиной создания новых схем лечения.
Патогенез. Что касается представлений о патогенезе ЯБ, то за последние 45 лет они не претерпели существенных изменений. В качестве основного механизма её развития рассматриваются нарушения равновесия между факторами “агрессии” (кислотно-пептический фактор, желчь и панкреатический сок (следствие дуоденогастрального рефлюкса), нарушение моторно-эвакуаторной функции желудка, хеликобактерная контаминация слизистой оболочки желудка) и факторами “защиты” слизистой оболочки желудка и слизистой оболочки двенадцатиперстной кишки (анатомический барьер, который состоит из клеток поверхностного эпителия, базальных мембран и системы микроциркуляции слизистой оболочки, а также желудочное слизеобразование, активная секреция гидрокарбонатов, регенераторно-трофические процессы в слизистой оболочке, простагландины, местные иммунные механизмы) («весы» Шея 1961 г.).
|
|
|
Вместе с тем такое понимание патогенеза не объясняет ряд явлений, типичных при ЯБ, а именно:
1) локальность поражений;
2) отсутствие зависимости формирования ЯБ от уровня кислотности желудочного сока.
Фактически до 2007 года не было теории, которая до конца бы объяснила механизм язвообразования, и роль хеликобактерной инфекции в этом процессе
В 2007 году украинскими учёными-патофизиологами Авраменко А.А. и Гоженко А.И. в результате 15-ти летних исследований была выдвинута новая теория – теория «едкого щелочного плевка», в основу которой положен вывод об отсутствии роли кислотного фактора желудка как фактора повреждения: главную роль в этом процессе отводится веществу, которое является производным НР-инфекции – аммиаку.
|
|
|
НР-инфекции для выживания в кислой среде необходим фактор, который бы способствовал нейтрализации соляной кислоты. Этим фактором является газ аммиак, который бактерия образует, расщепляя пищевую мочевину при помощи фермента уреазы. Соединяясь с водой, аммиак образует нашатырный спирт, в состав которого входит гидроксид аммония и который относится к едким щелочам.
В результате простой и всем известной химической реакции – реакции нейтрализации (кислота + щёлочь = вода и нейтральная соль) вокруг бактерии образуется нейтральная зона, благоприятная для её выживания.
Однако не весь аммиак идёт на нейтрализацию кислоты вокруг бактерий: часть аммиака – остаточный аммиак (ОА), учитывая летучесть этого газа, скапливается в полости желудка, который, по своей сути, представляет мышечный мешок. Учитывая высокую влажность в полости желудка (94 – 96%) здесь создаются условия для соединения остаточного аммиака с водой с образованием нашатырного спирта, однако низкой концентрации. В образовании нашатырного спирта высокой концентрации, способной повредить слизистую желудка и двенадцатиперстной кишки, участвуют 2 механизма: эффект «поршня» и эффект «кузнечных мехов»
|
|
|
1. ЭФФЕКТ « ПОРШНЯ»
В основе формирования эффекта «поршня» лежит способность желудка увеличивать глубину и ускорять быстроту перистальтической волны (гиперкинез) под воздействием стрессовых ситуаций. При этом глубина перистальтики настолько велика, что формирует своеобразный поршень, который с большой силой и под большим давлением гонит остаточный аммиак к выходу из желудка. Учитывая тот факт, что выходной отдел желудка имеет форму усеченного конуса, то с уменьшением площади сечения концентрация аммиака становиться больше, что способствует формированию повреждающего фактора – гидроксида аммония.
2. ЭФФЕКТ «КУЗНЕЧНЫХ МЕХОВ»
В основе формирования эффекта «кузнечных мехов» лежит эффект повышения давления в полости желудка при резком напряжении мышц передней брюшной стенки. При этом аммиак также будет больше концентрироваться в выходном отделе желудка.
В зависимости от диаметра пилорического жома язва может образовываться как в луковице двенадцатиперстной кишки, так и в выходном отделе желудка (рис. 1, 2).

Рис.1 Механизм формирования язвенных поражений луковицы двенадцатиперстной кишки:
а) направление потоков «остаточного» аммиака в полости желудка;
б) пилорический жом в полусомкнутом состоянии (d < 1,0 см);
в) место максимальной концентрации «остаточного» аммиака (пилорический канал) в виде устойчивого плотного потока;
г) место язвенных поражений тканей стенки луковицы двенадцатиперстной кишки (любой отдел луковицы двенадцатиперстной кишки).
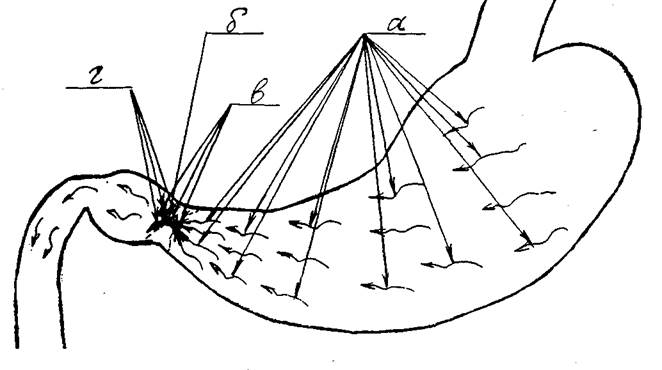
Рис.2 Механизм формирования язвенных поражений в препилорической зоне антрального отдела желудка, в пилорическом канале и в пилоробульбарной зоне у больных хроническим хеликобактериозом:
а) направление потоков «остаточного» аммиака в полости желудка;
б) пилорический жом в спастическом состоянии;
в) места максимальной концентрации «остаточного» аммиака (препилорическая зона антрального отдела желудка, пилорический канал и пилоробульбарная зона);
г) места язвенных поражений (препилорическая зона антрального отдела желудка, пилорический канал и пилоробульбарная зона).
К факторам, которые также влияют на концентрацию аммиака в полости желудка, относятся:
1) концентрация бактерий на слизистой желудка (чем больше бактерий, тем больше остаточного аммиака в полости желудка);
2) наличие мочевины в виде удобрения – карбамида – в овощах и фруктах (бактерия разлагает всю мочевину без ограничения, способствуя повышению концентрации остаточного аммиака);
3) повышение кислотности: естественным путём – стресс; искусственным – при приёме кофе, чёрного шоколада; алкоголя в виде пива, вина; специй, раздражающих слизистую (хрен, горчица и т.д.); приём очень кислых продуктов. Это провоцирует НР-инфекцию на выработку большего количества аммиака как общего, так и остаточного;
4) курение (при курении образуется аммиак, который вместе с бронхиальной слизью заглатывается больным в полость желудка.
Образование язв в луковице двенадцатиперстной кишки и в выходном отделе желудка объединяют в одну группу язв – пилоробульбарных, которые, как мы видим с точки зрения новой теории, имеют общий механизм.
Надо отметить, что эта группа язв образуется при достоверно большей концентрации НР-инфекции на слизистой антрального отдела желудка, что сразу создаёт большую концентрацию остаточного аммиака в этой зоне. Кроме того, по стадии развития хронического гастрита типа В, концентрация бактерий именно в этой зоне создаёт высокую кислотность в полости желудка, так как НР-инфекция, раздражая G –клетки этой зоны, провоцирует выработку гормона гастрин, который стимулирует выработку соляной кислоты. Отсюда и пошло заблуждение, что именно повышенная кислотность является причиной язвообразования.
Кроме пилоробульбарных язв имеются медиогастральные язвы – язвы, которые образуются по малой кривизне тела желудка при нормальной и низкой кислотности желудочного сока. Раньше образование этих язв сводилось к слабости слизистой желудка, что было малоубедительным. Исходя из наших исследований и согласно новой теории образование язв данной локализации зависит от двух факторов – концентрации бактерий именно в теле желудка и нахождения бактерий относительно клеток эпителия и желез слизистой желудка – внеклеточно или внутриклеточно.
Суть формирования язв в этой зоне заключается в том, что почти вся НР-инфекция переселяется на слизистую тела желудка, но по большой кривизне бактерии находятся на поверхности клеток, создавая высокую концентрацию остаточного аммиака, который, согласно законам физики, подымается вверх к малой кривизне, где бактерии находятся внутри париетальных клеток и блокируют выработку ими соляной кислоты, делая слизистую беззащитной перед едкой щёлочью, которая образуется в этом месте из остаточного аммиака. В формировании повреждающей концентрации гидроксида аммония большую роль играет только один эффект – эффект «кузнечных мехов», который возникает при ритмичной физической нагрузке, когда мышцы брюшного пресса, ритмично сокращаясь снизу – вверх, в том же направлении гонят остаточный аммиак – от большой кривизны тела желудка – к малой, где беззащитная слизистая подвергается воздействию концентрированного гидроксида аммония, в тезультате чего на слизистой образуется большой (до 2,5 – 4 см), глубокий дефект, который нередко сопровождается разрывом (прободением) язвы, что требует срочного оперативного лечения. Графически данный процесс можно представить следующим образом (рис. 3)

Рис.3 Механизм формирования медиогастральных язвенных поражений:
а) направление потоков «остаточного» аммиака в полости желудка;
б) пилорический жом в зияющем состоянии;
в) места максимальной концентрации «остаточного» аммиака (средняя треть – верхняя треть тела желудка по малой кривизне);
г) места язвенных поражений (ткани средней трети – верхней трети тела желудка по малой кривизне).
К факторам, которые также влияют на концентрацию аммиака в полости желудка и при формировании этих язв, также относятся:
1) концентрация бактерий на слизистой желудка (чем больше бактерий, тем больше остаточного аммиака в полости желудка);
2) наличие мочевины в виде удобрения – карбамида – в овощах и фруктах (бактерия разлагает всю мочевину без ограничения, способствуя повышению концентрации остаточного аммиака);
3) повышение кислотности: естественным путём – стресс; искусственным – при приёме кофе, шоколада; алкоголя в виде пива, вина; специй, раздражающих слизистую (хрен, горчица и т.д.); приём очень кислых продуктов. Это провоцирует НР-инфекцию на выработку большего количества аммиака как общего, так и остаточного;
4) курение (при курении образуется аммиак, который вместе с бронхиальной слизью заглатывается больным в полость желудка.
Таким образом можно сделать вывод, что исходя из новой теории, процесс язвообразования напрямую является следствием хронического гастрита типа В, который находится в активной форме. Формирование повреждающего фактора – концентрированного гидроксида аммония – зависит от ряда факторов, которые определяют как сам механизм формирования повреждающего фактора, так и локальность и место повреждения.
Понимание данного механизма язвообразования очень важно для врачей - реабилитологов, которые назначают больным ЛФК и массаж, которые также могут привести к повышению внутрижелудочного давления и спровоцировать язвообразование.
I . Болезни поджелудочной железы.
Панкреатит – воспаление поджелудочной железы, которое нередко протекает остро и может сопровождаться развитием панкреатического шока, опасного для жизни.
В этиологии панкреатита существенное значение придают злоупотреблению алкоголем и сопровождающему его перееданию, обильному приёму жирной пищи, жёлчным камням и полипам протока поджелудочной железы, механическому повреждению поджелудочной железы и сфинктера печёночно- поджелудочной ампулы (сфинктера Одди) при травмах и хирургических вмешательствах, интоксикации, действию антибиотиков. Последние данные, подтверждённые как последним Европейским съездом панкреатологов (Стокгольм, Швеция 2010 г.), так и Всемирным съездом панкреатологов (Токио, Япония, 2010 г.), говорят о большой роли курения в формировании этого процесса: курящие болеют гораздо чаще, чем даже сильно пьющие, хотя механизм воздействия курения на поджелудочную железу ещё плохо изучен.
В патогенезе панкреатита важную роль играют повышение секреции панкреатического сока, нарушение оттока секрета, повышение давления в протоке поджелудочной железы, попадание в проток желчи и дуоденального химуса (содержащего энтерокиназу), нарушение микроциркуляции, трофики и барьерных свойств экзогенных панкреоцитов.
Основным звеном патогенеза панкреатита является преждевременная активация ферментов (трипсина, эластазы, фосфолипазы А) непосредственно в протоках и клетках железы, которая происходит под воздействием энтерокиназы, желчи или при повреждении панкреацитов. Следствием этого является аутолиз (самопереваривание) ткани железы, некроз отдельных её участков и образование токсических (лизолецитин) и биологически активных веществ (БАВ), в число которых входят кинины, обладающие мощным сосудистым и гипотензивным действием. Выход пептидаз и других панкреатических ферментов в кровь приводит к тяжёлым расстройствам гемодинамики, дыхания и других жизненно важных функций (панкреатический шок).
Важную роль в патогенезе указанных нарушений играет изменение равновесия между протеолитическими ферментами и их ингибиторами. Последние вырабатываются самой железой и другими органами (слюнные железы, лёгкие) и с успехом применяются для лечения панкреатита.
Определённое значение в патогенезе панкреатита, особенно хронического, принадлежит нарушениям кровообращения в поджелудочной железе (при атеросклерозе, гипертонической болезни), а также иммунологическому (аутоаллергическому) фактору, о чём свидетельствует обнаружение противопанкреатических антител в крови у некоторых лиц, больных холецистопанкреатитом.
I I . Болезни печени
В основе различных заболеваний печени чаще всего лежат такие патологические процессы, как воспаление, нарушение периферического кровообращения, обмена веществ, опухоли.
Воспалительные поражения печени называются гепатитами, первичное изменение обмена веществ гепатоцитов с развитием дистрофии – гепатозами и обменными заболеваниями печени (например, жировой гепатоз или жировая дистрофия печени), а диффузное разрастание соединительной ткани на фоне дистрофии, некроза паренхимы и перестройки структуры органа – циррозом печени.
Этиология. По этиологии все поражения печени подразделяются на приобретенные и наследственные.
К этиологическим факторам, вызывающим болезни печени и синдромы, относятся следующие:
1) инфекционные - вирусы и бактерии (вирусы вирусного гепатита, возбудитель туберкулёза, сифилиса), простейшие (лямблии, амёбы), грибы (актиномицеты), гельминты (эхинококк, аскариды);
2) токсические вещества – экзогенного (алкоголь; лекарственные средства (особенно антибиотики, цитостатики); промышленные яды (хлороформ, мышьяк); растительные яды (мускарин, алколоиды) и эндогенного происхождения (продукты распада тканей при ожоге, некрозе, токсикоз беременности);
3) физические факторы – ионизирующая радиация (лучевой гепатит), механическая травма;
4) алиментарные факторы – белковое, витаминное голодание, жирная пища;
5) аллергические реакции - при введении вакцин, сывороток, пищевых и лекарственных аллергенов;
6) нарушение кровообращения в печени местного (ишемия, венозная гиперемия, тромбоз, эмболия) и общего характера (при сердечно-сосудистой недостаточности);
7) эндокринные и обменные нарушения в организме (сахарный диабет, ожирение);
8) опухоли - первичные (гепатокарцинома) и метастатические (при раке желудка, лёгких, молочной железы);
9) генетические дефекты обмена (наследственные ферментопатии), врождённые пороки анатомического положения и структуры печени вследствие нарушения внутриутробного развития.
Патогенез. В патогенезе поражений печени различной этиологии следует отметить две разновидности патологических реакций:
1) прямое повреждение печени этиологическим фактором (вирусы, химические вещества, нарушение кровотока), проявляющиеся дистрофическими изменениями в ней, вплоть до некроза;
2) аутоиммунное повреждение печени вследствие появления аутоантигенов (патологически изменённые компоненты гепатоцитов, образовавшиеся при прямом поражении печени) и развития аутоаллергических реакций гуморального и клеточного типа.
Последние углубляют повреждение печени в результате микроциркуляторных нарушений ( под влиянием БАВ, активированных при реакции антиген – антитело) и иммунного цитолиза при участии Т-киллеров.
Следует отметить определённую взаимосвязь патологических процессов в печени: как правило, воспалительные (гепатиты) и обменно-дистрофические (гепатозы) поражения печени завершаются развитием цирроза.
Для патологии печени характерна высокая частота сочетанных нарушений печени и органов пищеварительной системы, селезёнки, почек, что обусловлено анатомическими и функциональными связями между этими органами.
Так, секретируемая и экскретируемая печенью желчь участвует в переваривании и всасывании компонентов пищи в кишечнике, обеспечивает моторику кишок. В печени происходит промежуточный обмен продуктов гидролиза пищи, многие из которых депонируются в ней. Всё это позволяет рассматривать печень и органы ЖКТ как единую гепатоэнтеральную систему, в которой заболевание одной из частей влечёт за собой поражение другой.
Общность крово- и лимфообращения, иннервации и ряда функций (кроветворение и кроверазрушение, барьерная функция, иммунопоэз, метаболизм, депонирование крови) связывает печень с селезёнкой и приводит к частому совместному поражению этих органов (гепатолиенальный синдром).
Функциональная общность печени и почек как экскреторных органов обусловливает компенсаторное включение одного из них при поражении другого. Возможность их сочетанного поражения связана с тем, что печень участвует в обмене ряда гормонов и БАВ, регулирующих фильтрационную и реабсорбционную функцию почек (гепаторенальный синдром).
Общей закономерностью для заболеваний и синдромов поражения печени является развитие печёночной недостаточности, которая характеризуется частичным или полным нарушением основных функций печени.
Печень активно включается в адаптивные реакции при заболеваниях других органов и систем. В то же время функциональная недостаточность печени при её поражении может усугубить течение патологического процесса в других органах, изменить гормональную регуляцию, повлиять на эффективность лекарственной терапии.
Толковый словарь
к лекции № 16
Дата добавления: 2022-01-22; просмотров: 10; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!
