Гетероциклические соединения с двумя и более атомами азота
Существуют гетероциклические соединения, в молекулы которых входят по два и более атомов азота. Наиболее важными из них являются пиримидин и пурин. Эти соединения входят в состав нуклеиновых кислот, ответственных за передачу наследственной информации.
Пиримидин и пурин, а также их производные относят к азотистым основаниям, так как атом азота, не связанный с атомом водорода, придает этим соединениям основные свойства.
Производные пиримидина и пурина
В состав нуклеиновых кислот входят производные пиримидина: урацил, тимин и цитозин.
Из производных пурина в состав нуклеиновых кислот входят аденин и гуанин.
Нуклеиновые кислоты
Нуклеиновые кислоты – биологические полимеры, состоящие из большого числа нуклеотидов. В свою очередь, нуклеотиды образованы остатками пиримидиновых и пуриновых оснований, углеводами: рибозой или дезоксирибозой, а также остатками ортофосфорной кислоты.
Нуклеотиды соединены между собой сложноэфирными связями.
Нуклеиновые кислоты, в состав которых входят нуклеотиды, содержащие остатки углевода рибозы получили название РНК – рибонуклеиновые кислоты. В состав нуклеотидов РНК входят аденин, гуанин, урацил и цитозин. РНК представляют собой одиночную спираль.
ДНК – дезоксирибонуклеиновая кислота, образована нуклеотидами, состоящими из остатков углевода дезоксирибозы и азотистых оснований аденина, гуанина, тимина и цитозина. ДНК состоит из двух спиралей, соединённых друг с другом водородными связями.
|
|
|
Водородные связи могут образовываться только между азотистыми основаниями определённого вида. Пиримидиновое основание всегда соединяется с пуриновым, причем тимин (или урацил) всегда образует связь с аденином, а цитозин – с гуанином. Азотистые основания, образующие пары за счет водородных связей, называются комплементарными, то есть дополняющими друг друга.
Роль ДНК в живом организме трудно переоценить. В ней закодирован состав всех белков организма. РНК считывает эту информацию (транскрипция), переносит её к рибосомам и участвует в синтезе белка (трансляция).
ПРИМЕРЫ И РАЗБОР РЕШЕНИЙ ЗАДАЧ ТРЕНИРОВОЧНОГО МОДУЛЯ
1. Решение задачи на вычисление выхода продукта реакции.
Условие задачи: При йодировании 50 г пиррола получили 360 г тетрайодпиррола. Чему равен выход продукта реакции? Ответ запишите с точностью до десятых долей.
Шаг первый: вычислим молярную массу пиррола.
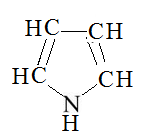 М1 = 4·12 + 14 + 5·1 = 67 г/моль.
М1 = 4·12 + 14 + 5·1 = 67 г/моль.
Шаг второй: вычислим молярную массу тетрайодпиррола:
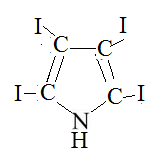 М2 = 4·12 + 14 + 4·127 + 1 = 571 г/моль.
М2 = 4·12 + 14 + 4·127 + 1 = 571 г/моль.
Шаг третий: найдем количество тетрайодпиррола при 100%-ном выходе. Для этого составим пропорцию:
|
|
|
50 : 67 = х : 571, откуда х = (50·571) : 67 = 426 г.
Шаг четвертый: найдём выход продукта реакции.
(360 : 426)·100 = 84,5 %.
Ответ: 84,5.
2.Решение задачи на определение необходимого количества реагента.
Условие задачи: Взаимодействием ацетилена и формальдегида с последующей обработкой промежуточного продукта аммиаком получают пиррол. Выход реакции при использовании 20%-ного избытка аммиака составляет 85%. Какой объём аммиака (л), измеренный при нормальных условиях, необходим для получения 0,5 кг пиррола?
Ответ запишите с точностью до десятых долей.
Шаг первый: В молекуле аммиака один атом азота и в молекуле пиррола тоже один атом азота, то есть для получения 1 моль пиррола требуется (без учёта избытка) 1 моль аммиака. При нормальных условиях 1 моль аммиака занимает объём, равный 22,4 л.
Шаг второй: вычислим молярную массу пиррола:
 М1 = 4·12 + 14 + 5·1 = 67 г/моль.
М1 = 4·12 + 14 + 5·1 = 67 г/моль.
Шаг третий: составим пропорцию и найдём необходимый объём аммиака.
х : 22,4 = 500 : 67. (0,5 кг = 500 г). х = 167 л.
Шаг четвёртый: найдём объём аммиака с учётом 20%-ного избытка.
167 л – 100 %;
V л – 120 %.
V = (167·120) : 100 = 200,6 л.
Ответ: 200,6
Дата добавления: 2021-12-10; просмотров: 43; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!
