ПРИЛОЖЕНИЕ № 1 «ХРОНИЧЕСКИЕ ГЕПАТИТЫ»
МИНИСТЕРСТВО ОБРАЗОВАНИЯ И НАУКИ
РОССИЙСКОЙ ФЕДЕРАЦИИ
ГОСУДАРСТВЕННОЕ ОБРАЗОВАТЕЛЬНОЕ УЧРЕЖДЕНИЕ ВЫСШЕГО ПРОФЕССИОНАЛЬНОГО ОБРАЗОВАНИЯ
«Сибирский государственный медицинский университет Федерального агентства по здравоохранению и социальному развитию»
(ГОУ ВПО СибГМУ Росздрава)
ДИФФЕРЕНЦИАЛЬНАЯ ДИАГНОСТИКА ПРИ СИНДРОМЕ ГЕПАТОСПЛЕНОМЕГАЛИИ
УЧЕБНОЕ ПОСОБИЕ ДЛЯ СТУДЕНТОВ
ТОМСК – 2005
УДК 616.36:616.411-007.61-079.4
ББК Р 413.31+Р 411.8+Р 34
Ш 185
А.А. Шаловай, М.И. Рачковский
Дифференциальная диагностика при синдроме гепатоспленомегалии: Учебное пособие для студентов VI курса лечебного факультета медицинских вузов. – Томск, 2005. – 105 с.
В пособии систематизированы современные данные, касающиеся дифференциальной диагностики при синдроме гепатоспленомегалии. Описаны диагностические критерии всех групп заболеваний, сопровождающихся увеличением печени и селезенки. Широко представлены новые подходы к диагностике и базисной терапии хронических вирусных гепатитов. Авторы подробно освещают алгоритм дифференциальной диагностики при вышеназванном синдроме. Несомненно ценным является наличие клинических ситуационных задач, позволяющих оценить усвоенный материал.
Рецензенты:
заведующий кафедрой факультетской терапии
Новосибирской государственной медицинской академии,
Заслуженный врач РФ, д.м.н., профессор А.Д. Куимов;
|
|
|
заведующая кафедрой госпитальной терапии
Иркутского государственного медицинского университета,
д.м.н., профессор Г.М.Орлова
Рекомендуется Учебно-методическим объединением по медицинскому и фармацевтическому образованию вузов России в качестве учебного пособия для студентов медицинских вузов
СОДЕРЖАНИЕ
1. Основные причины гепатомегалии………………………………………6
2. Основные группы заболеваний, проявляющиеся синдромом
гепатомегалии …………………………………………………………..7
3. Основные синдромы поражения печени…………………………………8
4. Основные причины гепатолиенального синдрома……………………..12
5. Дифференциально-диагностический поиск при
синдроме гепатомегалии…………………………………..……………..12
6. Программа дифференциально-диагностического
обследования больных с увеличением печени…………………………15
7. Основные диагностические критерии заболеваний, сопровождаю-
щихся гепатоспленомегалией:
Острый вирусный гепатит …………………………………………16
Хронические гепатиты …………………………………………….16
|
|
|
Жировая дистрофия печени ……………………………………….16
Цирроз печени ……………………………………………………...16
Гемохроматоз ………………………………………………………17
Амилоидоз печени …………………………………………………17
Гепатолентикулярная дегенерация ………………………………17
Рак печени …………………………………………………………18
Доброкачественные опухоли печени ……………………………18
Непаразитарные кисты печени …………………………………..18
Эхинококкоз печени ………………………………………………19
Милиарный туберкулез печени ………………………………….19
Туберкулезный гранулематоз ……………………………………19
Туберкулезный холангит …………………………………………19
Очаговый туберкулез …………………………………………….19
Сифилитическое поражение печени …………………………….20
Констриктивный перикардит …………………………………….20
«Застойная» печень ……………………………………………….20
Кардиальный цирроз печени ……………………………………..21
Миксома правого предсердия ……………………………………21
Инфаркт миокара правого желудочка …………………………..21
|
|
|
Болезнь Бадда – Киари ……………………………………………21
8. Гепатомегалия при заболеваниях органов кроветворения:
Острый лейкоз ……………………………………………………22
Хронический миелолейкоз ………………………………………22
Миелофиброз и остеомиелосклероз ……………………………..23
Лимфогранулематоз ………………………………………………24
Болезнь Вальденстрема …………………………………………..24
9. Приложение № 1 "Хронические гепатиты":
Классификация ХГ…………………………………………….….25
Этиологические факторы ХГ……………….…………………….26
Аутоиммунный гепатит…………………………………………..26
Хронический вирусный гепатит В…………………….…………28
Хронический вирусный гепатит D……………………………..35
Хронический гепатит С…………………………………………36
Гепатит G………………………………………………………..39
Хронический лекарственный гепатит………………………….40
Степень активности процесса………………………………….40
Стадия заболевания.......................................................... ….41
Примеры формулировки диагноза.................................. ….41
Алкогольное поражение печени....................................... ….41
Современные подходы к лечению ХГ............................. ….42
|
|
|
Специфическая профилактика.......................................... …53
10. Приложение № 2 " Циррозы печени":
Классификация циррозов печени ..................................... …55
Морфологическая классификация ЦП .............................. …56
Вирусные ЦП ..................................................................... …58
Алкогольный ЦП ................................................................ …68
Первичный билиарный ЦП ................................................ …69
Вторичный билиарный ЦП ................................................ …72
ЦП как проявление генетически обусловленных нарушений
обмена веществ:
Недостаточность альфа-1-антитрипсина.................... ..73
Гемохроматоз...................................................................... ..74
Поздняя кожная порфирия................................................. ..75
Болезнь Вильсона-Коновалова ............................................ ..76
Кардиальный ЦП .......................................................... ...77
Осложнения ЦП .................................................................... ..78
Гепаторенальный синдром……………………………………… …78
Лечение ЦП............................................................................ ...81
11. Клинические ситуационные задачи ...................................... . …86
12. Ответы на клинические ситуационные задачи……………………….95
13. Приложение №3 "Обмен билирубина в норме и патологии. Виды
желтух. Сканограммы печени"………..………………………………….96
14. Литература ............................................................................. ...103
ПРИНЯТЫЕ СОКРАЩЕНИЯ
| AT | аутоиммунный гепатит | |
| АлАт | аланинаминотрансфераза | |
| АсАТ | аспартатаминотрансфераза | |
| ВГ | вирусный гепатит | |
| ГВ | гепатит В | |
| ГГТ | гамма-глютамилтранспептидаза | |
| ГКС | глюкокортикостероиды | |
| ГС | гепатит С | |
| HBV | вирус гепатита В | |
| HDV | вирус гепатита D | |
| HCV | вирус гепатита С | |
| ДНК | дезоксирибонуклеиновая кислота | |
| IgM | иммуноглобулины класса М | |
| IgG | иммуноглобулины класса G | |
| ИФН | интерферон | |
| ЛГ | лекарственный гепатит | |
| ЛДГ | лактатдегидрогеназа | |
| ПТИ | протромбиновый индекс | |
| ПОЛ | перекисное окисление липидов | |
| ПБЦ | первичный билиарный цирроз печени | |
| РНК | рибонуклеиновая кислота | |
| ХАГ | хронический активный гепатит | |
| ХГ | хронический гепатит | |
| ХГВ | хронический гепатит В | |
| ХГС | хронический гепатит С | |
| ХЛГ | хронический лобулярный гепатит | |
| ХПГ | хронический персистирующии гепатит | |
| ЦП | цирроз печени | |
| ЩФ | щелочная фосфатаза |
Цель темы: научить составлению и реализации основ диагностических действий при синдроме гепатоcпленомегалии.
Задачи:
1. Научить диагностике и лечению болезней, проявляющихся гепато-
лиенальным синдромом и гепатомегалией.
2. Научить дифференциальной диагностике отдельных форм хрониче-
ских гепатитов (ХГ) и циррозов печени (ЦП).
АНКЕТА ДЛЯ ПРОВЕРКИ БАЗИСНЫХ ЗНАНИЙ.
1. Группы заболеваний, сопровождающиеся увеличением печени, гепатолиенальным синдромом.
2. Лабораторные и клинические синдромы поражения печени.
3. Новые аспекты диагностических критериев ХГ (этиологические,
активности, стадии заболевания, серологические маркеры).
4. Лечение ХГ ( базисная, этиотропная, патогенетическая, симптома-
тическая терапия).
5. Диагностические критерии ЦП.
6. Диагностические критерии жирового гепатоза, эхинококкоза, рака
печени и доброкачественных опухолей, туберкулеза печени, болезни Бад-
да-Киари.
7. Диагностические критерии гемохроматоза, амилоидоза печени,
болезней накопления.
8. Особенности гепатомегалии при сердечно-сосудистых заболевани-
ях ("застойная" печень, кардиальный ЦП), болезнях крови.
ОСНОВНЫЕ ПРИЧИНЫ ГЕПАТОМЕГАЛИИ
1. Собственно болезни печени (острые и хронические гепатиты,
циррозы печени, опухоли, жировая дистрофия, непаразитарные кисты, ту-
беркулез, болезнь Бадда-Киари).
2. Болезни накопления (гемохроматоз, гепатолентикулярная дегене-
рация, амилоидоз).
3. Болезни сердечно-сосудистой системы (констриктивный перикардит).
ОСНОВНЫЕ ГРУППЫ ЗАБОЛЕВАНИЙ, ПРОЯВЛЯЮЩИЕСЯ СИНДРОМОМ ГЕПАТОМЕГАЛИИ
1. Острые и хронические диффузные поражения печени:
- стеатоз
- острый вирусный гепатит
- острый алкогольный гепатит
- хронический вирусный гепатит
- аутоиммунный гепатит
- лекарственный гепатит
- хронический алкогольный гепатит
- реактивный гепатит
- фиброз печени
- цирроз печени (алкогольный, вирусный, врожденный, первичный
билиарный)
- гемосидероз
2.Холестаз внепеченочный:
- холецистит
- холангит
- холелитиаз
- стриктуры и кисты холедоха
- новообразования
3. Застой крови в воротной и печеночной венах:
- сердечная недостаточность (гипертоническая и коронарная болезнь, легочное сердце, пороки сердца, констриктивный перикардит)
- болезни сосудов (эндофлебит)
- фиброэластоз
4.Болезни крови и кроветворных органов:
- острые лейкозы
- миелопролиферативные заболевания (хронический миелолейкоз, ос-
теомиелофиброз, эритремия)
-лимфопролиферативные заболевания (хронический лимфолейкоз,
лимфогранулематоз)
5. Инфекционные заболевания:
- малярия, мононуклеоз, Коксаки
- сепсис
- эндокардит
- специфические заболевания (сифилис, туберкулез)
6. Паразитарные заболевания:
- описторхоз
- эхинококкоз
7. Очаговые поражения печени:
- кисты печени
- доброкачественные опухоли печени (гемангиома, аденома)
- первичный рак печени ( гепатоцеллюлярная карцинома, холангио-
карцинома)
- метастатический рак печени
8. Наследственные болезни:
- болезнь Жильбера
- гемохроматоз
- гепатолентикулярная дегенерация
- болезнь Ниманна-Пика
- альфа 1-антитрипсиновая недостаточность
- первичный амилоидоз печени
2. Системные заболевания (СКВ, ревматоидный артрит,с.Фелти и т.д.)
ОСНОВНЫЕ СИНДРОМЫ ПОРАЖЕНИЯ ПЕЧЕНИ
Астеновегетативный синдром:
клиническими признаками являются слабость, выраженная утомляемость, снижение работоспособности, нервозность, ипохондрия, резкое похудание, нарушение сна.
Диспепсический синдром:
тошнота, плохой аппетит, рвота, тяжесть в эпигастрии и правом подреберье, отрыжка, упорное вздутие живота, запоры.
Мезенхималъно-воспалителъный синдром (иммуновоспалительный синдром).
Обусловлен сенсибилизацией клеток иммунокомпетентной ткани и активацией ретикулогистиоцитарной системы. Гистологическим выражением этого синдрома является лимфомакрофагальная инфильтрация, клинические признаки - это лихорадка, артралгии, васкулиты, лимфадено-патия. Лабораторные признаки - повышение уровня гамма-глобулинов (нередко с гиперпротеинемией), изменение осадочных проб (повышение тимоловой и уменьшение сулемовой), увеличение содержания ЦИК и иммуноглобулинов классов G, М, А, появление LE-клеток, неспецифических антител к ДНК, гладкомышечным волокнам, митохондриям, снижение титра комплемента, теста бласттрансформации лимфоцитов и реакции торможения миграции лейкоцитов.
Цитолитический синдром
обусловлен нарушением целостности мембран гепатоцитов и их органелл, приводящим к выделению составных частей клеток в межклеточное пространство и кровь. Гистологические изменения характеризуются зернистой, а затем баллонной (гидропической) дистрофией гепатоцитов и развитием некрозов. Для цитолитического синдрома характерны:
а), повышение активности ферментов - индикаторов цитолиза и пече-ночноклеточных некрозов - аспартатаминотрансферазы (АсАТ), аланина-минотрансферазы (АлАТ), альдолазы, глютаматдегидрогеназы, сорбитде-гидрогеназы, орнитинарбамилтраннсферазы, лактатдегидрогеназы (ЛДГ) и ее изоферментов ЛДГ-4 и ЛДГ-5;
б) гипербилирубинемия с повышением преимущественно прямой
фракции;
в) повышение в сыворотке крови концентрации витамина В12, железа.
Холестатический синдром
обусловлен недостаточным выделением всех или основных компонентов желчи. Морфологическим проявлением холестаза служит накопление желчных пигментов в гепатоцитах и (или) желчных протоках.
Выделяют следующие виды холестаза:
1. Внутрипечночный. За начальный уровень холестаза принимают измененные органеллы печеночной клетки, в частности гладкую эндоплазматическую сеть или группу органелл гепатоцита, называемую желчесекреторным аппаратом. Протоки портального тракта признают конечным уровнем внутрипеченочного холестаза.
2. Внепеченочный (частичный или полный) холестаз обусловлен внутрипротоковым препятствием току желчи камнем, аденокарциномой, редко доброкачественной опухолью; сдавлением протоков опухолью, особено в области ворот печени, острым или хроническим панкреатитом, опухолью головки поджелудочной железы; воспалением с развитием стриктуры и склероза внепеченочных желчных ходов; заболеваниями двенадцатиперстной кишки (ДПК): стенозом сфинктера, стенозом и опухолью большого дуоденального сосочка, опухолью двенадцатиперстной кишки , дивертикулом ДПК. Основными клиническими признаками, как внутри-, так и внепеченочного холестаза, являются упорный кожный зуд (сопровождает холестаз и связан с задержкой желчных кислот и раздражением кожных рецепторов), ахоличный или гипохоличный стул, моча темно-коричневого цвета, желтуха, пигментация кожи, наличие ксантом - внутри-кожных бляшек, располагающихся особенно часто на веках (ксантелазмы), кистях , локтях, коленях, стопах, ягодицах, в подмышечных областях.
Биохимические проявления синдрома холестаза связаны с повышением в сыворотке крови уровня компонентов желчи - холестерина, фосфоли-пидов, В-липопротеидов, прямого билирубина, желчных кислот и ферментов, являющихся маркерами холестаза: щелочной фосфатазы (ЩФ), лейцинаминопептидазы, гамма-глютамилтранспептидазы (ГГТ).
Синдром печеночно-клеточной недостаточности
связан главным образом с нарушением синтетической функции печени. Морфологическим субстратом данного синдрома являются дистрофические изменения гепатоцитов и (или) значительное уменьшение функционирующей паренхимы печени вследствие некрозов.
Клинические признаки достаточно многообразны и связаны с дефицитом тех или иных компонентов, продуцируемых печенью. У больных отмечается «печеночный язык» (малиновая окраска, сглаженные сосочки, что обусловлено гиповитаминозом В12); «печеночные» ладони (т.н. пальмарная эритема - симметричное пятнистое покраснение в области тенара и гипотенара, реже сгибательной поверхности пальцев); сосудистые звездочки (телеангиэктазии, звездчатые ангиомы) состоят из пульсирующей центральной части и лучеобразных разветвлений сосудов, напоминающих ножки паука. Механизм возникновения сосудистых звездочек и «печеночных ладоней» связывают с повышением количества эстрогенов в крови и изменением чувствительности сосудистых рецепторов. Также наблюдаются гинекомастия и женский тип оволосения, атрофия яичек (частые симптомы выраженного расстройства функции печени у мужчин, связанные с гиперэстрогенемией ввиду уменьшения их инактивации в печени); изменения ногтей (феномен «белых ногтей»).
Особо необходимо отметить наличие геморрагического диатеза
- появление на коже кровоизлияний и кровоподтеков на коже и в подкожной клетчатке, кровоточивость десен, носовых кровотечений, гематурии, в отдельных случаях маточных, геморроидальных кровотечений, а также из варикозно расширенных вен пищевода и желудка. В основе синдрома лежат три группы причин: уменьшение синтеза факторов свертывания крови в печени, повышенное потребление факторов свертывания и изменение функциональных свойств тромбоцитов.
Лабораторно недостаточность печени характеризуется снижением содержания в крови альбуминов (ниже 30-35 г/л), трансферрина, уровня про-тромбинового индекса (ПТИ), фибриногена, эфиров холестерина, прокон-вертина, а-липопротеидов, а также снижением активности фермента холи-нэстеразы (ложная или неспецифическая холинэстераза - относится к α2-глобулинам, синтезируется в основном в эндоплазматической сети гепато-цитов).
Синдром портальной гипертензии
- развивается вследствие повышения давления в бассейне воротной вены, вызванного нарушением кровотока различного происхождения и локализации: в портальных сосудах, печеночных венах и нижней полой вене. Клинические симптомы портальной гипертензии - развитие коллатерального кровообращения (расширение вен передней брюшной стенки, а в последующем и в области пупка, вплоть до развития «головы медузы»; варикозное расширение вен пищевода, желудка, геморроидальных вен и кровотечения из них; асцит; спленомегалия).
При внутрипеченочной форме портальной гипертензии препятствие кровотоку находится в самой печени;
при подпеченочной (предпеченочной) препятствие локализуется в стволе воротной вены или ее крупных ветвых, а в случае
надпеченочной (постпеченочной) - кровоток нарушен во внеорганных отделах печеночных вен или в нижней полой вене проксимальнее места впадения в нее печеночных вен.
Спленомегалия.
Основные причины увеличения селезенки при болезнях печени - это портальная гипертензия и системная гиперплазия ретикулогистиоцитарной ткани печени и селезенки в ответ на воспаление. Морфологически в селезенке имеет место гиперплазия ретикулогистиоцитарных элементов, застой крови, диффузное разрастание фиброретикулярной ткани, обеднение пульпы свободными клетками, отложение гемосидерина, увеличение числа артериовенозных шунтов.
Синдром гиперспленизма
нередко сопровождает увеличение селезенки и выражается в усилении и извращении нормальной функции селезенки по удалению разрушенных тромбоцитов, гранулоцитов и эритроцитов. При этом уменьшено количество всех трех типов или отдельных типов клеток периферической крови. Патогенез гиперспленизма обусловлен несколькими факторами. Установлено повышение фагоцитоза в селезеночной пульпе, несомненно и значение портальной гипертензии. Вначале снижается количество тромбоцитов, позже гранулоцитов и при прогрессирующем течении - эритроцитов. Важную роль играют иммунные механизмы, которые приводят к иммунной цитопении. Она развивается вследствие образования селезенкой антител к форменным элементам периферической крови. Красный костный мозг вначале пролиферирует и отвечает повышенным миелопоэзом. Это повышение происходит в известных границах и сменяется негативными изменениями.
Гепатолиенальный синдром
- сочетанное увеличение печени и селезенки. Он объясняется наличием ретикулогистиоцитарного аппарата, объединяющего эти органы, а также тесной связью обоих органов с системой воротной вены, общностью их иннервации и путей лимфооттока.
ОСНОВНЫЕ ПРИЧИНЫ ГЕПАТОЛИЕНАЛЬНОГО СИНДРОМА:
- хронические гепатиты
- альвеококкоз печени
- цирроз печени
- болезни сосудов печени (тромбоз воротной и селезеночной вен, синдром и болезнь Бадда-Киари, тромбоз и воспаление печеночных вен, тромбоз нижней полой вены, веноокклюзионная болезнь)
- наследственные болезни (гемохроматоз, гепатоцеребральная дистрофия, альфа-1антитрипсиновая недостаточность, первичный амилоидоз печени)
- болезни крови и кроветворных органов (хронический миелолейкоз, доброкачественный сублейкемический миелоз, болезнь Вальденстрема, хронический эритромиелоз, хронические моноцитарный, мегакариоцитарный, базофильный и эозинофильный лейкозы, гемолитические анемии, острые лейкозы)
- инфекционный мононуклеоз
- хронический холангит
- слипчивый перикардит с застойным циррозом типа Фридль-Пика
- инфекции, протекающие с одновременным увеличением печени и селезенки.
ДИФФЕРЕНЦИАЛЬНО-ДИАГНОСТИЧЕСКИЙ ПОИСК ПРИ СИНДРОМЕ ГЕПАТОМЕГАЛИИ
Клиническое обследование больных с болезнями печени требует подробного расспроса и тщательного осмотра, так как многие симптомы не привлекают сразу внимание врача.
Расспрос. Сведения о профессии и образе жизни больного помогают выявить длительный контакт с промышленными ядами или инсектицидами
и заподозрить такие инфекции и инвазии, как лептоспироз, эхинококкоз, наиболее частые у людей, занятых в сельском хозяйстве.
Важны указания на периоды голодания больного, в частности недостаток белка в пищевом рационе и длительные заболевания желудочно-кишечного тракта, ведущие к белково-витаминному дефициту. Необходимо обратить внимание на плохую переносимость алкоголя, жиров, никотина.
Употребление алкоголя должно быть изучено максимально точно ввиду его значения в патологии печени. Применение лекарств влечет за собой разнообразные поражения печени, диагностика которых невозможна без знания принятых лекарств и их возможной гепатотоксичности.
Семейный анамнез
позволяет заподозрить наследственные заболевания - доброкачественные гипербилирубинемии, гемолитическую анемию. Неврологические расстройства и патология печени у ближайших родственников больного могут иметь значение в диагностике болезни Вильсона-Коновалова.
Эпидемиологический анамнез.
Важно установить были ли контакты с больными вирусным гепатитом, предшествовавшие данному заболеванию, а также инфекции, переливания крови, стоматологические вмешательства, операции, иньекционная или инфузионная терапия, хронический гемодиализ и другие манипуляции с повреждением кожи и слизистых оболочек, а также наличие наркомании, беспорядочной половой жизни, половых извращений. Существенное значение для диагностики может иметь указание на пребывание больного в очагах вирусного гепатита, лептоспироза, желтой лихорадки, описторхоза и других гепатотропных инфекций и инвазий. Нужно также учитывать принадлежность больного к группам повышенного риска в отношении парентерального гепатита - медработники, персонал станций переливания крови, центров гемодиализа, больные туберкулезных и венерологических стационаров.
Общее состояние следует изучать также тщательно, как и специфические симптомы поражения печени.
Диспепсический синдром
наблюдается при многих болезнях печени и желчных путей, особенно при острых гепатитах, ЦП, холелититазе. Плохой аппетит, тошнота, иногда рвота, тяжесть в эпигастрии, отрыжка, непереносимость жирной пищи, упорное вздутие живота, иногда запоры, дегтеобразный стул могут быть обусловлены печеночно-клеточной недостаточностью, портальной гипертензией.
Похудание возможно при активном гепатите, ЦП, опухолях. Чувство тяжести, давления и ноющая боль в правом подреберье исходят из капсулы печени (серозной оболочки, висцеральной брюшины). К интенсивной боли приводит острое растяжение капсулы печени при остром вирусном гепатите (ОВГ), застойной сердечной недостаточности. При ХГ и ЦП болевые ощущения незначительны или вовсе отсутствуют.
Воспалительное поражение капсулы печени (перигепатит) и спаечный процесс между фиброзной оболочкой и париетальной брюшиной также
приводят к боли в правом подреберье и наблюдаются при раке, абсцессе, сифилисе печени.
Печеночная и желчная колики возникают при желчнокаменной болезни и гипермоторной дискинезии желчных путей.
Лихорадка обычно свойственна холангиту, абсцессу печени. Но возможна и в преджелтушной стадии ОВГ, при токсических поражениях печени, хронических гепатитах, активной стадии ЦП и раке печени.
Увеличение печени –
наиболее частый симптом болезней печени, ее уменьшение наблюдается значительно реже. Патоморфологически увеличение печени может быть обусловлено: дистрофией гепатоцитов (например при гепатозах и тезаурисмозах); лимфо-макрофагальной инфильтрацией при острых и хронических гепатитах; развитием регенераторных узлов и фиброза при ЦП; застоем крови при сердечной недостаточности, эндофлебите печеночных вен, констриктивном перикардите; холестазом внутрипеченочным при первичном билиарном циррозе печени (ПБЦ) и внепеченочным при болезнях, ведущих к нарушению оттока желчи и формированию вторичного билиарного ЦП; очаговыми поражениями при опухолях, кистах, абсцессах.
Увеличенная печень видна в ряде случаев уже при осмотре живота как смещающаяся при дыхании опухоль в правом подреберье или в подложечной области. Длительное и значительное увеличение печени может привести к деформации грудной клетки, межреберные промежутки при этом не заполняются.
Перкуссия органа дает весьма приблизительные результаты. Определяют размеры печени по Курлову (в норме 10-12, 9-11, 8-10 см).
Пальпация дает более определенные результаты. У 88% здоровых людей нижний край печени прощупывается, он мягкий, безболезненный, закруглен, поверхность печени ровная, консистенция эластичная. При болезнях печени край может быть плотным (ХГ), острым (ЦП); у больных с сердечным застоем - закругленным; бугристым - при опухолях, ЦП и паразитарных заболеваниях.
За край правой доли печени можно принять новообразования желчного пузыря, толстой кишки, правой почки. Имитировать гепатомегалию может также гепатоз.
Патология смежных органов может влиять на топографию печени. Так, смещение печени вверх может иметь место при метеоризме, асците, уменьшении легких, высоком стоянии диафрагмы, уменьшении размеров печени. Опущение печени наблюдается при низком стоянии диафрагмы, пневмотораксе, поддиафрагмальном абсцессе, эмфиземе легких, быстрой потере веса, экссудативном плеврите. Отграничить истинное увеличение печени от этих состояний позволяют пальпация в различных положениях больного и обзорная рентгеноскопия брюшной полости, эхолокация печени.
Быстрое увеличение печени характерно для ОВГ, злокачественных опухолей. Быстрое уменьшение органа, если оно не связано с приемом мочегонных препаратов при застойной сердечной недостаточности, указывает на развитие массивных некрозов и является плохим прогностическим признаком.
Болезненность при пальпации печени наиболее свойственна застойной печени, острым воспалительным изменениям. При хронических заболеваниях печени болезненность органа при пальпации появляется в периоды активности процесса, присоединения холангита, гнойных осложнений.
Программа дифференциально-диагностического распознавания болезней, проявляющихся увеличением печени, включает два этапа (схема 1). На первом этапе устанавливают диффузный или очаговый характер носит заболевание печени. На втором этапе проводятся специальные исследования (пункционная биопсия, лапароскопия, ангиография) в гастроэнтерологическом стационаре.
Схема 1
ПРОГРАММА
ДИФФЕРЕНЦИАЛЬНО-ДИАГНОСТИЧЕСКОГО
ОБСЛЕДОВАНИЯ БОЛЬНЫХ С УВЕЛИЧЕНИЕМ ПЕЧЕНИ



 Ультразвуковое исследование печени
Ультразвуковое исследование печени
Сканирование печени
Указания на очаговые поражения
 |
а-фетопротеин
 |
Указание на диффузное поражние
 |


 Пункционная биопсия печени Лапароскопия
Пункционная биопсия печени Лапароскопия
 Положителен Отрицателен
Положителен Отрицателен
Реакция Каццони

 Гепатома
Гепатома

 Положительная Отрицательная
Положительная Отрицательная
 |

 Эхинококкоз печени Лапароскопия
Эхинококкоз печени Лапароскопия
Ангиография печени

Хронический гепатит
 Жировая дистрофия печени
Жировая дистрофия печени
 Амилоидоз
Амилоидоз
 Гемохроматоз
Гемохроматоз
 Цирроз
Цирроз
 Рак печени
Рак печени
 Ангиома
Ангиома
 Поликистоз
Поликистоз
 Киста солитарная
Киста солитарная
Как уже указывалось, заболевания, проявляющиеся преимущественно увеличением печени, разделяются на три группы: собственно болезни печени, болезни накопления и болезни сердечно-сосудистой системы. Для распознавания важно помнить диагностические критерии этих заболеваний.
ОСТРЫЙ ВИРУСНЫЙ ГЕПАТИТ
1. Указание на гемотрансфузии, иньекции, операции и неблагоприятный эпидемиологический анамнез.
2. Повышение активности аминотрансфераз и альдолазы сыворотки крови.
3. Обнаружение маркеров вирусных гепатитов А, В, С, Д.
4. Морфологические признаки острого гепатита в биоптате печени.
5. Печень пальпаторно имеет мягкую консистенцию, болезненна.
ХРОНИЧЕСКИЕ ГЕПАТИТЫ
Вирусный гепатит:
1. Острый вирусный гепатит в анамнезе.
2.Наличие маркеров вирусного гепатита в сыворотке крови или в биоптате печени.
3.Гистологические признаки хронического гепатита .
Аутоиммунный гепатит:
1. Артралгии, лихорадка, синовиты.
2. Маркеры вирусных гепатитов отсутствуют.
3. Иммунные феномены: наличие широкого спектра аутоантител.
4. Гистологические признаки аутоиммунного гепатита.
Более подробная информация по вопросу этиологии, патогенеза, современной классификации хронических гепатитов дана в «Приложении №1» (см).
ЖИРОВАЯ ДИСТРОФИЯ ПЕЧЕНИ
1. Алкоголизм, сахарный диабет, заболевания ЖКТ в анамнезе.
2. Упорный диспепсический синдром.
3. Печень увеличена, с закругленным краем, гладкой поверхностью.
4. Характерных функциональных критериев нет.
5. УЗИ - признаки жирового гепатоза.
6. Диффузное ожирение гепатоцитов в биоптате печени.
ЦИРРОЗ ПЕЧЕНИ
1. Острый вирусный гепатит, алкоголизм в анамнезе.
2. Внепеченочные сосудистые знаки, гинекомастия.
3.Повышение содержания γ-глобулинов, активности аминотрансфераз, понижение содержания альбуминов, протромбина сыворотки крови.
4. Расширение вен пищевода, желудка, геморроидальных вен.
5. На эхограмме очагово-диффузная акустическая неоднородность тканей, деформация сосудистого рисунка, увеличение диаметра селезеночной вены и размеров селезенки, расширение портальной вены.
6. Активное накопление Аи-198 в селезенке - симптом сканирующей селезенки.
7. Печень - пальпаторно край острый, консистенция плотная, поверхность бугристая.
8. Мультилобулярные узлы до 5мм в диаметре при макронодулярной форме; узлы одинаковых размеров до 1 мм в диаметре и фиброзные септы одинаковой длины при микронодулярной форме, ЦП по данным лапароскопии и прицельной биопсии печени.
Подробно вопросы классификации, диагностических критериев отдельных форм ЦП изложены в «Приложении №2» (см).
ГЕМОХРОМАТОЗ
В начальной стадии характерные клинические симптомы могут отсутствовать.
1. Значительное повышение содержания железа в сыворотке крови, повышенное насыщение железом трансферрина, резкое повышение уровня ферритина сыворотки.
2. Обильное отложение железа, дающего положительную реакцию Перльса в биоптате печени.
Более детально критерии гемохроматоза см. в «Приложении №2».
АМИЛОИДОЗ ПЕЧЕНИ
1. Повышение содержания α2- и γ-глобулинов.
2. Иммунные нарушения: снижение бласттрансформации лимфоцитов и миграционного индекса.
3. Обнаружение амилоида в биоптате печени в виде гомогенных масс, окрашивающихся конго красным в розовый цвет.
4. Печень плотная, малоболезненная, увеличивается на поздней стадии болезни.
ГЕПАТОЛЕНТИКУЛЯРНАЯ ДЕГЕНЕРАЦИЯ (болезнь Вильсона-Коновалова)
1. При абдоминальной форме характерных клинических симптомов нет. Неврологическая симптоматика: дрожательно-ригидный симптом или гиперкинезы, снижение интеллекта.
2. Кольцо Кайзера-Флейшера при осмотре роговицы при помощи щелевой лампы.
3. Снижение содержания сывороточного церулоплазмина. Увеличение содержания не связанной с церулоплазмином меди в сыворотке крови.
4. Повышение содержания меди в биоптате печени.
Более подробно см. «Приложение №2».
РАК ПЕЧЕНИ
1. Боль в области печени, резкое похудание, признаки раковой интоксикации.
2. Быстрое увеличение печени, возможна плотная печень или бугристая.
3. «Немые» зоны различной величины и формы на сканограммах печени.
4. Выявление четких очагов со сниженной, по сравнению с нормальной паренхимой, плотностью при компьютерной томографии.
5. Значительное повышение альфа-фетопротеина.
6. Данные лапароскопи с прицельной биопсией печени.
ДОБРОКАЧЕСТВЕННЫЕ ОПУХОЛИ ПЕЧЕНИ
1. Тень опухоли на контуре печени, высокое стояние диафрагмы при обзорной рентгеноскопии.
2. Округлые, четко очерченные «дефекты» накопления радионуклида на сканограмме печени.
3. Данные лапароскопии и прицельной биопсии при расположении опухоли на участках, доступных осмотру.
4. Данные ангиографии при глубоком расположении опухоли.
НЕПАРАЗИТАРНЫЕ КИСТЫ ПЕЧЕНИ
1. Округлая выпуклость на контуре печени, оттеснение диафрагмы на рентгенограмме.
2. Дефекты накопления радионуклида на сканограмме. На эхограмме сферические или овальные образования с ровными контурами, свободные от эхосигналов.
3. Данные лапароскопии - множественные или солитарные, мелкие, наполненные жидкостью кисты.
4. Возможно сочетание с поликистозом почек, легких.
ЭХИНОКОККОЗ ПЕЧЕНИ
1. Высокое стояние диафрагмы, выбухание купола печени, обызвествление стенок кист на рентгенограмме с пневмоперитонеумом.
2. Дефекты накопления радионуклида на сканограмме. картина, характерная для кистозных образований на эхограмме.
3. Положительные результаты серологических реакций на cпецифические антитела (реакция гемагглютинации и реакция Кацони).
4. Характерные узлы на поверхности печени по данным лапароскопии.
МИЛИАРНЫЙ ТУБУРКУЛЕЗ ПЕЧЕНИ
1. Развивается обычно в конечной стадии туберкулеза легких.
2. Клинические признаки основного процесса.
3. Лихорадка, ознобы, потливость, иногда спленомегалия, желтуха редко.
ТУБЕРКУЛЕЗНЫЙ ГРАНУЛЕМАТОЗ
1. Функциональные пробы печени обычно не изменены.
2. Туберкулезные гранулемы по данным лапароскопии с прицельной биопсией печени.
ТУБЕРКУЛЕЗНЫЙ ХОЛАНГИТ
1. Желтуха связана с внутрипеченочным холестазом.
2. Признаки туберкулезной интоксикации.
ОЧАГОВЫЙ ТУБУРКУЛЕЗ
1. На поверхности увеличенной печени иногда можно пальпировать опухолевидные выпячивания.
2. Общие признаки туберкулезной интоксикации.
3. Прицельная биопсия печени.
СИФИЛИТИЧЕСКОЕ ПОРАЖЕНИЕ ПЕЧЕНИ
ОСТРЫЙ СИФИЛИТИЧЕСКИЙ ГЕПАТИТ
1. Равивается во II стадии сифилиса.
2. Гепатомегалия, желтуха, появляющаяся одновременно с сифилитической сыпью.
3. Клиническая картина сходна с ОВГ.
4. Повышение активности аминотрансфераз, ПТ, ЛДГ, резкое и диспропорциональное повышение активности ЩФ.
5. Выявление в 50% спирохет в биоптатах печени при применении серебрения.
СИФИЛИТИЧЕСКИЕ ГУММЫ, ДОЛЬЧАТАЯ ПЕЧЕНЬ
1. Третичный сифилис.
2. Печень грубо деформирована, с большими узлами на поверхности.
3. Редко наблюдаются желтуха, асцит и портальная гипертензия.
4. Мало измененные функциональные пробы печени.
5. Сифилис в анамнезе, положительная реакция Вассермана в спинномозговой жидкости.
6. Критерий достоверного диагноза - данные лапароскопии.
КОНСТРИКТИВНЫЙ ПЕРИКАРДИТ
1. Травма в области сердца, туберкулез в анамнезе.
2. Одышка при физической нагрузке, протодиастолический тон на верхушке сердца.
3. Повышение венозного давления до 250-300 мм вод.ст.
4. Нормальные размеры сердца с уменьшенной пульсацией при ретгеноскопическом исследовании.
5. Уменьшение амплитуды зубцов на ЭКГ.
6. Уменьшение пульсации контуров сердца по данным рентгенокимографии или эхокардиографии.
«ЗАСТОЙНАЯ» ПЕЧЕНЬ
1 Печень увеличена, край закругленный (в дальнейшем - заостряется по мере нарастания недостаточности кровообращения), консистенция мягкая (по мере прогрессирования НК - плотная), поверхность ровная, болезненность при пальпации.
2 Изменчивость размеров печени, связанная с состоянием центральной гемодинамики и с лечением (в частности, сердечными гликозидами и мочегонными).
3 Желтуха чаще выражена незначительно, повышение билирубина умеренное, чаще за счет связанной фракции.
4 Выраженных отклонений функциональных проб печени не отмечается.
КАРДИАЛЬНЫЙ ЦИРРОЗ ПЕЧЕНИ
1. Наличие заболевания сердца, признаки недостаточности кровообращения.
2. Печень плотная, край острый и неровный, иногда спленомегалия и другие признаки портальной гипертензии.
3. Функциональные пробы изменены умеренно.
4. Течение ЦП чаще латентное, без выраженных обострений.
МИКСОМА ПРАВОГО ПРЕДСЕРДИЯ
(первичная доброкачественная опухоль сердца с локализацией в правом предсердии)
1. Внезапное увеличение печени и быстропрогрессирующая сердечная недостаточность без ревматического анамнеза.
2. Данные эхокардиографии или ангиографии, указывающие на наличие опухоли правого предсердия.
ИНФАРКТ МИОКАРДА ПРАВОГО ЖЕЛУДОЧКА
(протекающий без болевого синдрома - острая коронарная недостаточность с некрозом участка миокарда)
1. Указание в анамнезе на ангинальные боли.
2. Боли в правом подреберье
3. Характерные изменения на ЭКГ.
4. Повышение активности сывороточных ферментов.
БОЛЕЗНЬ БАДДА-КИАРИ
1. Травма живота, туберкулез в анамнезе.
2. Увеличение печени, сопровождающееся болью в правом подреберье, повышением температуры тела: быстрое развитие портальной гипертензии и печеночной недостаточности при острой форме.
3. Сужение печеночных вен по данным ангиографических исследований (нижней каваграфии и веногепатографии).
ГЕПАТОМЕГАЛИЯ ПРИ ЗАБОЛЕВАНИЯХ ОРГАНОВ
КРОВЕТВОРЕНИЯ
Поражение печени при лейкозах обусловлено прежде всего специфической лейкозной инфильтрацией. Существенную роль играет интоксикация, вызванная основным заболеванием и неблагоприятное воздействие на печень цитостатической терапии. Вирусы гепатитов могут быть одной из причин поражения печени при лейкозах.
ОСТРЫЙ ЛЕЙКОЗ
При острых лейкозах гистологически в печени выявляется лейкоз-ная инфильтрация и лейкозные клетки в просвете синусоидов. Лейкозная инфильтрация портальных полей может сочетаться с внутридольковыми скоплениями лейкозных клеток. Фиброз печени локализуется преимущественно в портальных полях и периферических зонах долек и зависит от выраженности лейкозной инфильтрации и продолжительности заболевания.
Различий в частоте гепатомегалии в зависимости от варианта лейкоза выявить не удается, увеличение печени обычно незначительное, и только при остром лимфобластном лейкозе гепатомегалия выражена. Увеличение печени обычно не является прогностически неблагоприятным признаком и не влияет на продолжительность жизни больных. Тяжесть и боль в правом подреберье обычно ощущают больные с быстрым увеличением печени.
Желтуха чаще развивается в терминальной стадии. Биохимически имеет место синдром цитолиза, гипоальбуминемия, гипохолестеринемия, снижение показателей сулемовой пробы. Успешная цитостатическая терапия ведет к улучшению функционального состояния печени у этих больных.
ХРОНИЧЕСКИЕ ЛЕЙКОЗЫ
Клеточный состав лейкозной инфильтрации печени и селезенки определяется видом лейкоза. Фиброзные изменения чаще наблюдаются при эритремии, возможно в связи с нарушением гемодинамики и микроциркуляции, приводящими к тканевой гипоксии и повышенным распадом огромной массы эритроцитов, а также при остеомиелосклерозе. Однако ЦП обычно не развивается.
ХРОНИЧЕСКИЙ МИЕЛОЛЕЙКОЗ
Развивается вследствие малигнизации клетки-предшественницы мие-лопоэза. Доброкачественная (моноклонованя) стадия болезни протекает с лейкоцитозом за счет увеличения числа главным образом зрелых и незрелых гранулоцитов. В терминальной (поликлоновой) стадии могут поражаться другие ростки миелопоэза в клетках которых, как и в клетках гранулоци-тарного ряда, обнаруживается патологическая (Ph-филадельфийская) хромосома из 22-й пары.
Гепатолиенальный синдром относится к характерным признакам хронического миелолейкоза (ХМЛ). Замечено также, что чем больше число лейкоцитов в крови, тем больше размер селезенки. Увеличение ее в развернутом периоде болезни отмечают у 95% больных. Она плотная, безболезненная. Край ее закруглен с легко определяющейся на нем инцизурой -важным дифференциально-диагностическим признаком. Иногда в селезенке образуются инфаркты, и тогда она становится болезненной.
Печень увеличена примерно у половины больных. В печени и селезенке отмечаются очаги экстрамедуллярного кроветворения.
Диагноз обычно не трудно поставить по картине крови, если имеется типичное увеличение числа лейкоцитов (до 100 000 и более) с преобладанием незрелых клеток (миелобласты, миелоциты). Большей частью встречаются все стадии созревания от миелобластов до зрелых нейтрофилов. Диагноз уточняется результатами стернальной пункции с исследованием костного мозга.
МИЕЛОФИБРОЗ И ОСТЕОМИЕЛОСКЛЕРОЗ
Это заболевание относится к ретикулезам. Разрастаются клетки, относящиеся к элементам активной мезенхимы, из которой в эмбриональном периоде образуются кроветворные клетки, а в постнатальном - клетки ретикуло-гистиоцитарной системы. Это объяснение позволяет представить клиническую симптоматику заболевания как следствие разрастания клеток одного типа. Так, для остеомиелоретикулосклероза типично разрастание как различных кровяных клеток ( эритроцитов, лейкоцитов, тромбоцитов ), так и элементов ретикуло-гистиоцитарной системы (фиброз). В большинстве случаев имеет место миелоидная метаплазия селезенки, печени. Хроническое течение болезни с постепенно нарастающей спленомегалией периодически сопровождается острой болью в животе. В основе ее лежат повторные инфаркты селезенки. Характерны нарастающая портальная гипертен-зия, боли в конечностях, ЖКТ-кровотечения.
В отличие от лейкоза, костный мозг апластический. Невозможность получить костный мозг при стернальной пункции - весьма характерный признак миелофиброза, причем нередко в нем обнаруживаются своеобразные гигантские клетки (мегакариобласты). Ренгенологически иногда удается выявить миелосклероз, не поражаются обычно только кости черепа. При биопсии кости получают решающие диагностические данные.
ЛИМФОГРАНУЛЕМАТОЗ
Может проявляться гепатомегалией, желтухой, асцитом. Чаще гепа-томегалия умеренная, на фоне лихорадки, увеличения лимфатических узлов. Поражение печени обычно сочетается со специфичесим поражением селезенки. При формах с изолированным поражением гепатолиенальной системы начало болезни внезапное - с лихорадки, увеличения печени, выраженной желтухи и похудания. Желтуха часто сочетается с кожным зудом. Желтуха чаще всего обусловлена внутри- или внепеченочным холестазом вследствие перипортальной и портальной инфильтрации лимфоцитами, эо-зинофилами, плазматическим клетками, а также многоядерными гигантскими клетками Березовского-Штернберга и сдавления внепеченочных желчных протоков увеличенными лимфатическими узлами.
БОЛЕЗНЬ ВАЛЬДЕНСТРЕМА
Злокачественные опухоли, происходящие из В-лимфоцитов, способны синтезировать и секретировать в окружающую среду иммуноглобулины в виде целых молекул или их фрагментов (легких или тяжелых цепей). В крови таких больных, как правило, обнаруживают моноклоновые иммуноглобулины. К числу таких болезней относится и макроглобулинемия Вальден-стрема. В основе ее лежит пролиферация лимфоидно-плазмоцитарных клеток первоначально в костном мозге, а позднее в селезенке, печени и других органах.
Клетки этой опухоли чаще всего продуцируют IgM. В костном мозге обычно отмечается преобладание лимфоидных клеточных форм и увеличение тучных тканевых клеток. СОЭ чрезвычайно резко ускорена.
Электрофоретически узкие высокие зубцы в области бета- и гамма-глобулинов (М-градиент). В крови здорового человека на долю макроглобулинов приходится не более 15% всех глобулинов. В крови больного макроглобу-линемией их содержание достигает 20-40%. Макроглобулинемия Вальдестрема включена в настоящий раздел только потому, что увеличение печени и селезенки при ней наблюдается несколько чаще, чем поражение лимфатических узлов. Предположительный диагноз болезни должен быть подтвержден результатами исследования препаратов костного мозга.
ПРИЛОЖЕНИЕ № 1 «ХРОНИЧЕСКИЕ ГЕПАТИТЫ»
Конец XX столетия ознаменовался возрастающим интересом к проблеме хронических гепатитов. Согласно данным ВОЗ, в разных странах мира только вирусными гепатитами инфицировано или перенесли в прошлом до 2 млрд. человек. Важно отметить, что данная патология нередко носит прогрессирующий характер, поражаются лица наиболее трудоспособного возраста, часты тяжелые осложнения с исходом в цирроз печени (ЦП) и гепатоцеллюлярную карциному (ГЦК). В настоящее время существуют две классификации хронических гепатитов (ХГ). Во-первых, Международная классификация болезней 10 пересмотра, согласно которой ХГ классифицированы в следующих рубриках:
В 18 Хронический вирусный гепатит
В 18.0 Хронический вирусный гепатит В с дельта-антигеном (вирусом)
В 18.1 Хронический вирусный гепатит В без дельта-антигена (вируса)
В 18.2 Хронический вирусный гепатит С
К 70 Алкогольная болезнь печени
К70.1 Алкогольный гепатит
К 73 Хронические гепатиты
К73.0 Хронический персистирующий гепатит (ХПГ)
К73.1 Хронический лобулярный гепатит (ХЛГ)
К73.2 Хронический активный гепатит (ХАГ)
К73.9 Хронический гепатит, неуточненный
Разделение ХГ на ХАГ, ХЛГ и ХПГ основано на морфологических критериях. Так, ХАГ соответствует перипортальный воспалительный процесс с лимфоцитарно-гистиоцитарной инфильтрацией, развитием мелкоочагового ступенчатого некроза. Важнейшим критерием является нарушение целостности пограничной пластинки, ее прорыв, сопровождающийся распространением инфильтрации вглубь печеночной дольки с нарушением ее архитектоники, возникновением деструктивных изменений в значительной части гепатоцитов. Морфологическая характеристика ХПГ ограничивается воспалительной круглоклеточной инфильтрацией портальных трактов при полном отсутствии признаков повреждения пограничной пластинки и развития ступенчатого некроза. Сохраняется структура печеночных долек. ХЛГ по своей структуре - дольковый гепатит с воспалительной инфильтрацией не по ходу портальных полей, а внутри долек.
Международным конгрессом гастроэнтерологов, состоявшимся в Лос-Анджелесе в 1994 году, предложена новая классификация, которая учитывает следующие основные критерии: этиологию, патогенез, степень активности и стадию хронизации заболевания.
Сущность ХГ - это группа болезней печени, вызываемая несколькими причинами, характеризуется различной степенью гепатоцеллюлярного некроза и воспаления. Понятие "ХГ" обусловлено длительностью заболевания: условная граница хронизации составляет 6 мес. Однако эксперты справедливо пишут, что во многих случаях, особенно при аутоиммунном гепатите (АГ), диагноз ХГ может быть поставлен ранее 6 месяцев.
Следует отметить, что среди этиологических факторов отсутствует алкогольный гепатит, он классифицирован только в рамках "Алкогольной болезни печени" по МКБ-10. По мнению ряда авторов, его исключение из новой (1994г.) классификации не вполне обосновано (Серов В., Лапиш К., 1995, Takase S. et all.).
ЭТИОЛОГИЧЕСКИЙ ФАКТОР
В новой классификации выделяют 4 вида гепатита: аутоиммунный, вирусный, лекарственный, криптогенный.
хронический аутоиммунный гепатит
АГ включен в группу этиологических видов гепатита, выделен на основании особенностей патогенеза, а не этиологии - ведь факторы, снижающие иммунологическую толерантность ткани печени и "запускающие" аутоиммунный процесс при этом заболевании, неизвестны. Поэтому при АГ должны отсутствовать иммунологические (серологические) признаки гепатитов В, С, D. Диагностика АГ до сих пор остается трудной, чем объясняется высокая частота ошибок в распознавании данного заболевания (до 33%) или позднее установление диагноза (в 30% случаев). Постановка диагноза АГ должна базироваться главным образом на патогенетических механизмах. Основными диагностическими критериями являются сочетание тяжелого поражения печени с нарушениями в иммунной системе:
- наличие в крови специфических аутоантител (в титре не менее 1:40),
- увеличение СОЭ (более 20мм/ч), гипергаммаглобулинемии более 18
г/л за счет IgG, типичных антигенов гистосовместимости (В8ДЖЗ, DR4),
- характерная морфологическая картина печени: инфильтрация моно-
нуклеарными и плазматическими клетками портальных трактов с распро
странением на дольку,
- ступенчатые или мостовидные некрозы, соединительнотканные тя
жи по ходу портальных трактов, регенерация с образованием розеток,
- положительный эффект применения кортикостероидов и иммуно-
супрессивной терапии,
- отсутствие этиологического фактора.
Среди аутоантител выделяют: антинуклеарные антитела (ANA), антитела к микросомам печени и почек (LKM) с подтипами LKM-1, LKM-2, LKM-3, антитела к гладкомышечным клеткам (SMA), растворимому печеночному антигену (SLA), структурам печени и поджелудочной железы (LP), плазматической мембране гепатоцитов (LM), компонентам ге-патоцитов (LC), печеночному лектину. Антимитохондриальные антитела (АМА) при АГ встречаются редко или отсутствуют.
Выделяют три типа АГ:
1 тип - характерно наличие ANA и (или) SMA,
2 тип - характерно наличие анти-LKM-l, направленных против ци-
тохрома Р-450 II D6 и (или) антител к компонентам гепатоцитов LC-1 ти-
па,
3 тип - наличие SLA, отсутствие ANA и анти-LKM.
С иммунопатологическими реакциями в известной степени связаны и внепеченочные, или системные, проявления, характерные для АГ. К ним относятся:
- эндокринные расстройства (аменорея, кушингоидный синдром, ти-
реотоксикоз, гипотиреоз, тиреоидит Хашимото, сахарный диабет),
- кожные изменения (акне, стрии, не связанные с приемом ГКС, кра-
пивница, гиперемия лица в виде "бабочки", напоминающей красную
волчанку, элементы красного плоского лишая и кожной порфирии, папу-
лезный акродерматит, малакоплакия, узловатая и мультиформная эритема,
кожный некротизирующий васкулит),
- гематологические (иммунные цитопении, смешанная криоглобули-
немия, неходжкинская В-лимфома, макроглобулинемия Вальденстрема,
аутоиммунная гемолитическая анемия, апластическая анемия),
- поражение слюнных желез и глаз (лимфоцитарный сиалоаденит,
язвы роговицы, увеит, синдром Шегрена - сухость слизистых оболочек
полости рта в сочетании с кератоконьюнктивитом и полиартритом),
- нейромышечные и суставные ( миопатический синдром, перифери-
ческая полинейропатия, синдром Гиллена-Барре, артриты, артралгии),
- почечные (гломерулонефрит),
- сердечные (миокардит, гипертрофическая кардиомиопатия),
- легочные (фиброзирующий альвеолит, интерстициальный легочной
фиброз, легочной васкулит),
- узелковый периартериит (системный некротизирующий васкулит),
- CRST - синдром,
- антифосфолипидый синдром,
- дерматомиозит.
ХРОНИЧЕСКИЙ ВИРУСНЫЙ ГЕПАТИТ
Современный этап называют " золотой эрой" изучения вирусных гепатитов (ВГ). Открыты возбудители ВГ - А, В, С, D, Е. Однако использование новых методов исследования показало, что "гепатитный алфавит" еще далеко не исчерпан. Хронизация процесса регистрируется исключительно при сывороточных гепатитах - В, С, D. В последние годы наблюдается достаточно высокий рост доли вирусных гепатитов в структуре заболеваний органов пищеварения. Так, проведенный подобный анализ в научно-практическом Центре гастроэнтерологии (Областная клиническая больница, г.Томск) показал, что ХГ вирусной этиологии составляют 64% среди всех заболеваний инфекционной и паразитарной этиологии в 1999г. против 39% в 1997г. Причем, с учетом напряженной эпидемиологической обстановки и достаточно широкого распространения гепатотропной вирусной инфекции, безусловно, можно прогнозировать неуклонный рост этих цифр.
ХРОНИЧЕСКИЙ ВИРУСНЫЙ ГЕПАТИТ В (ХГВ)
Первые сведения о возбудителе гепатита В (ГВ) были получены B.S. Blumberg в 1965 г. Из крови аборигена Австралии был выделен ранее не определявшийся белок, ставший известным под названием "австралийского антигена". А в 1970 г. D.Dane впервые описал полный вирион вируса ГВ, получивший наименование частиц Дейна.
Вирус ГВ (HBV) содержит дезоксирибонуклеиновую кислоту (ДНК). HBV-ДНК представляет кольцевую молекулу, состоящую из двух цепей, одна из которых - плюс-цепь на 1/3 короче другой - минус-цепи. Плюс-цепь постоянно достраивается с помощью фермента ДНК-полимеразы. Обязательным компонентом репликационного цикла HBV является механизм обратной транскрипции прегеномной РНК в минус-цепь, поскольку РНК-полимераза активно участвует в достраивании плюс-цепи. Достроенные вирионы содержат полноценную ДНК, определяющую способность HBV к репликации, что характеризует их инфекционность.
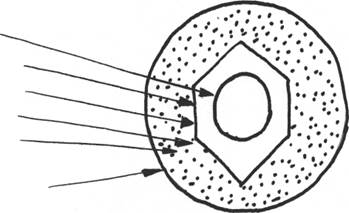
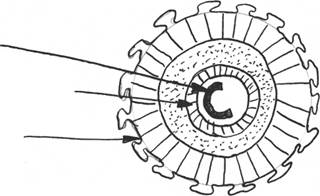
Внутреннее образование вириона представлено нуклеокапсидом-сердцевиной (core). В нем расположены основные вирусные белки-антигены, детерминирующие репликативную активность HBV. Это внутренний или сердцевинный антиген - HBcore Ag (HBcAg) и близкий к нему HBprecoreAg, получивший название HBeAg. В структуре вируса HBeAg локализуется рядом с HBcAg, представляя секретируемую растворимую его часть. Допускают существование двух антигенных вариантов - HBeAg-1 и HBeAg-2, отличающихся по степени связи с HBcAg. В отличие от HBcAg, обнаруживаемого исключительно в биоптатах печени в ядрах гепа-тоцитов, HBeAg циркулирует в крови. Индикация HBeAg в крови имеет первостепенное значение, косвенно подтверждая наличие HBcAg в ткани печени - в ядрах гепатоцитов.
ДНК
HBcAg
HВeAg
Pre-Sl
Pre-S2
HbsAg
Рис.1. Схема структуры вируса гепатита В
В сердцевине вируса расположен еще один антиген, условно обозначенный как HBxAg, что соответствует пока еще недостаточной информации о его значении.
Белок внешней облочки HBV представляет "поверхностный" (superficialis) антиген - HBsAg, его и именовали поначалу "австралийским". Содержание HBsAg в крови больных варьирует в широких пределах от очень небольших величин (1-10 нг в 1 мл) до огромных концентраций порядка 500 мкг/мл. На наружной оболочке HBV в зоне, предшествующей области S-антигена расположены белки pre-S - pre-Sl, pre-S2, играющие важную роль в механизме взаимодействия HBV с печеночными клетками.
В организме больного ГВ ко всем вирусным антигенам вырабатываются антитела: анти-НВс, анти-HBs, анти-НВе, анти-pre-Sl, анти-рге-82, анти-НВх. Все антигены и антитела к ним по своей совокупности представляют комплекс специфических маркеров HBV, индикация которых имеет разное по информативности диагностическое, прогностическое и эпидемиологическое значение.
HBV высокоустойчив, сохраняясь в условиях комнатной температуры 3 мес, в холодильнике - 6 мес, в замороженном виде - 15-20 лет, в высушенной плазме - 25 лет. Кипячение обеспечивает гарантированную инактивацию вируса только при условии достаточной продолжительности (более 30 мин.). Вирус противостоит действию практически всех дезинфицирующих средств и консервантов крови. Так, в 1-2% растворе хлорамина инактивация наступает через 2 часа, в 1,5% растворе формалина - только при 7-дневной экспозиции. Вирус устойчив к лиофилизации, воздействию эфира, ультрафиолетовому облучению.
ГВ является антропонозной нетрансмиссивной кровяной инфекцией. Его особенностью является наличие множественных - естественных и искусственных путей передачи, разнообразие источников инфекции.
Потенциальные источники HBV -инфекции:
- больные хроническими формами ГВ;
- доноры и реципиенты крови, гемопрепаратов, органов, спермы;
- наркоманы с внутривенным введением наркотиков;
- медицинские работники - хирурги, стоматологи, представители лабораторной службы;
- больные и персонал отделений гемодиализа, реанимации, болезней
крови, онкологических и туберкулезных стационаров;
- больные хроническими заболеваниями печени неустановленной
этиологии;
- гомосексуалисты;
- лица, ведущие неупорядоченную половую жизнь при незащищен-
ном сексе;
- дети, рожденные от инфицированных матерей;
- больные и персонал учреждений для умственно отсталых;
- ВИЧ/СПИД-инфицированные лица;
- лица, приехавшие из гиперэндемичных регионов (перселенцы, беженцы, временно проживавшие).
Заражение ГВ происходит при инокуляции очень малых обьемов крови - 0,0005мл. Инфекционность крови может сохраниться при ее разведении в 8-10 раз. Для сравнения - инфицирующая доза крови при ВИЧ/СПИД-инфекции на несколько порядков выше: 0,1 мл. Соответственно, контагиозность ГВ, по крайней мере, в 100 раз выше, чем при ВИЧ-инфекции.
Пути передачи ГВ существуют искусственные (артифициальные) - в результате парентеральных медицинских (лечебных и диагностических), а также немедицинских иньекций (наркомания). Естественные неартифици-альные пути передачи HBV-инфекции реализуются перинатальным заражением, половым путем, а также в результате так называемых гемоперкутант-ных контактов (порезы, трещины на губах, ссадины, кровоточивость десен). Важную группу риска представляют медицинские работники, что подтверждает высокую долю горизонтального пути инфицировния HBV. При анализе профессиональных заражений работников здравоохранения было установлено, что факторами передачи могут явиться брызги инфицированной слюны, попадающие на поврежденные участки кожи.Статистика инфицированности вирусными гепатитами среди медперсонала показывает, что наиболее неблагополучны в этом отношении отделения гемодиализа, гематологии, лабораторная служба. Проведенные нами исследования на базе научно-практического Центра гастроэнтерологии Областной клинической больницы (г.Томск, 1998г.) подтверждают высокую частоту выявления маркеров вирусных гепатитов именно в данных отделениях. Так в отделении гемодиализа около 38% медперсонала являются больными ХГ или носителями вирусов гепатита, причем наблюдается их неуклонный рост.
После острого гепатита В хронизация наступает в 5-10% случаев, хотя в последние годы называется гораздо более низкий процент хрониза-ции(1%).
Патогенетической особенностью ГВ является отсутствие прямого ци-топатического эффекта вируса, его повреждющее действие иммуноопосре-довано. В основе патоморфологических изменений при ГВ, как и других вирусных гепатитах, лежит цитолиз гепатоцитов, инициирующий развитие прогрессирующего некротического процесса. Развитие цитолиза связано с активацией прооксидантных и, наоборот, угнетением антиоксидантных систем клетки, что сопровождается накоплением свободных радикалов, усиливается перекисное окисление липидов (ПОЛ). В гидрофобном барьере биомембран появляются "дыры", определяющие повышение их проницаемости, а затем этот процесс распространяется и на внутриклеточные органеллы. Особо важное значение приобретает повреждение мембран ли-зосом, из которых выходят мощные протеолитические ферменты - гидролазы, что в значительной степени определяет развитие некроза гепатоцитов.
Репликация отдельных компонентов HBV происходит раздельно: нуклеокапсида - в ядрах гепатоцитов, белков внешней оболочки (HBsAg) -в цитоплазме. Конечный этап состоит в сборке полного вириона. При этом избыток HBsAg, не использованного для сборки вириона, через межклеточные пространства попадает в кровь. Сборка вириона в гепатоцитах заканчивается презентацией его растворимого нуклеокапсидного антигена HBeAg на мембране гепатоцитов, где происходит его "узнавание" иммуноцитами. Циркулирующий HBeAg подавляет оба звена иммунитета. Клеточный - путем снижения продукции гамма-интерферона, играющего важную пусковую роль в механизме "узнавания" антигенов вируса Т-лимфоцитами, гуморальное - подавлением антителообразования В-лимфоцитами.
Важным открытием современного этапа явилось установление возможности внепеченочной репликации HBV, в частности, в клетках костного мозга, крови, лимфатических узлов и селезенки. Репликация HBV в мо-нонуклеарных клетках крови, которые не контролируются иммуноцитами, способствует еще одному пути "ускользания" вируса от иммунного надзора. Важно отметить существование мутантных штаммов HBV, возникающих в основном у больных ХГ и фульминантным гепатитом. При длительном нахождении HBV в гепатоцитах происходит внедрение - интеграция его генетического аппарата с геномом клетки, что делает вирус недосягаемым для иммунного контроля и является одним из основных механизмов хронизации HBV-инфекции, а равно и потенциальной угрозы малигнизации.
Согласно новым рекомендациям, при ХГВ следует разграничивать два варианта - с высокой и низкой репликативной активностью вируса, а критерий их разграничения - индикация HBeAg. Сохранение циркуляции HBeAg в крови спустя 6 мес. и больше от начала болезни подтверждает развитие ХГВ с высокой репликативной активностью (HBeAg-позитивный ХГВ). Наступление к этому времени сероконверсии с прекращением циркуляции HBeAg и появлением анти-НВе при сохранении персистирующей HBs-антигенемии характеризует развитие ХГВ с низкой репликативной активностью (HBeAg-негативный ХГВ). Причем, при последнем варианте предусмотрено его дополнительное разграничение в зависимости от уровня АлАТ. Нормальные или близкие к норме показатели АлАТ соответствуют персистирующему течению HBV-инфекции с интеграцией вируса с геномом гепатоцита без активного иммунного цитолиза (интегративный тип ХГВ).
Сохранение высокого уровня АлАТ при отсутствии признаков активной репликации HBV требует исключения присоединения других вирусов гепатотропного действия (интегративный микст-гепатит В+С, B+D, В+А).
Специфическими маркерами HBV при хроническом ГВ являются:
1. Для ХГВ с активной репликацией ( ХГВ, HBeAg-позитивный вари
ант, репликативная форма) - это обнаружение в крови HBV-ДНК (высокое
содержание), HBeAg, HBsAg, анти-HBcIgM, анти-HBcor сумм., антитела к
HBV-полимеразе, повышение циркулирующих иммунных комплексов
типа HBeAg - анти-НВе.
2. Для ХГВ без активной репликации (ХГВ, HBeAg-негативный вари
ант, интегративная форма) - это обнаружение в крови HBV-ДНК (очень
низкое содержание, в ремиссию чаще отсутствует), HBsAg, анти-НВе в
низких титрах без тенденции к нарастанию, анти-HBcIgG. Анти-HbcIgM
чаще отсутствуют или выявляются в небольших количествах.
Важно уточнить, что отсутствие в крови HBeAg может соответствовать штамму HBV, лишенному способности синтезировать HbeAg (HBVe-штамм). К особенностям ХГВ, вызванного HBVe-, следует отнести: отсутствие клинического улучшения при наступлении сероконверсии HBeAg-анти-НВе, сохранение повышенной активности АлАТ при исключении микст-гепатита, обнаружение в крови HBV-ДНК, нередко в высокой концентрации. Такой вариант ХГВ может быть обозначен как HBeAg-негативный гепатит, протекающий с сохранением репликативной активности. Отсутствие HbeAg у мутантного типа объясняется наличием мутации pre-core-региона, что и приводит к нарушению продукции данного антигена (Brunetto et al., 1989).
Для обоих типов вируса («дикого» и «мутантного») общими маркерами служат HBsAg, HBcorAglgG, HBV ДНК.
Маркеры репликации «дикого» и «мутантного» типов HBV
1. "Дикий "тип: HBsAg+, HBeAg+, HBeAb-, HBcorIgG+, HBV ДНК.
2. «Мутантный» тип: HBsAg+, HBeAg-, HBeAb+, HBcorIgG+, HBV ДНК.
КЛИНИЧЕСКАЯ ХАРАКТЕРИСТИКА
Большей частью ХГВ имеет в основном сглаженное малосимптом-ное течение. У большинства больных с несомненными клинико-лабораторными и морфологическими признаками ХГВ вообще нет указаний на перенесенный когда-либо в прошлом острый гепатит. Это вполне объяснимо с учетом угрозы развития хронизации исключительно после легких, стертых желтушных и чаще безжелтушных форм острой фазы болезни, в значительной части остающихся нераспознанными.
В основном ХГВ протекает без желтухи, другие проявления его тоже не столь манифестны, что определяет ХГВ как «немой» гепатит. Первые проявления соответствуют жалобам больных на быструю утомляемость, ухудшение общего самочувствия, слабость, головные боли, снижение толерантности к физическим нагрузкам, чувство усталости уже в утренние часы. Появление и прогрессирование этих симптомов соответствует постепенному развитию печеночной недостаточности.
С относительно меньшим постоянством присоединяются диспепсические расстройства, редко бывает болевой абдоминальный синдром. Может иметь место субфебрилитет. Оценка астено-вегетативных и диспепсических расстройств, установление их гепатогенной природы облегчается при выявлении увеличения печени, причем большей частью незначительное. Пальпаторно имеется ее уплотнение, что подтверждает известную давность болезни.
Не часто гепатомегалия сопровождается увеличением селезенки, что характеризует генерализованную реакцию ретикулоэндотелиальной системы. Гепатоспленомегалия иногда протекает с увеличением лимфатических узлов. Признаки гиперспленизма наблюдаются редко, преимущественно при тяжелом течении болезни по типу ХАГ-цирроза.
Анемия и тромбоцитопения, наряду с гиперспленизмом, могут быть обусловлены геморрагическим синдромом. Последний связан с угнетением белковосинтезирующей функции печени и уменьшением выработки факторов свертывания, прежде всего прокоагулянтов (протромбина, проконвер-тина, проакцелерина). Снижение коагулогического потенциала крови сопровождается мелкими кожными кровоизлияниями, ограниченными пете-хиальными высыпаниями, кровоточивостью десен, транзиторными носовыми кровотечениями. Развивающаяся анемия носит апластический характер, что подтверждается невысокими показателями содержания ретикулоцитов.
Существенно при ХГВ и развитие внепеченочных изменений, но их выраженность и спектр существенно меньше, чем при аутоиммунном гепатите (см. "Аутоиммунный гепатит").
Хроническое носительство HBsAg . Это сугубо условное наименование, которым принято обозначать субклинические и инаппарантные формы ХГВ. Чаще соответствует клинически латентной интегративной форме хронической HBV-инфекции. Ее характеризуют не как носительство отдельного HBsAg, а полного вириона HBV. Наряду с этим, следует отметить возможность и носительства именно HBsAg в результате его избыточного синтеза в гепатоцитах. Формирование хронического носительства HbsAg обусловлено прежде всего неполноценностью иммунного ответа и оно встречается несравненно чаще клинически манифестных форм ХГВ. Причем установлены четкие половые различия - преимущественная частота носительства HBsAg среди мужчин. Это связано с генетически детерминированным у них ослабленным иммунным ответом.
Диагностика хронического носительства
основывается на выявлении длительной HBs-антигенемии (не менее 6 мес.) при полном отсутствии каких-либо клинических проявлений HBV-инфекции. У носителей HBsAg в крови часто обнаруживаются антитела к HBcAg класса G, которые могут сохраняться в течение неопределеноого времени. Установлена возможность спонтанного исчезновения HBsAg. Морфологическая диагностика ХГВ более важна для определения активности процесса в печени, а не установления этиологической принадлежности гепатита, определяемую исключительно серологически. По морфологии нельзя судить и о репликатив-ной активности HBV. В то же время имеется ряд неспецифических гистологических критериев, которые с большой долей вероятности могут быть отнесены к HBV-инфекции. Это совокупность следующих изменений в биоптатах печени:
- гидропическая дистрофия гепатоцитов,
- ацидофильные тельца Каунсильмена,
- лимфогистиоцитарная инфильтрация,
- фиброз портальных трактов,
- "матовостекловидные" гепатоциты (маркер HBsAg),
- "песочные" ядра (маркер HBcAg).
Исходы ХГВ.
ХГВ должен рассматриваться как потенциально обратимый. Но при репликативном и интегративном типе ХГВ может развиваться ЦП, а также гепатоцеллюлярная карцинома. Последняя представляет первичную неметастатическую опухоль, происходящую из печеночных клеток, и вместе с холангиокарциномой (опухолью, происходящей из клеток внутрипеченочных желчных протоков) и гепатохолангиомой (опухолью смешанного происхождения) описывается под объединяющим названием первичного рака печени. Считается, что вирусная ДНК, не обладая прямым онкогенным действием, в условиях многолетней персистенции в гепатоцитах, активирует клеточные онкогены. Это, с одной стороны, приводит к усиленной пролиферации, а с другой - стимулирует апоптоз, т.е. "программирует" ускоренную гибель клеток. Таким образом, многолетнюю интеграцию HBV с геномом гепатоцита рассматривают как "потенциальный предвестник первичного рака печени".
ХРОНИЧЕСКИЙ ВИРУСНЫЙ ГЕПАТИТ D (ХГD)
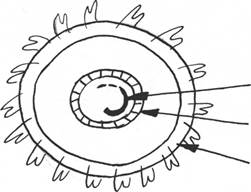
Вирус гепатита дельта (HDV) является уникальным, совершенно не похожим на все известные вирусы человека. HDV не имеет ни внешней, ни внутренней оболочки. Его структура состоит из генома и белка, кодирующего синтез специфического антигена - HDAg. Геном представляет однони-тевую РНК очень мелких размеров (Рис.2.).
Важнейшей особенностью HDV является его облигатная зависимость от наличия вспомогательного вируса, т.к. только при этом условии становится возможной репликация HDV. Роль вируса-помощника играет HBV, во внешнюю оболочку которого, состоящую из HBsAg и встраивается HDV.
РНК HDV
core Ag
HbsAg
Рис.2. Схема структуры вируса гепатита D.
Заражение обоими вирусами может произойти одновременно, что соответствует развитию HDV/HBV-коинфекции. Другим вариантом является внедрение HDV в ранее HBV-инфицированные гепатоциты, в основном у хронических носителей HBsAg. Это называют HDV/HBV-суперинфекцией.
Эпидемиологическая характеристика (распространенность, источники инфекции и пути передачи) ГВ и TD достаточно близка. Особенностью является то, что при гемотрансфузионном пути заражения относительно чаще возникает сочетанное заражение HBV и HDV. Кроме того, больные отделения гемодиализа - одна из основных групп высокого риска заражения ГВ, относительно мало поражены HDV-инфекцией. За последние годы резко возросла доля HDV-инфицированных наркоманов с внутривенным введением наркотических средств. При HDV-инфекции отмечено относительно меньшее значение полового пути передачи.
Патогенетической особенностью ГВ является развитие микст-гепатита, возникновение поражения печени под влиянием двух гепато-тропных вирусов - HBV и HDV. При первичной HDV/HBV-коинфекции ак-тивная репликация HDV приводит к подавлению репродукции HBV. Содержание HBV-ДНК уменьшается, или полностью исчезает из крови, прекращается циркуляция HBeAg, падает содержание или исчезает HBsAg. Подавление репликации HBV чаще временное, но может быть и стабильным.
В случае же HDV/HBV-суперинфекции имеется прогрессирующее течение болезни с развитием фульминантного гепатита и ЦП, что обусловлено прежде всего HDV. Ниже приведены критерии разграничения сочетания двух инфекций:
1. Маркеры HDV / HBV -коинфекции:
наличие в сыворотке крови HBV-ДНК, HBeAg, анти-НВс IgM, HBsAg, HDV-PHK, анти-HDV IgM, часто тяжелое течение, частота хронизации соответствует частоте хронизации HBV.
2. Маркеры HDV / HBV -суперинфекции:
HBsAg, анти-HBcor сумм., HDV-PHK, анти-HDV IgM, быстрое прогрессирование процесса в ХГ и ЦП, малая эффективность противовирусной терапии.
ХГ является при HDV/HBV-суперинфекции основной формой болезни. Клинически манифестные формы характеризуются прогрессирующим течением, близким к хроническому репликативному ГВ. В начальной стадии преобладают субъективные расстройства. Хронические носители HBsAg, ранее вполне компенсированные, начинают испытывать быструю утомляемость, слабость. Резко снижается трудоспособность, половая активность, у женщин появляются расстройства менструального цикла. Наблюдаются диспепсические нарушения, беспричинное похудание. Характерно более постоянное сочетание гепатомегалии с увеличением селезенки с признаками гиперспленизма. Известным отличием XГD от ХГВ является отсутствие внепеченочной репликации вируса в моноцитах и других клетках.
Основной особенностью XГD является его циррозогенность. Угроза малигнизации при XГD относительно меньшая, чем при ГВ.
ХРОНИЧЕСКИЙ ГЕПАТИТ С (ХГС)
Вирус гепатита С (HCV) обладает наиболее высоким хрониогенным потенциалом. Частота хронизации после острого гепатита С составляет 75-85%. Именно HCV-инфекция является основной причиной формирования всей группы хронических болезней печени - ХГ, ЦП, гепатокарциномы.
HCV остается загадочным вирусом, его называют "ласковым убийцей". Не выяснен до конца патогенез гепатита С (ГС), который объяснил бы возможность летальных исходов спустя четверть века торпидного течения. Спорна даже сама возможность выздоровления больных ГС.
| РНК |
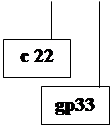
HCV представляет мелкий, покрытый оболочной сферический вирус с однонитевой линейной РНК (Рис.3.).
| ||||||||||||||
Рис.3. Схема структуры вируса гепатита С.
Геном вируса кодирует струтурные и 6 неструктурных белков. К структурным, наряду с белками сердцевины (C-core protein), относят и гликопротеины облочки (E-envelope protein 1 и 2). Неструктурную область представляет комплекс белков с ферментативной активностью. Из них ключевая роль в репликации HCV принадлежит NS3- протеиназе - ферменту, катализирующему заключительный этап синтеза вирусного полипротеина.
Существенной особенностью HCV является его генетическая гетерогенность. Для целей клинической практики достаточно разграничивать 5 генотипов HCV: la, lb, 2а, 2Ь и За.


|
|
|
|

 NS2
NS2
|
 | |||||||
 |  | 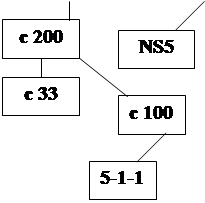 | |||||
|
|
|
|
Рис.4. Схема организации генома вируса гепатита С.
Пути передачи и источники инфекции аналогичны таковым при ГВ. При ГС меньшее значение имеет вертикальный путь передачи от инфицированных матерей. У значительного числа больных ХГС нет никакого парентерального анамнеза, вирус обнаруживается не только в крови, но и слюне, моче и даже слезной жидкости, хотя и в очень малых концентрацях.
Патогенетической основой ГС является его проникновение в гепато-циты, где и происходит репликация. У HCV имеется также внепеченоч-ная репликация, в частности, в мононуклеарах крови. Он обладает пря-мым цитопатическим действием, вызывающим цитолиз. Но антигены HCV обладают существенно меньшей иммуногенностью и не индуцируют, по крайней мере, выраженных иммунопатологических реакций. Вирус спосо-бен вызывать "Т-клеточную анергию", что в значительной мере способст-вует хронизации процесса, в том числе имеет значение апоптоз вирусспе-цифических Т-клеток. Гуморальный иммунный ответ при ГС также сла-бее, о чем говорит менее интенсивное антителообразование. Преимущест-венные темпы хронизации ГС - у алкоголиков и злостных курильщиков. Возможна к тому же и реинфекция. В основе "ускользания" HCV из-под иммунного надзора основная роль принадлежит уникальной способности вируса изменять антигенную структуру, многократно обновляющуюся в течение одной минуты.
Морфологические особенности ХГС (хотя и не патогномоничные) преставлены сочетанием изменений:
- очаги некроза гепатоцитов,
- сочетание жировой и гидропической дистрофии гепатоцитов,
- ацидофильные тельца Каунсильмена,
- лимфоидные фолликулы в портальных полях и интралобулярно,
- активация синусоидальных клеток,
- "цепочки" лимфоцитов в синусоидах,
- поражение желчных протоков, пролиферация дуктул.
Отличительной особенностью ХГС является малосимптомное, латентное течение, большей частью остающееся нераспознанным, вместе с тем постепенно прогрессирующее и в дальнейшем бурно финиширующее с развитием ЦП и гепатоцеллюлярной карциномы. В многолетнем течении HCV-инфекции выделяют три последовательные фазы: острую, латентную и реактивации. Причем в острую фазу иммунный контроль частично сохранен, чему соответствует пусть редкая, но все же возможность выздоровления.
В латентную фазу остаточный иммунитет уже недостаточен для элиминации вируса. Эта фаза соответствует хроническому перси-стирующему течению HCV-инфекции с сохранением вирусемии при полном или почти полном отсутствии клинических проявлений. Ее условно характеризуют как хроническое носительство HCV. Важно отметить существенные отличия от хронического носительства при HBV. Латентная фаза ГС является предстадией фазы реактивации инфекционного процесса с развитием клинически манифестного ХГС. При HBV-инфекции хроническое носительство HBsAg, при отсутствии HDV-суперинфекции, крайне редко является предстадией клинически манифестного ХГВ.
Латентная фаза
может продолжаться многие годы, до 15-20 лет, при этом инфицированные лица считают себя здоровыми. Имеется небольшой астенический синдром, умеренная гепатомегалия, уплотненная консистенция печени, селезенка не увеличена. Может быть 1,5-2 кратное повышение активности АлАТ, у 1/3 больных - нормальные значения. HCV-PHK обнаруживается непостоянно, в низких концентрациях. Положительная реакция на HCV-PHK в латентную фазу подтверждает диагноз, однако не обязательно характеризует репликативную активность вируса. В крови закономерно присутствуют анти-HCV NS3-4, анти-HCV IgG. Анти-HCV класса IgM, как правило, отсутствуют. Выделяют инаппарантную форму (АлАТ - норма) и субклиническую (АлАТ до 3-х норм).
Наступление фазы реактивации
знаменует практически полную утрату иммунитета, что приводит к всплеску активности HCV-инфекции, основной клинической формой которой является ХГ. ХГ дебютирует нередко гиперферменемией, которая может опережать клиническую картину заболевания (см. ХГВ). Критериями фазы реактивации является наличие: HCV-PHK, анти-HCVcore IgM, анти-HCVcore IgG, aHTH-NS4, увеличение АлАТ в 3 и более раз. Преимущественные темпы прогрессирования фазы реактивации отмечены при 1 генотипе HCV.
В клинической картине ХГС, по аналогии с ХГВ, следует учитывать возможность развития многочисленных внепеченочных проявлений (см. « Аутоиммунный гепатит» ).
ГЕПАТИТ G
К настоящему времени идет поиск новых видов возбудителей вирусных гепатитов, что сокращает список криптогенных заболеваний печени. Наиболее перспективными оказались исследования группы GB- вирусов (их наименование соответствует инициалам больного, 34-летнего хирурга, у которого впервые диагностирован данный гепатит). Позднее удалось выделить еще три новых вирусных агента, обзначенных как GBV-A , GBV-B, GBV-C. Геном вируса представлен одноцепочечной РНК, он близок по структуре к HCV. Эпидемиологическая характеристика гепатита HGV/GBV-C близка к другим сывороточным гепатитам, особенно С. Это касается источников заражения и путей передачи. Основным маркером данного гепатита является РНК HGV/GBV-C в сыворотке крови. Имеются сообщения о возможности развития хронического гепатита HGV, причем чаще выявляется его коинфекция с другими сывороточными гепатитами. Клинически могут быть сглаженные и манифестные формы, с развитием внепеченочных проявлений.
ХРОНИЧЕСКИЙ ЛЕКАРСТВЕННЫЙ ГЕПАТИТ
Его рассматривают как длительно протекающее воспалительное заболевание печени, обусловленное негативным эффектом медикаментов. Оно может быть связано как с прямым токсическим воздействием лекарств или их метаболитов, так и с идиосинкразией к ним. При этом идиосинкразия может проявляться метаболическими либо иммунологическими нарушения-ми. Поэтому, видимо, лекарственный гепатит (ЛГ) может быть подобен вирусному или аутоиммунному с антиядерными и антимикросомальными антителами. При аутоиммунном варианте ЛГ воспалительный процесс в печени быстро исчезает после отмены препаратов.
ХРОНИЧЕСКИЙ КРИПТОГЕННЫЙ ГЕПАТИТ
Под ним, согласно новой классификации 1994г., "следует понимать заболевание печени с характерными для ХГ морфологическими изменениями при исключении вирусной, аутоиммунной или лекарственной этиологии" (Desmet V. и соавт., 1994г.).
СТЕПЕНЬ АКТИВНОСТИ ПРОЦЕССА
является следующим после этиологии новым критерием ХГ. Ее установлению способствуют как лабораторные тесты, так и морфологическое исследование биоптатов печени.
Морфологические критерии активности процесса новая классификация рекомендует определять с использованием полуколичественного метода и подсчетом гистологического индекса степени активности (ГИСА) по R.G.Knodell. ГИСА учитывает в баллах следующие морфологические компоненты ХГ:
1. Перипортальные некрозы гепатоцитов, включая мостовидные -
оцениваются от 0 до 10 баллов;
2. Внутридольковые фокальные некрозы и дистрофия гепатоцитов -
от 0 до 4 баллов;
3. Воспалительный инфильтрат в портальных трактах - от 0 до 4
баллов;
4. Фиброз - от 0 до 4 баллов.
ГИСА оценивается от 1 до 3 баллов как "минимальный" ХГ, от 4 до 8 баллов как "мягкий или слабовыраженный" ХГ от 9 до 12 баллов как "умеренный" ХГ, от 13 до 18 баллов как "тяжелый" ХГ.
Новая классификация, к сожалению, не рассматривает проявления активности процесса за пределами печени, особенно при вирусном и АГ. Но все же внепеченочные (системные) проявления необходимо учитывать, поскольку они в значительной степени являются отражением активности гепатита.
СТАДИЯ ЗАБОЛЕВАНИЯ
(по V.Desmet et all, 1994) характеризует степень хронизации процесса и оценивается только гистологически по выраженности фиброза в печени, с подсчетом гистологического индекса стадии хронизации (ГИСХ). Варианты фиброза: портальный, перипортальный (включая порто-портальные, порто-центральные септы). Порто-центральные септы более важны для развития ЦП.
Выделяют:
0 - отсутствие фиброза;
1 стадию хронизации (слабая степень фиброза: портальный и пери-
портальный фиброз);
II стадию хронизации (умеренная степень фиброза: порто-
портальные септы одна или более);
III стадию хронизации (тяжелая степень фиброза: порто-центральные
септы одна или более);
IV стадия (цирроз).
ПРИМЕРЫ ФОРМУЛИРОВКИ ДИАГНОЗА
1. Хронический гепатит В, фаза репликации вирусной инфекции,
умеренной степени активности (ГИСА 9 баллов), I стадия хронизации.
2. Хронический гепатит С, латентная фаза, инаппарантная форма,
минимальной степени активности (ГИСА 3 балла), I стадия хронизации
(слабая степень фиброза).
3. Хронический гепатит С, фаза реактивации, выраженой степени
активности (ГИСА 13 баллов), III стадия хронизации (тяжелая стадия
фиброза).
АЛКОГОЛЬНОЕ ПОРАЖЕНИЕ ПЕЧЕНИ
Алкогольный гепатит, как указано выше, сохраняет свое существование только в рамках МКБ-10. Причем наиболее частой формой поражения печени при алкоголизме является алкогольный стеатоз, далее - алкогольный гепатит с трансформацией в ЦП.
Поражение печени возникает при ежедневном употреблении не менее 80 г этанола в течение 5-8 лет (10 г этанола содержатся в 25 мл водки или в 85 мл вина или в 230 мл пива). Факторами риска алкогольной болезни печени являются:
- генетически обусловленная чувствительность к алкоголю
- плохое питание (дефицит белка)
- злоупотребление алкоголем с молодого возраста
- женский пол
- скорость метаболизма этанола в печени
Алкогольная болезнь развивается в результате:
1. Прямого токсического действия этанола (пероксидация липидов -
свободные радикалы - пероксидация мембранных фосфолипидов – повреж-
дение гепатоцита);
2. Воздействия токсичных продуктов метаболизма этанола;
3. Влияния генетических и иммунных факторов;
4. Недоедания;
5. Инфицирования HBV и HCV, которое наблюдается гораздо чаще у
алкоголиков, чем в популяции.
Клинические симптомы алкогольной болезни неспецифичны: диспепсия, боли в верхнем квадранте живота, энцефалопатия, гепатомегалия с преимущественным увеличением левой доли печени. При лабораторных исследованиях выделяют лейкоцитоз, соотношение АсАТ/АлАТ 2:1, снижение уровня гамма-глютамилтранспептидазы на фоне абстиненции.
СОВРЕМЕННЫЕ ПОДХОДЫ К ЛЕЧЕНИЮ ХРОНИЧЕСКИХ
ГЕПАТИТОВ
С учетом классификации ХГ комплексная терапия заболевания должна учитывать степень активности патологического процесса в печени, ведущего синдрома болезни, наличия признаков цирротической стадии, фазы развития вирусной инфекции.
ЛЕЧЕНИЕ АУТОИММУННОГО ГЕПАТИТА
В лечении АГ используют 2 схемы: монотерапия преднизолоном и сочетание преднизолона с 6-меркаптопурином (азатиоприном). Комбинированное лечение предпочтительнее, так как дает значительно меньше побочных эффектов.
Монотерапия преднизолоном проводится больным, имеющим противопоказания к назначению цитостатиков (цитопения, желтуха). Доза преднизолона - 30-40 мг/сут в течение месяца, далее ежемесячно суточную дозу снижают на 5 мг; поддерживающая доза составляет 10-15 мг/сут. Терапия длительная, не менее 2 лет.
Комбинированную терапию преднизолоном и 6-меркаптопурином проводят при нарастании активности процесса на фоне уменьшения дозы преднизолона, а также при быстром развитии осложнений преднизолонотерапии, при учете отсутствия противопоказаний к цитостатикам. Чаще используют две схемы лечения. Одна из них предусматривает включение азатиоприна после предшествующего 1-2 месячного курса преднизолонотерапии при снижении дозы последнего до 15-20 мг/сут. Назначают азатиоприн из расчета 1,5 мг/кг, в среднем 50-100 мг/сут. Поддерживающие дозы преднизолона составляют 5-10 мг/сут., азатиоприна - 25 мг/сут.
По другой схеме комбинированной терапии преднизолон и азатио-прин назначают одновременно. В течение первой недели преднизолон идет в дозе 30 мг/сут., 2-й - по 20 мг/сут., 3-й и 4-й - по 15 мг, а с 5-й недели переходят на прием поддерживающей дозы 10 мг/сут. Доза азатиоприна на всем протяжении составляет 50 мг/сут.
Поддерживающая терапия независимо от избранной схемы должна проводиться в течение 1-2 лет после достижения стойкой клинико-морфологической ремиссии.
ЛЕЧЕНИЕ ВИРУСНЫХ ХГ
При любых синдромах и любой степени активности обязательна базисная терапия, которая включает:
1. Диета-стол 5 с индивидуальными модификациями, комплекс вита-
минов, особенно С, Е, Р, минеральные воды.
2. Режим, исключение приема алкоголя, гепатотоксичных лекарств,
инсоляции, вакцинаций, сауны, профессиональных и бытовых вредностей,
обязательное лечение сопутствующих заболеваний.
3. Средства, нормализующие деятельность желудочно-кишечного
тракта, препятствующие дисбактериозу, накоплению кишечных эндотокси-
нов, эндотоксинемии. К числу таких средств можно отнести эубиотики
(лактобактерин, колибактерин, бифидумбактерин и им подобные).
Целесообразен прием лактулозы, нормазе, плохо всасывающихся антибиотиков, энтеродеза, энтерола, при необходимости - ферментов (панкреатин, фестал и др.).
4. Гепатопротекторы, обладающие некоторым метаболическим дей-
ствием:
- Карсил (силибор, силимарин) по 1 драже 3 раза в день, курсом до 2
мес;
- Эссенциале по 1 капсуле 3 раза в день;
- Лохеин по 5 мл 3 раза в день за 30' до еды; а также ряд других пре-
паратов (максар, катерген, гепабене, гептрал).
5. Лекарственные травы, обладающие противовирусным действием
(зверобой, календула, чистотел и др.), слабовыраженным желчегонным и
преимущественно спазмолитическим действием (чертополох, мята, спорыш
и др.).
6. Физиотерапевтические мероприятия, лечебная физкультура.
7. Психологические (психотерапия, гипноз и др.) и социально-профессиональные аспекты терапии.
ЭТИОТРОПНАЯ И ИММУНОМОДУЛИРУЮЩАЯ ТЕРАПИЯ
Наибольшее значение в терапии вирусных гепатитов имеют этиотропные препараты, основным из которых является интерферон (ИФН).
Назначение ИФН и других противовирусных препаратов целесообразно только в репликативную фазу вирусной инфекции, ведущим маркером которой служит выявление в крови и ткани печени нуклеиновых кислот вирусов.
Интерфероны представляют собой группу низкомолекулярных пептидов, обладающих противовирусной, противоопухолевой, иммунорегуля-торной активностью. В настоящее время выделяют два типа ИФН. I тип включает в себя альфа-ИФН и бета-ИФН, II тип – гамма-ИФН.
Подразделение на типы обусловлено различной биологической ролью. Если альфа- и бета-ИФН свойственна в основном противовирусная активность, стимуляция выработки противовоспалительных цитокинов, экспрессия антигенов HLA I класса, то гамма-ИФН является универсальным эндогенным иммуностимулятором: под его воздействием усиливается связывание антигенов клетками, экспрессия антигенов HLA, повышается ответ лимфоцитов на митогены, лизис клеток-мишеней, продукция иммуноглобулинов, фагоцитарная активность макрофагов и их кооперативное взаимодействие с Т- и В-клетками; он ингибирует рост опухолевых клеток и подавляет внутриклеточное размножение бактерий и простейших, способствует дифференцировке Т-лимфоцитов. Кроме того, ИФН одного класса может потенцировать действие ИФН другого класса.
Продукция ИФН осуществляется:
Альфа - ИФН - В-лимфоцитами, нулевыми лимфоцитами, макрофагами;
Бета - ИФН - фибробластами, эпителиальными клетками, макрофагами;
Гамма – ИФН - NK-лимфоцитами и Т-лимфоцитами (субпопуляции CD3+, CD4+, CD8+, CD 11+) при наличии вспомогательных клеток (моноциты, макрофаги, дендритные клетки).
На современном этапе ИФН являются основным средством этиотроп-ной терапии вирусных гепатитов. Широко используются как нативный (лейкоцитарный), т.е. получаемый из культуры лейкоцитов человека, так и синтезируемый при помощи рекомбинантной техники ИФН. Гамма -ИФН получил меньшее распространение. Различий в терапевтической эффективности нативного и рекомбинантного ИФН не выявлено. Применяются следующие препараты ИФН:
Альфа - ИФН: nl, nЗ - из культуры лейкоцитов; 2а, 2Ь, 2с - рекомбинантные;
Бета - ИФН : n - из культуры фибробластов, г, la, lb - рекомбинантные;
Гамма -ИФН: r, lb - рекомбинантные.
Все звенья противовирусного эффекта ИФН до конца не изучены. По современным представлениям, клетки под влиянием ИФН приобретают "противовирусное состояние" в результате связывания его со специфическим клеточным рецептором, что приводит к активации внутриклеточных ферментов, в частности 2′, 5′- олигоаденилсинтетазы и так называемых эф-фекторных белков. Это, в свою очередь, вызывает активацию нутриклеточ-ных рибонуклеаз, разрушающих вирусную транспортную РНК. Кроме того, ИФН ингибируют процесс "раздевания", трансляции, сборки вирусов в процессе репликации. В противовирусном эффекте играют также роль некоторые защитные иммунные механизмы: усиление экспрессии антигенов HLA I типа на поверхности инфицированных клеток, стимуляция макрофагов, узнающих вирус-НЬА-антигенный комплекс на поверхности клеточной мембраны, усиление активности цитотоксических Т- и NK-лимфоцитов.
Уникальные свойства ИФН способствовали активной разработке различных технологий его производства и сделали препараты интерферона незаменимыми в терапии внутриклеточных инфекций. В таблице 1 представлены зарегистрированные в нашей стране препараты ИФН.
Таблица 1
ПРЕПАРАТЫ ИФН
| Препарат | Тип ИФН | Фирма | Страна |
| Роферон-А | α-2а | "Roche" | Швейцария |
| Интрон А | α-2Ь | "Schering-Plough" | США |
| Реальдирон | α-2Ь | "Biofa" | Литва |
| Альфаферон | а | "Alpha Wassermann" | Италия |
| Вэллферон | аn-1 | "Glaxowellcome" | Англия |
| Бетаферон | b-lb | "Schering" | ФРГ |
| Виферон | α-2 | ЗАО БКИ | Россия |
| Реаферон | α-2 | НПО "Вектор" | Россия |
Лечение ХГВ. Программа лечения должна быть строго дифференцированной. При этом в основу должна быть положена прежде всего оценка активности инфекционного процесса с разграничением ХГВ с высокой (репликативный, HBeAg-позитивный вариант) и низкой (интегративный, HBeAg-негативный вариант) репликацией HBV. При обоих типах ХГВ терапевтическая программа требует также морфологического контроля био-птатов печени, прежде всего для своевременного выявления формирования ЦП и уточнения необходимых лечебных мероприятий.
I. ХГВ с высокой репликативной активностью.
При данном варианте основную задачу лечения представляет возможно полное подавление репликации HBV, являющееся непременным условием прекращения прогрессирования патологических изменений в печени и улучшения состояния больного.
Показания для назначения ИФН:
1. Обязательно подтвержденная высокая репликативная активность HBV: обнаружение в крови (или выявление возможных маркеров в биоптатах печени) HBV-ДНК, HBeAg, анти-НВе класса IgM, ДНК-полимеразы.
2. Повышение активности АлАТ не менее, чем в 1,5 раза.
3. Гистологическая картина ХГ.
4. Давность ХГ не более 2 лет.
5. Вoзраст до 45 лет.
6. Отсутствие ЦП.
7. Отсутствие микст-гепатита (HDV, HCV).
Не показано лечение (опасность декомпенсации, быстрого прогреси-рования):
1. ХГВ в интегративной фазе;
2. ХГВ, вызванный мутантным штаммом HBV (НВе- штамм). Рядом
авторов считается (Подымова С.Д., Буеверов А.О., 1997), что при заражении
мутантной формой HBV (т.е. при наличии вирусной ДНК, ДНК-
полимеразы, но отсутствии HBeAg), имеется устойчивость к лечению
ИФН. Однако рядом исследователей рекомендуется все же попытка лечения
комбинацией препаратов (например интерфероном-альфа в дозе 6 млн ME
3 раза в неделю в течение 6 мес.и аналогом нуклеозидов ламивудином).
Противопоказания к назначению ИФН:
1. Признаки АГ и другие аутоиммунные заболевания (тиреоидит,
тромбоцитопения и др.).
2. Депрессивные состояния.
3. Ишемическая болезнь сердца.
4. Сосудистые заболевания головного мозга.
5. Почечная недостаточность.
6. Сахарный диабет.
7. Беременность.
Программа терапии.
Препараты ИФН назначают в/м или п/к в дозе 3-5 млн МЕ/сут, 3 раза в неделю в течение 6 мес. Такая схема лечения при ХГВ рассматривается как "золотой стандарт". В клинической практике предпочитают более высокие дозы ИФН до 10 млн МЕ/сут 3 раза в неделю или 5 млн МЕ/сут ежедневно. Однако такое увеличение дозировки, с одной стороны, терапевтически не оправдано, с другой - при многомесячном курсе лечения способствует более выраженному побочному действию ИФН и небезопасно. Длительное применение высоких доз ИФН подавляет продукцию эндогенного ИФН, угнетает антительный ответ на вирусный антиген, что может способствовать персистированию инфекционного процесса.
Оценка терапевтического эффекта проводится по положительному ответу на ИФН в виде трансформации репликативного ХГВ в интегративный. Об этом свидетельствует сероконверсия HBeAg в анти-НВе, сохраняющаяся в течение 6 мес. после отмены препарата. Эффективность интрона курсом в 6-12 месяцев составляет 40-50%. Устойчивые благоприятные результаты лечения ИФН, сохраняющиеся в течение года и более после отмены препарата, удается достичь лишь у 25-35% больных.
При ХГВ результаты лечения ИФН можно в известной степени прогнозировать. Наиболее надежные критерии эффективности интерферо- нотерапии (Соринсон С.Н., 1998):
- Небольшая давность болезни, отсутствие указаний о гепатите, пе-
ренесенном в детстве.
- Молодой возраст (до 45 лет).
- Отсутствие выраженных проявлений ЦП.
- Отсутствие избыточной массы тела.
- Отсутствие микст-гепатита (маркеров HDV, HCV и др.).
- Отсутствие выраженного иммунодефицита.
- Относительно невысокий уровень HBV-ДНК (менее 100 нг/л).
- Подтверждение признаков "дикого" (HBVe+), а не мутантного
(HBVe-) штамма HBV.
- Отчетливое повышение АлАТ в начале курса лечения (через 4-8
недель т.н. "цитолитический криз").
- Обнаружение в крови анти-НВс IgM.
- Отсутствие выраженного побочного действия ИФН.
- Женский пол.
Побочное действие ИФН
обусловлено длительными курсами лечения, особенно при назначении высоких доз (свыше 5 млн ME) и проявляется в виде:
- гриппоподобного синдрома ( лихорадка до 38-39 градусов, головная
боль, боль в глазных яблоках, мышцах, суставах);
- появлением аутоиммунных реакций ( тиреоидит, сахарный диабет,
гломерулонефрит и др.);
- умеренная нормохромная анемия, лейко- и тромбоцитопения;
- тошнота, снижение аппетита, диарея;
- нервно-психические расстройства (появляются и прогрессируют
раздражительность, беспокойство, повышенная возбудимость, ощущение
постоянной тревоги, вялость, апатия, попытки к суициду);
- мышечная слабость;
- алопеция.
ПРЕДЛЕЧЕНИЕ ГЛЮКОКОРТИКОСТЕРОИДАМИ
Его рекомендуют в целях повышения эффективности последующей терапии ИФН. Оно рассчитано не столько на терапевтический эффект ГКС, сколько на снижение активности инфекционного процесса, закономерно развивающегося после их отмены. В эту вторую "рикошетную" фазу регистрируется стимуляция защитных механизмов, увеличивается выработка эндогенного ИФН, усиливается иммунный лизис инфицированных гепа-тоцитов, чему соответствует закономерное повышение АлАТ. Предлече-ние показано больным с хроническим HBeAg-позитивным ГВ с незначительным увеличением или полным отсутствием повышения активности АлАТ. Назначают внутрь преднизолон в течение 7-8 недель - первые 2 недели по 60 мг, 3-4 - по 40 мг, последние 2 недели - по 20 мг ежедневно. Через 2 недели назначают ИФН.
П. ХГВ с низкой репликативной активностью.
При данном варианте основную задачу составляют предупредительные мероприятия, исключающие возможность активации инфекционного процесса. Успех лечения ИФН в данном случае проблематичен. При выявлении морфологических признаков ХАГ с циркуляцией анти-НВе считается полезным предлечение глюкокортикостериодами (ГКС) в целях подавления чрезмерной иммунной реакции, поддерживающей активный гепатит.
Возможно применение гепатопротекторов (см. выше). Предупредительные мероприятия включают рациональное трудоустройство, с исключением перегрузок, командировок, хорошей организацией труда и отдыха. Рекомендовано домашнее питание с некоторыми ограничениями жирной и жареной пищи, желательно с высоким содержанием овощей и фруктов. Исключается сухоедение, острые закуски. Система питания должна обеспечивать ежедневный стул. Запрещаются спиртные напитки. При возникновении сопутствующих заболеваний, требующих применения лекарственных средств, должны быть исключены потенциально гепатоток-сичные. Практически тот же комплекс предупредительных мероприятий может быть рекомендован и при латентном хроническом носительстве HBsAg.
Характеристика состояния больных ХГ требует динамического контроля за появлением и прогрессированием признаков ЦП. Согласно принятой в зарубежной клинической практике терминологии эти критерии в своей совокупности характеризуют как "качество жизни". Разработана система интегральной его оценки в баллах (%), получившая известность под названием индекса Карновского (табл.2).
Таблица 2
КРИТЕРИИ ОЦЕНКИ КАЧЕСТВА ЖИЗНИ БОЛЬНЫХ ХГ
(индекс Карновского)
| Признаки | Тип А 100-80% | Тип В 70-50% | Тип С 40-10% |
| Жалобы | Нет | Редко | Постоянны выражены |
| Физическая активность | В основном сохранена | Ограничена | Недоступна |
| Утомляемость | Незначительно | Характерна | При малейшей нагрузке |
| Трудоспособность | Ограничена | Практически утрачена | Утрачена |
| Самообеспечение | Полное | Частичное | Отсутствует |
| Потребность в уходе | Отсутствует | Большей частью | Постоянно |
| Необходимость госпитализации | Отсутствует | Чаще отсутствует | Постоянно |
| Степень компенсации | Полная компенсация | Субкомпенсация | Декомпенсация |
Вычисление индекса Карновского регламентирует решение социальных вопросов, экспертизу трудоспособности, установление группы инвалидности, прогнозирование дальнейшего течения болезни и продолжительности жизни.
ЛЕЧЕНИЕ ХГС
Задачи ИФН-терапии при ХГС аналогичны таковым при ХГВ: подавление активной репликации вируса, предупреждение развития ЦП и гепатоцеллюлярной карциномы.
Показания для назначения ИФН:
1. Репликативная активность НСV (положительные результаты инди-
кации HCV-PHK, анти-HCV IgM в крови, а также HCV-PHK и HC-Ag в
биоптатах печени.
2. Повышение исходного уровня активности Ал AT в 3 раза и более.
Программа терапии при ХГС, как и при ХГВ, в основном применяют препараты рекомбинантного α-2-ИФН, прежде всего интрон А. Дозы - по 3 -5 млн МЕ/сут, п/к или в/м, 3 раза в неделю в течение 6-12 мес. В последние годы перспективным является применение нового препарата ПегИнтрона А (пегинтрон альфа-2Ь), коньюгированного с полиэтиленгликолем. Пегилирование Интрона А обеспечивает увеличение длительности его действия за счет значительного замедления почечного клиренса и соответственно повышения длительности периода полувыведения примерно с 4 до 40 часов. Доза - 0,5, 1,0 и 1,5 мкг/кг один раз в неделю.
В связи с присущим HCV прямого цитопатического действия благоприятная реакция на ИФН знаменуется не цитолитическим кризом с повышением активности АлАТ, а постепенным снижением. Оценку эффективности можно проводить по критериям ремиссии Консенсуса Европейской группы по изучению гепатита:
1. Биохимические критерии - контроль уровня активности АлАТ
(ежемесячно в процессе лечения, в первые 6 мес. ежемесячно после лече
ния, затем каждые полгода не менее 36 мес. подряд).
Первичная ремиссия - положительная динамика активности АлАТ на ранних этапах (2 последовательных нормальных значения АлАТ, взятых ближе к окончанию лечения с интервалами не менее 2 недель).
Рецидив
- а/, прекращение ремиссии еще в процессе лечения ("ускользание"),
т.е. нормализация активности АлАТ в первые 6 мес, а затем, еще до окон
чания лечения, вновь повышение ее активности (при 2 последовательных
патологических значениях АлАТ с интервалом не менее 2 недель);
- б/, прекращение ремиссии после окончания лечения: любое повы
шение активности АлАТ, если первично после лечения имелось нормали
зация ее значений.
Стабильная ремиссия - стабильно нормальные значения АлАТ в течение 6 мес. после лечения.
Длительная ремиссия - стабильно нормальные значения АлАТ в течение 24 мес. после лечения.
Отсутствие ремиссии - отсутствие нормализации значений АлАТ или снижение < чем на 50%.
2 Вирусологические критерии - по индикации HCV-PHK.
Первичная ремиссия - отсутствие HCV-PHK к окончанию курса тера
пии.
Прекращение ремиссии - повторное выявление HCV-PHK после ее первичного исчезновения.
Стабильная ремиссия - отсутствие HCV-PHK через 24 мес. после окончания лечения.
Длительная ремиссия - отсутствие HCV-PHK через 24 мес. после наступления первичной ремиссии.
Отсутствие ремиссии - выявление HCV-PHK к окончанию лечения.
3. Гистологические критерии могут быть оценены при динамическом
контроле за биоптатами печени (за 6 мес. до лечения и через 12 мес. после
его окончания). Критерий оценки - ГИСА.
Ремиссия - отсутствие активного воспаления в дольках, отсутствие или незначительная инфильтрация портальных полей, отсутствие прогрес-сирования в ЦП (если его не было). Неполная ремиссия - снижение ГИСА не менее чем на 2 балла по сравнению с исходным, отсутствие прогрессирования в ЦП.
Отсутствие ремиссии - любой другой тип изменений.
Необходимо отметить, что биохимические, вирусологические и гистологические критерии могут не совпадать.
Критерии благоприятного ответа на ИФН-терапию:
- Раннее начало лечения (оптимально - в первый год после заражения)
- Молодой возраст (до 45 лет)
- Низкий уровень HCV-PHK
- Генотип HCV 2а, 2Ь, За (при генотипе la, lb - резистентность к
ИФН)
- Фиброз гистологически - незначительный
- Женский пол
- Отсутствие избыточного веса
- Исходно повышенные значения АлАТ (нормальные или близкие к
норме показатели АлАТ рассматриваются как критерий отрицательного
прогноза)
- исчезновение анти-HCV core IgM в процессе лечения.
-
Отрицательным критерием ответа на ИФН служит повышение содержания железа в сыворотке крови и накопление железа в печени. В отношении его уровня в крови установлены даже параметры отрицательного прогноза - выше 32 ммоль/л у мужчин и выше 28 ммоль/л у женщин.
Особенно острожным должно быть назначение ИФН у больных, у которых не исключен АГ. При возникновении сомнений в диагнозе рекомендуют даже проводить ex juvantibus лечение ГКС. Назначают пробный курс преднизолона (30 мг в день) в сочетании с азатиоприном (50 мг) в течение 3 мес. Положительные результаты такого курса подтверждают аутоиммунную природу гепатита и должны расматриваться как критерии противопоказания к ИФН-терапии. При назначении ГКС может наступить обострение инфекционного процесса с повышением АлАТ. Вместе с тем считают, что назначение ГКС при ХГС потенциально куда менее опасно, чем применение ИФН при аутоиммунном гепатите.
Предлечение ГКС - рекомендуют при ХГС с нормальными исходными показателями АлАТ (см. "Лечение ХГВМ).
Латентая фаза HCV-инфекции требует в основном комплексной поддерживающей терапии, которую усиливают:
- Предупредительные мероприятия (см. «Лечение ХГВ»)
- Урсофальк (урсосан) - 10 мг/кг/сутки, 3-6 мес.
- Гептрал - 800-1600 мг/сут, сначала в/м (в/в) 2 нед., затем внутрь 3
мес.
- Витамин Е (токоферол) - 200-300 мг/сут, 2-4 мес.
МЕТОДЫ АЛЬТЕРНАТИВНОЙ ТЕРАПИИ
Подразумевают сочетанное применение ИФН с другими препаратами противовирусной, противовспалительной, иммуномодулирующей направленности, реже - в качестве монотерапии. Применяют:
1. Рибавирин (Ребетол) - препарат группы аномальных нуклеозидов
вирусостатического действия (на РНК и ДНК содержащие вирусы). Назна-
чают в течение 5 мес. с постепенным увеличением дозы: 1-2 мес. -600, 3-
4 мес. - 1000 и 5-6 мес. - 1200 мг/сут. Побочный эффект - нерезкий гемо-
лиз, гиперурикемия.
2. Ламивудин (зеффикс, эпивир) - синтетический аномальный нуклео-
зид, его преимуществом является подавление процессов фиброзирования, а
также известная эффективность при заражении мутантным штаммом HBV.
Назначается внутрь в дозе 100-300 мг/сут в течение 4-12 мес.
3. Индукторы синтеза эндогенного ИФН - различаются по тому, на
какие клетки-продуценты действуют и синтез какого вида ИФН они вызы-
вают, а также по времени достижения максимальной концентрации ИФН в
сыворотке крови и продолжительности действия препарата.
Циклоферон (камедон, неовир) - растворимый синтетический аналог природного алкалоида из культуры Citrusgraudis. Стимулирует синтез раннего ИФН в макрофагах, нейтрофилах, В-клетках с максимальной продукцией через 4-6 часов и длительностью действия 24 ч.
Применяется в/м по схеме 4,0 мл 12,5% р-ра один раз в 10 дней в те-
чение 6 месяцев. Амиксин - действует преимущественно на Т-клетки с
образованием позднего α-ИФН и β-ИФН с максимумом продукции через 12-18 час.
Наряду с этими существуют другие индукторы ИФН (кагоцел, лари-фан, ридостин). Перспективным направлением является применение отечественного индуктор β-ИФН - йодантипирина у больных ХГВ и ХГС.
4. Сизофиран - полисахарид, экстракт культуры Schizophillum
commune Fries. Способствует иммунному цитолизу инфицированных гепа-
тоцитов и элиминации вирусов. Доза - 10 мг/сут, 1 раз в неделю в течение
3-6 мес.
5. Пропагерманиум - органическое соединение германия, активизи-
рует хелперные и цитотоксические функции Т-лимфоцитов, увеличивает
образование интерлейкинов I и II, натуральных киллеров, способствует
продукции эндогенного γ-ИФН. Доза - 30 мг/сут. внутрь, 3-4 недели.
Однако все вышеперечисленные критерии оценки эффективности этиотропной терапии (уровень аминотрансфераз, индикация РНК и ДНК вирусов в крови, клиническая картина) в настоящее время все большим числом исследователей признаются суррогатными, а единствено правильными и достоверными служат отсутствие прогрессирования ХГ в ЦП и гепатоцеллюлярную карциному при многолетнем наблюдении за больными ХГ.
СИНДРОМАЛЬНАЯ ТЕРАПИЯ
Цитолитический синдром, выявляемый при ХГ, требует коррекции путем введения белковых препаратов (альбумины), факторов свертывания крови (плазма, криопреципитат), перфузии крови через пласты гетеропече-ни, методов экстракорпоральной детоксикации. Холестатический синдром купируется путем назначения адсорбентов желчных кислот (холестирамин, билигнин), адсорбентов (карболен, полифепан, ваулен), а также, как показано в последние годы, препаратов ненасыщенных жирных кислот (урсо-фальк, хенофальк и др.), гемо- и плазмосорбции.
ЛЕЧЕНИЕ АЛКОГОЛЬНОГО ПОРАЖЕНИЯ ПЕЧЕНИ
Помимо первого и необходимого условия - отказа от приема алкоголя, логичным представляется использование эссенциальных фосфолипидов. Основным препаратом является эссенциале, возможно использование других гепатопротекторов. Также назначается гептрал (аденозил-α-метионин), липотропные средства (липоевая кислота и др.), урзодезоксихолевая кислота.
СПЕЦИФИЧЕСКАЯ ПРОФИЛАКТИКА
Начиная с 1982 года стали доступны для профилактики гепатита В хорошо переносимые эффективные вакцины. Задачей вакцинации является стимулировать выработку антител к вирусу гепатита В, довольно быстро и с достаточно высоким титром обеспечивающим иммунитет.
К настоящему времени разработаны 2 типа лицензированных коммерческих вакцин против ГВ: плазменная и дрожжевая геноинженерная.
Плазменные вакцины представляют собой высокоочищенный HBsAg, получаемый из крови хронических носителей с высоким его содержанием. Вакцину приготовляют с включением HBsAg разных субтипов, что обеспечивает ее поливалентную иммуногенность.
Анти-HBs начинают накапливаться уже через 1-6 нед. после начала вакцинации, их концентрация достигает пика через 3 мес. после ее окончания. Пороговый протективный титр анти-HBs составляет 10 МЕ/л. Он обеспечивается трехкратным введением вакцины с повторными иньекциями через 1 и 6 (или 2) мес. и длительно сохраняется в крови. Критерием высокой защищенности является титр анти-HBs 50 МЕ/л и выше. Ревакцинацию считают показанной через 5 лет после первой. Надежное защитное действие у большинства привитых обеспечивают сравнительно большие дозы вакцины - до 20 мкг HBsAg, что определяет высокую стоимость плазменных вакцин.
Началу вакцинации всегда должно предшествовать скрининговое обследование намеченных контингентов на маркеры HBV. Важно выявить, с одной стороны, инфицированных (HBsAg), с другой - защищенных, ранее перенесших ГВ (анти-HBs > 10 ME/л). И те, и другие иммунизации не подлежат.
Геноинженерные рекомбинантные вакцины внедрены с 1987 г. Их преимуществом является полное отсутствие человеческой плазмы, исключающее необходимость инактивации и контроля безвредности. Эти вакцины по своей иммуногенности не уступают плазменным. Получают геноинженерные вакцины на дрожжевых клетках, экспрессирующих HBsAg. Назначают в тех же дозах и по той же схеме, что и плазменные вакцины. При иммунизации людей старше 40 лет предпочтительна программа, состоящая из двух последовательных введений 2 высоких доз вакцины (20-40 мкг HBsAg) с интервалом 6 мес.
В последние годы применяют комбинированные вакцины (против гепатита А и В). В частности имеется бивалентная вакцина «Твинрикс» производства компании «Смит-Кляйн Бичем».
Эффективность вакцинации высокая. Одним из факторов, препятствующих активной иммунизации, является наличие у вакцинированных HCV-инфекции.
Существуют и активно-пассивные методы иммунизации, преимущественно используются у детей, родившихся от HBsAg- позитивных ( особенно HBeAg-позитивных) матерей . Вводится вакцина и параллельно гипериммуноглобулин В (IgHB), содержащий высокий титр готового анти-HBs.
Дата добавления: 2021-12-10; просмотров: 17; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!
