Связь пространственного строения с биологической активностью
Введение в биоорганическую химию.
Пространственное строение органических молекул.
Биоорганическая химия возникла на стыке наук, таких как:
· Органическая химия
· Биологическая химия
· Биология
· Молекулярная генетика, однако, базируется она в основном на материале органической химии, используя ее теоретические представления и весь арсенал ее методов исследования.
Главная цель изучения биоорганической химии заключается в формировании системных знаний о структуре и закономерностях в химическом поведении основных классов природных органических соединений, лежащих в основе как строения живых объектов, так и всех процессов жизнедеятельности.
Основные понятия органической химии
Химический состав молекулы – представляет собой количество атомов отдельных химических элементов, входящих в данную молекулу. Выражается в виде молекулярной формулы, например, для молочной кислоты. С3Н6О3
Химическое строение вещества – устойчивый порядок соединения атомов в молекуле с учетом характера связей между ними.
Химическое строение вещества может быть представлено в виде структурной формулы или формулы строения, например, для молочной кислоты:
СН3-СН(ОН)-СООН
Конфигурация – фиксированное пространственное расположение атомов или атомных групп в молекуле относительно друг друга.
Конфигурация может быть представлена или в виде стереохимических формул или в виде проекционных формул Фишера. Для лактата:
|
|
|

Конформации – называют различные энергетически неравноценные геометрические форму молекулы соединения, переходящие друг в друга за счет вращения отдельных частей молекулы вокруг одинарных связей. Конформации могут быть представлены или в виде стереохимических формул, или в виде проекционных формул Ньюмена.
Внутренняя энергия молекулы – энергия взаимодействия входязих в нее атомов и кинетическая энергия, обусловленная движением молекулы. Энергия атомных взаимодействий в молекуле может быть подразделен на:
· Энергию химических связей между атомами
· Энергию так называемых несвязных взаимодействий (конформационная энергия).
Химический состав молекулы может быть установлен в ходе качественного и количественного элементарного анализа химического соединения, а на основании изучения свойств соединения может быть установлено его химическое строение.
Возможность выяснения химического строения соединения на основе изучения его свойств является краеугольным камнем теории химического строения, предложенного А. И. Бутлеровым.
|
|
|
Именно А. И. Бутлеров впервые обратил внимание на то, что различный порядок соединения одних и тех же атомов может дать различные вещества, тем самым он дал объяснение широко распространенному в мире органических соединений явлению изомерии. Этот вид изомерии получил название структурной изомерии.
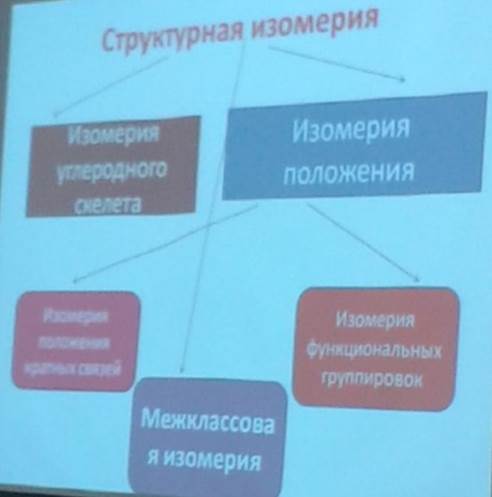
Вместе с тем, во второй половине 19 века выяснилось, что существуют вещества, имеющие одинаковый порядок соединения атомов в молекуле, но отличающиеся друг от друга по некоторым свойствам, таким, например, как способность вращать в разные стороны плоскость поляризованного луча света или способность кристаллизоваться в виде кристаллов, похожих друг на друга как предмет и его зеркальное изображение.
Необходимость объяснения этих различий привела к формированию новой области химии – стереохимии, т.е. учения о трехмерной структуре.
В основе стереохимии органических соединений лежит идея тетраэдричности насыщенного атома углерода.
При изображении строения органической молекулы все связи между атомами располагают в одной плоскости, предполагая тем самым, что и молекулы плоские, двумерные.
Вант Гофф и Лебель были первыми, кто указал на ошибочность такого рода представлений.
|
|
|
В реальном трехмерном пространстве валентные связи атома углерода располагаются не в одной плоскости, а под углом друг к другу. Если по всем четырем валентностям атом углерода связан с одинаковыми атомами или группами атомов, то угол между валентными связями составляет 109.5 градусов, а валентные связи будут направлены к вершинам тетраэдра. И тогда молекула становится трехмерной.
При изображении на бумаге такого тетраэдрического атома углерода поступают следующим образом:
· Связи, лежащие в плоскости бумаги изображают обычными линиями;
· Связи, идущие к наблюдателю, изображают в виде зачерненного клина;
· Связи, уходящие за плоскость бумаги – пунктиром или заштрихованным клином
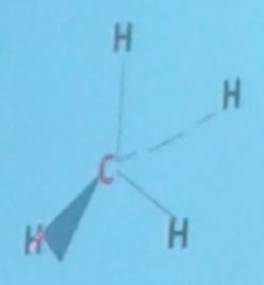
Молекула метана симметрична, поскольку атом углерода является центром ее симметрии. Если заменить атом водорода на какой-либо другой атом или группировку, молекула не потеряет симметричности, т.к. будет иметь ось симметрии:
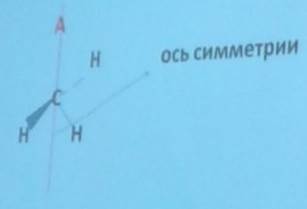
Замена еще одного атома водорода на какую-либо другую группировку также не приведет к потере симметрии, т.к. сохранится плоскость симметрии.
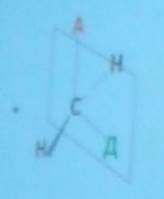
При замене третьего атома водорода на группировку не идентичную двум другим, молекула теряет все элементы симметрии.
|
|
|
Такие молекулы получили название хиральных молекул.
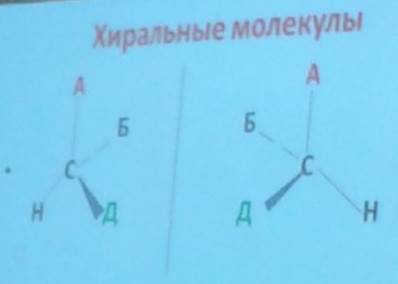
Хиральные молекулы
Хиральные молекулы могут существовать в двух пространственных формах, похожих друг на друга как предмет и его изображение в зеркале («хирон» - рука). Эти молекулы не идентичны, поскольку попытки совместить одну молекулу с другой безуспешны.
Данные молекулы – изомеры, отличающиеся друг от друга не порядком соединения атомов в молекуле, а их фиксированным расположением.
Изомерия, связанная с различным пространственным расположением атомов в молекуле, называется пространственной или стереоизомерией.
В виду того, что порядок соединения атомов в молекулах рассматриваемых изомеров одинаков, они чрезвычайно сходны друг с другом по химическим свойствам. Тем не менее их можно различить по некоторым физическим свойствам, например, по способности вращать плоскость поляризованного луча света (один из них вращает влево, другой – вправо).
Такие стереоизомеры получили название оптических (зеркальных) изомеров.
Оптической активностью обладают только хиральные молекулы; молекулы, имеющие те или иные элементы симметрии (ахиральные), оптической активностью не обладают.
Все хиральные молекулы содержат в своей структуре атом углерода, связанный по всем четырем валентностям с разными атомами или атомными группировками – хиральный атом, в качестве которого обычно находится атом углерода в состоянии sp-3 гибридизации.
В качестве хиральных атомов могут быть атомы серы, азота, фосфора.
Оптические изомеры, являющиеся зеркальными изомерами, называются энантиомерами.
Энантиомер, вращающий плоскость поляризованного луча вправо, обозначается как /+/, а вращающий плоскость луча поляризованного луча влево, обозначается как /-/.
Эквимолекулярные смеси энантиомеров, содержащих равные количества право- и левовращающих изомеров, называются рацемическими смесями (рацематами).
Рацематы оптической активностью не обладают.
D и L стереохимические ряды
Конфигурация асимметрического атома углерода в соединении может быть описана тем или иным способом. Наиболее широко применяются правила Фишера, использующие обозначения D и L и правила Кана-Ингольда-Прелога, использующие обозначения R и S.
Правила Фишера связывают расположение атомов и атомных групп
У асимметрического атома углерода рассматриваемого соединения со стандартом, в качестве которого был избран глицериновый альдегид /+/.
Этому энантиомеру глицеринового альдегида была произвольно приписана определенная конфигурация, которую обозначили как D.
Левовращающему глицериновому альдегиду приписали зеркальную конфигурацию, которую обозначили буквой L.
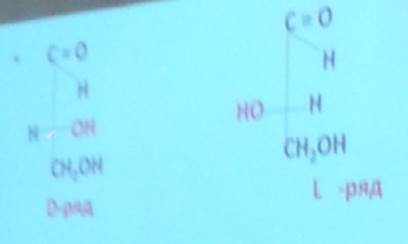
Конфигурация хиральной молекулы обозначается D или L в зависимости от того, аналогична ли она конфигурации D или L глицеринового альдегида.
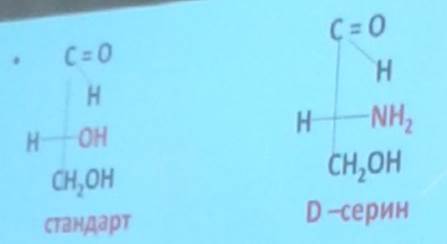
В молекуле может присутствовать несколько асимметрических атомов углерода. В таком случае количество стереоизомеров возрастает. Часть из них будет зеркальными изомерами (энантиомерами).
Остальные стереоизомеры, не являющиеся энантиомерами, называются диастереомерами.
Общее число стереоизомеров можно рассчитать по формуле 2n, где n – число асимметрических центров в молекуле.
Диастереомеры отличаются друг от друга по физическим и химическим свойствам.
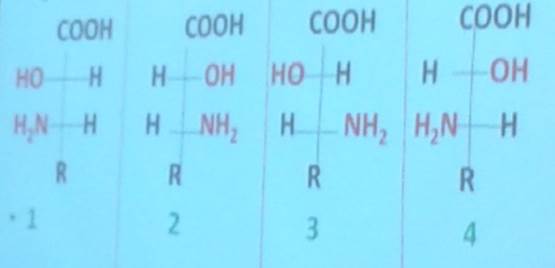
1,2; 3,4 – энантиомеры
1,3; 1,4; 2,3; 2,4 – диастереомеры
Связь пространственного строения с биологической активностью
Большинство метаболитов являются хиральными молекулами. При взаимодействии одних хиральных молекул с другими хиральными молекулами появляются различия в их химических свойствах. Такие молекулы обычно реагируют одновременно несколькими реакционными центрами и характер их взаимодействия будет зависеть от их взаимной ориентации.
В процессе обмена в клетке участвует L-яблочная кислота, L-молочная кислота, L-аминокислоты, D-сахара.
Хиральными молекулами являются белки, построенные из L-аминокислот, фосфолипиды, витамины, гормоны и т.д.
Стереоизомерия лежит в основе специфичности взимодействия субстрат – фермент, гормон – рецептор, антиген – антитело и др.
Фармакологическое действие ряда лекарственных веществ обусловлено их взаимодействием с рецепторами клетки.
При создании новых лекарственных веществ, имеющих хиральные центры, следует иметь в виду, что различные энантиомеры могут обладать различным и даже противоположным действием, биодействием.
Например, препарат тамидомид (+)R-изомер – хороший транквилизатор и снотворное, а(-)S-энантиомер – является тератогенов (оказывает токсическое действие на плод).
Левовращающий энантиомер кокаина почти в 2 раза более активен в качестве местного анастетика, чем его правовращающий оптический антипод.
Из двух энантиомеров адреналина наибольшую фармакологическую активность имеет R(-) адреналин; S(+) адреналин биологической активностью не обладает.
Причиной такой специфичности взаимодействия является комплементарность – взаимное соответствие дополняющих друг друга структур (макромолекул, коферментов, субстратов, радикалов и др.), определяемое их пространственной структурой и химическими свойствами (способностью образовывать водородные и другие связи).
Аналогичная картина характерна и для ряда джругих лекарственных средств. Так, правовращающий изопропиладреналин (изодрин) проявляет в 800 раз более сильное бронхорасширяющее действие, чем его левовращающий энантиомер.
Лекарственное средство противоопухлевого действия саркозилин является левовращающим энантиомером; правовращающий сарколизин не активен.
Дата добавления: 2023-01-08; просмотров: 183; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!
