Рецидивирующий и повторный инфаркт миокарда
Глава 10
ЗАТЯЖНОЙ, РЕЦИДИВИРУЮЩИЙ И ПОВТОРНЫЙ ИНФАРКТ МИОКАРДА
Затяжное течение инфаркта миокарда
Обычная для инфаркта миокарда продолжительность острого приступа составляет от десятков минут до нескольких часов, максимально 1—2 сут.
Однако у части больных острый (даже острейший) период заболевания может продолжаться несколько дней.
В течение этого периода продолжается расширение зоны некроза миокарда непосредственно в области первоначального инфаркта миокарда, по его периферии и — намного реже — в отдаленных отделах сердечной мышцы.
Не существует четкой границы между обычным и затяжным течением инфаркта миокарда.
Мы полагаем, что о последнем можно говорить, если формирование свежих очагов некроза продолжается свыше 48 ч после начала приступа, однако такое (или иное) деление является условным.
Причинами затяжного течения инфаркта миокарда являются:
— гибель в зоне первоначального некроза уцелевших островков мышечной ткани, находящихся в наиболее неблагоприятных условиях;
— распространение некроза на периинфарктную ишемизированную область сердечной мышцы;
— продолжающийся внутрикоронарный тромбоз и коронароспазм;
— недостаточность коронарного кровообращения в интактных отделах миокарда в условиях их компенсаторной гиперфункции и распространенного атеросклероза коронарных артерий.
|
|
|
Затяжному течению инфаркта миокарда будут способствовать все обстоятельства, увеличивающие несоответствие между потребностью сердечной мышцы в кровоснабжении и его фактическим уровнем: повышенная работа миокарда (гиперкинетический тип сердечной деятельности, высокое артериальное давление), артериальная гипотония, тахиаритмии и т. д.
Обычным клиническим проявлением затяжного течения инфаркта миокарда являются многодневные рецидивирующие ангинозные боли, не уступающие обычной антиангинальной терапии и требующие повторных инъекций наркотиков, нейролептаналгезии, внутривенного введения нитроглицерина.
Сходная картина наблюдается при постепенно развивающихся надрывах и разрывах миокарда, однако и при них, как правило, в массивных участках некроза продолжает погибать уцелевшая мышечная ткань.
В тех случаях, когда свежие некрозы появляются в перинекротической зоне и в отдалении от нее, боли ярко выражены, а иногда даже превосходят по силе первоначальный приступ.
Чаще всего это наблюдается при распространении субэндокардиального инфаркта миокарда до трансмурального.
Однако при гибели «внутриинфарктных» первоначально уцелевших участков миокарда боль может быть несильной и даже отсутствовать.
|
|
|
В таких случаях клиническая картина затяжного инфаркта миокарда может ограничиваться повторными эпизодами острой левожелудочковой недостаточности, нарушениями сердечного ритма, падениями АД.
Лабораторные показатели при затяжном течении инфаркта миокарда длительно остаются характерными для острой стадии заболевания.
Спустя несколько суток после начала приступа СОЭ возрастает, но это не сопровождается обычным снижением уровня креатинфосфокиназы»
Наиболее убедительным признаком затяжного течения инфаркта миокарда являются электрокардиографические признаки распространяющегося некроза миокарда: позднее формирование зубца Q(QS), увеличение числа отведений с признаками инфаркта миокарда, появление признаков инфаркта миокарда новой локализации.
Менее доказательно, но должно насторожить врача появление нарушений проводимости и собственно аритмий сердца (не обусловленных ятрогенией).
При обширном некрозе с формированием аневризмы сердца гибель замурованных в толще инфаркта «островков» миокарда может вообще не сопровождаться какой-либо электрокардиографической динамикой или появляются небольшие изменения сегмента ST и зубца Г, которые сами по себе не дают оснований предположить появление свежих очагов некроза.
|
|
|
Приведем несколько характерных примеров.
Больной 68 лет госпитализирован через 3 ч после начала ангинозного приступа. Боли не были полностью купированы кардиологической бригадой скорой помощи. При поступлении на ЭКГ — картина острого субэндокардиального инфаркта миокарда передней стенки и верхушки левого желудочка (рис. 32, а). В течение 5 дней по несколько раз в сутки возникали тяжелые ангинозные приступы, прекращавшиеся лишь после нейролептаналгезии; почти постоянно проводилось капельное введение нитроглицерина; проводилось также лечение антагонистами кальция и гепарином. В течение недели уровень MB фракции КФК в крови оставался в 4—5 раз выше нормы. Наибольший подъем был отмечен на 3-й день болезни после двухчасового приступа болей, сопровождавшихся сердечной астмой. В течение 1 недели заболевания регистрировались нечастые одиночные левожелудочковые экстрасистолы. Со 2-й недели ангинозные приступы прекратились. При активизации больного появилась стенокардия напряжения: боли возникали при ускорении темпа ходьбы, прекращались при остановке или сразу после приема нитроглицерина (нитрокора, нитроспрея). Динамика электрокардиограммы свидетельствовала о том, что у больного сформировался трансмуральный некроз в той же зоне (рис. 32, б, в).
|
|
|
Больной 69 лет госпитализирован через 1,5 ч после начала болей.
Болевой приступ продолжался около 1 ч и был купирован введением таламонала.
При поступлении болей нет, на ЭКГ — признаки трансмурального инфаркта миокарда переднебоковой стенки левого желудочка.
Через 1 ч после поступления в клинику возобновились боли, продолжавшиеся, несмотря на массивную антиангинальную терапию, в течение нескольких часов.
В последующие 4 дня боли возникали ежедневно; наряду с приступами стенокардии, прекращавшимися после приема нитроглицерина (нитрокора, нитроспрея), 2—3 раза в сутки развивались тяжелые болевые приступы.
С первого дня появилась левожелудочковая недостаточность: одышка, тахипноэ, застойные хрипы в нижних отделах легких, умеренный акроцианоз.
По ночам возникали приступы сердечной астмы. В течение всех этих дней электрокардиограмма практически не менялась, сохранялся высокий уровень КФК и а-ГБДГ в крови. На шестой день болезни в момент очередного болевого приступа возникла фибрилляция желудочков (на экране кардиомонитора — крупноволновое мерцание желудочков). После дефибрилляции и восстановления сердечной деятельности больной стал жаловаться на сильную боль в груди, метался в постели.
Вновь возникла фибрилляция желудочков (мелковолновая). Реанимационные мероприятия оказались безуспешными.
На вскрытии: обширный инфаркт миокарда переднебоковой стенки и верхушки левого желудочка с очагами некроза различной давности.

Рис. 32. ЭКГ при затяжном течении инфаркта миокарда. Объяснения в тексте
Чем больше размеры инфаркта миокарда, тем вероятнее, что отдельные ишемизированные участки сердечной мышцы погибают не сразу, т. е. имеется затяжное течение инфаркта миокарда, не всегда сопровождающееся соответствующей клинической и электрокардиографической симптоматикой.
Об этом свидетельствуют, в частности, секционные данные.
Больной 72 лет госпитализирован по поводу трансмурального инфаркта миокарда переднебоковой стенки левого желудочка через 6 ч после начала болей. Болевой приступ был купирован врачом скорой помощи. В течение 4 дней периодически жаловался на тупые несильные боли в области сердца, стихавшие самостоятельно или после инъекций анальгина. Электрокардиограмма существенно не менялась. На пятый день болезни возникла резкая боль за грудиной с иррадиацией в левое плечо. В момент осмотра врачом произошла остановка сердца. На электрокардиограмме — редкий идиовентрикулярный ритм, сменившийся асистолией. Реанимационные мероприятия, включая трансвенозную кардиостимуляцию, не дали эффекта. Был диагностирован разрыв аневризмы сердца с гемотампонадой. На секции диагноз подтвердился, причем в области аневризмы были обнаружены очаги некроза различной давности, что свидетельствовало о затяжном течении инфаркта миокарда; вероятно, этим объясняется и относительно поздний разрыв сердца.
Расширение зоны некроза, безусловно, увеличивает возможность возникновения сердечной недостаточности, нарушений ритма и проводимости, образования аневризмы и разрывов сердечной мышцы. Однако главная опасность при затяжном течении инфаркта миокарда — вероятность развития фибрилляции желудочков.
Лечение больного с затяжным течением инфаркта миокарда проводится вплоть до стабилизации его состояния в отделении (блоке) интенсивной терапии при постоянной готовности медперсонала к реанимационным мероприятиям.
Определенные трудности возникают при назначении тромболитических и антикоагулянтных препаратов прямого действия больным с затяжным течением трансмурального инфаркта миокарда, когда имеется реальная угроза разрыва сердца.
По-видимому, при наличии убедительных признаков распространения некроза эти препараты все же должны применяться, поскольку возможность провоцирования ими разрыва миокарда и гемотампонады менее вероятна, чем возникновение фибрилляции желудочков и других тяжелых осложнений.
Рецидивирующий и повторный инфаркт миокарда
До тех пор пока не найдены радикальные методы лечения ишемической болезни сердца, лица, пережившие инфаркт миокарда, будут оставаться группой повышенного риска возникновения новых некрозов сердечной мышцы.
Различные вмешательства на коронарных артериях могут улучшить ситуацию, но не изменить ее принципиально.
Повторные некрозы миокарда могут развиваться спустя дни, месяцы и годы после перенесенного инфаркта миокарда и являются наряду с внезапной смертью одной из основных причин летальности у больных с постинфарктным кардиосклерозом.
По отношению к перенесенному инфаркту миокарда повторные некрозы могут быть разделены на ранние и поздние, причем какой-либо общепринятой градации не существует.
В отечественной литературе принят термин «рецидивирующий инфаркт миокарда» для повторных некрозов, развивающихся в процессе излечения от перенесенного инфаркта миокарда. А.Л. Мясников выделил рецидивирующий инфаркт миокарда в качестве особой формы заболевания в докладе на V Международном конгрессе терапевтов в Филадельфии в 1958 г.
По справедливому замечанию академика РАМН профессора В.В. Серова, термин «рецидивирующий инфаркт миокарда» нельзя признать удачным, поскольку в отличие от рецидивирующего воспаления, ишемии и т. д. инфаркт заканчивается необратимыми изменениями — некрозом и рубцеванием. Однако он вошел в практику.
Было бы правильнее говорить о раннем повторном инфаркте миокарда, отнеся к нему критерии рецидивирующего инфаркта миокарда.
Как правило, к рецидивирующему инфаркту миокарда относят повторные некрозы, возникающие в течение 8—12 нед. после перенесенного инфаркта миокарда [Попов В.Г., Гватуа Н.А., 1957; Струков А.И., 1959; Лукомский П.Е., 1964].
В зарубежной литературе обычно не разделяют рецидивирующие и повторные инфаркты миокарда.
Нами [Сыркин А.Л. и др., 1981] под рецидивирующим инфарктом миокарда понимается вариант болезни, при котором новые участки некроза миокарда возникают в сроки от 72 ч после развития инфаркта миокарда и до окончания основных процессов рубцевания, т. е. приблизительно в течение 8 нед. после возникновения инфаркта миокарда.
При этом после возникновения каждого нового очага некроза отсчет времени начинается заново.
Увеличение размеров очага некроза и появление новых очагов в течение первых 72 ч после развития инфаркта миокарда мы рассматриваем как расширение зоны формирующегося инфаркта миокарда и в таких случаях диагноз рецидивирующего инфаркта миокарда не ставим.
К рецидивирующему варианту мы не относим также затяжное течение инфаркта миокарда, при котором не возникает «светлых» промежутков (исчезновение болей, снижение гиперферментемии и т. д.), а имеет место длительный — от нескольких дней до 1 нед. и более — период следующих один за другим болевых приступов с постоянно повышенной активностью ферментов крови, лихорадкой и другими признаками свежих некротических изменений в миокарде.
Определение сроков возникновения рецидивирующего инфаркта миокарда, конечно, весьма условно.
Наиболее обоснованной представляется точка зрения А.Л. Мясникова (1969), не связывающего рецидивирующий инфаркт миокарда с каким-либо определенным сроком, но относящего к этому варианту повторные некрозы миокарда, возникающие до развития компенсации функциональных и морфологических поражений, вызванных предыдущим инфарктом.
Необходимо, однако, сделать оговорку, что речь не идет о тех нарушениях, которые не могут быть компенсированы даже после окончательного формирования постинфарктного рубца.
Патогенетические механизмы рецидивирующего инфаркта миокарда сходны с описанными выше для затяжного течения заболевания и связаны преимущественно с функциональной и анатомической недостаточностью кровоснабжения сохранившегося миокарда [Наддачина Т.А., Смольянников А.В., 1963].
В.Г. Попов (1972) у 100% погибших больных с рецидивом инфаркта миокарда обнаружил выраженный стенозирующий атеросклероз, часто с облитерацией одной из венечных артерий. У 23 из 25 больных был обнаружен коронарный тромбоз.
По его данным, основным условием возникновения рецидивирующего инфаркта миокарда является тяжелый стенозирующий атеросклероз коронарных артерий при поражении коллатеральных сосудов; в этих случаях не только выключение какой-либо коронарной артерии в результате тромбоза, но даже нарушение способности ее к адекватному расширению при одновременном функциональном отягощении миокарда могут явиться причиной нового некроза миокарда.
Высказывалось мнение о возможности аутоиммунного генеза рецидивов инфаркта миокарда [Шестаков С.А. и др., 1970; Виноградов С.А. и др., 1970; Durnbusch S., 1956].
В наших наблюдениях (морфологические исследования проведены Л.В. Раиновой) при изучении сердец 32 погибших больных с рецидивирующим инфарктом миокарда атеросклероз коронарных артерий имел стенозирующий характер у 30 человек [Сыркин А.Л. и др., 1981].
У 23 больных из 32 рецидив инфаркта миокарда развился за счет некроза участков сохранившихся мышечных волокон в зоне первичного поражения и за счет некроза в периинфарктной зоне.
Для рецидивирующего инфаркта миокарда наиболее характерно наличие очагов колликвационного некроза с резко замедленной пролиферативной реакцией и больших зон резко измененных дистрофичных волокон как в периинфарктной зоне, так и в зоне грануляции.
Тромбоз коронарных артерий при рецидиве инфаркта миокарда был обнаружен у 24 из 32 умерших, в том числе у 8 из 9 больных с рецидивом в интактной зоне.
Таким образом, складывается впечатление, что рецидивирующий некроз в отдаленных отделах миокарда обычно возникает при тромбозе соответствующих артерий. Для возникновения же рецидива в зоне инфаркта и в периинфарктной области может оказаться достаточным увеличение несоответствия между потребностью в кровоснабжении и состоянием коронарного кровотока (эмоциональная и физическая нагрузка, другие функциональные факторы).
Частота рецидивирующего течения инфаркта миокарда колеблется, по данным различных авторов, от 4% [Хомякова Г.Н., 1969] до 31% [Попов В.Г., 1967].
Столь значительные расхождения могут объясняться различием наблюдавшихся контингентов больных и критериев диагностики рецидива.
Клиническое значение рецидивов инфаркта миокарда чрезвычайно велико. Уменьшается масса сократительного миокарда, возрастает число больных с хрони234
Глава 10
ческой недостаточностью кровообращения и нарушениями сердечного ритма. Значительно удлиняется продолжительность стационарного лечения.
Вновь возникший некроз резко увеличивает опасность летального исхода. Так, по нашим данным, из 656 больных, остававшихся в живых спустя 72 ч после возникновения инфаркта миокарда, в период дальнейшего пребывания в стационаре погиб 41 человек, при этом среди больных с рецидивирующим инфарктом миокарда умерли 32 из 105 человек, а среди остальных лишь 9 из 551 человека.
Рецидив инфаркта миокарда явился причиной 35% всей больничной летальности от инфаркта миокарда, а среди остававшихся в живых спустя 72 ч от начала болезни и погибших в более поздние сроки рецидив был основной причиной смерти (78% погибших больных).
При трансмуральном характере инфаркта миокарда и его рецидива летальность, по нашим данным, достигает 72%.
При сопоставлении затяжного и рецидивирующего вариантов инфаркта миокарда важной особенностью последнего является его нередкое возникновение на фоне более или менее удовлетворительного состояния больного.
При затяжном течении опасность, как правило, очевидна, поэтому больной находится под постоянным наблюдением медперсонала в отделении интенсивной терапии.
Рецидив некроза возникает в любые сроки больничного лечения, вплоть до момента выписки больного из стационара.
Лишь у части больных предвестником рецидива может явиться ранняя постинфарктная стенокардия напряжения и особенно покоя, требующая всегда исключительного внимания.
Существуют определенные трудности и в диагностике рецидивирующего инфаркта миокарда. Поскольку значительная часть рецидивов связана с гибелью участков мышцы, находящихся среди уже некротизированной ткани, они «умирают молча», без болей.
По сравнению с обычным инфарктом миокарда рецидив характеризуется большей частотой аритмического, гастралгического, астматического и бессимптомного вариантов клинической картины. По нашим наблюдениям, среди больных с рецидивирующим инфарктом миокарда рецидив протекал с ангинозным статусом у 66%, а первоначальный инфаркт миокарда — у 89% больных.
Больной 51 года находился в клинике по поводу трансмурального инфаркта миокарда переднеперегородочной области левого желудочка.
Заболевание протекало без осложнений, за исключением нечастых и нетяжелых приступов стенокардии напряжения. Через 2 нед. после возникновения инфаркта миокарда при обычном самочувствии на очередной электрокардиограмме зарегистрировано распространение некроза на боковую стенку левого желудочка (рис. 33, а, б).
Содержание КФК в крови оказалось вдвое выше нормы (при предшествующем биохимическом исследовании крови этот показатель был близок к нормальному уровню). Дальнейшее течение заболевания — без осложнений.
Некоторые трудности могут возникнуть и при оценке лабораторных показателей у больных с рецидивирующим инфарктом миокарда.
Во-первых, при возникновении рецидива в первые 1—2 нед. болезни эти показатели могут еще оставаться повышенными и на этом фоне повторное их увеличение будет менее заметным.
Во-вторых, сдвиги в лабораторных данных (в особенности это относится к лейкоцитозу и СОЭ) могут быть ошибочно объяснены другими причинами, например присоединением пневмонии.
Наконец, если некротизируется очаг миокарда, сохранившийся в зоне формирующегося рубца, резорбция из области свежего некроза затруднена и уровень ферментов или миоглобина может оказаться ниже, чем следовало бы ожидать.
Возможны различные варианты электрокардиографической динамики при развитии рецидива некроза:
— появление признаков свежего некроза миокарда на фоне изменений, обусловленных предшествующим инфарктом миокарда;
— появление признаков свежего некроза с исчезновением ранее имевшихся электрокардиографических признаков инфаркта миокарда;
— ложноположительная динамика ЭКГ;
— возникновение нарушений сердечного ритма и проводимости без других указаний на рецидив некроза миокарда.
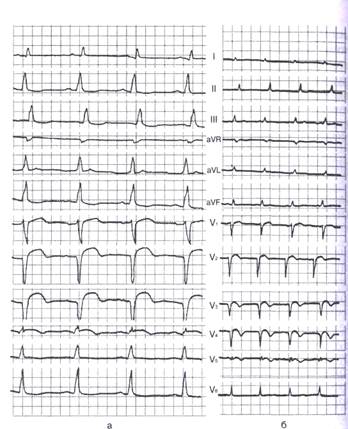
Рис. 33. Трансмуральный инфаркт миокарда переднеперегородочной области с последующим распространением некроза на боковую стенку левого желудочка: а — ЭКГ перед возникновением рецидива; б — после рецидива
Исчезновение признаков инфаркта миокарда при появлении электрокардиографических симптомов рецидива чаще всего происходит при возникновении трансмурального рецидива у больного с эндокардиальным (интрамуральным) инфарктом миокарда, причем локализация инфаркта и рецидива совпадает.
При трансмуральном инфаркте миокарда и рецидиве трансмурального некроза той же локализации желудочковый комплекс QR может смениться комплексом QS.
Больной 64 лет 11 лет назад перенес инфаркт миокарда, госпитализирован после ангинозного приступа с диагнозом: повторный инфаркт миокарда переднебоковой стенки левого желудочка и межжелудочковой перегородки (рис. 34, а).
На 4-й день болезни возник тяжелейший ангинозный статус, который не купировался в течение 2 сут.; развился трансмуральный рецидив инфаркта миокарда передней стенки левого желудочка и межжелудочковой перегородки (рис. 34, б), осложненный политопной желудочковой и предсердной экстрасистолией, формированием острой аневризмы сердца, инфарктом правого легкого, желудочным кровотечением. Течение рецидива носило затяжной характер. Больной находился в стационаре 91 день, выписан в относительно удовлетворительном состоянии. После реабилитации в загородной больнице и санаторного лечения вернулся к работе.
Диагностика рецидивирующего инфаркта миокарда, равно как и определение его локализации, в таких случаях не представляет трудности. Клиническое значение этого типа изменений ЭКГ при рецидиве некроза состоит в том, что инфаркт миокарда, если он не был диагностирован ранее, уже не выявляется на ЭКГ и свежие очаговые изменения могут трактоваться не в качестве рецидива, а как собственно инфаркт миокарда.
По нашим наблюдениям, это бывает нередко, причем приступы болей, возникавшие за несколько дней до наиболее тяжелого приступа, приводящего к госпитализации, трактуются как прединфаркт.
В действительности же у этих больных возникает инфаркт миокарда без зубца Q, а госпитализируют их с опозданием по поводу трансмурального рецидива инфаркта миокарда.
Ложноположительная динамика ЭКГ чаще всего сводится к исчезновению или уменьшению «коронарного» зубца Т. При этом ЭКГ меньше изменена, чем до возникновения рецидива инфаркта миокарда.
Клиническое значение данного типа электрокардиографической динамики при рецидивирующем инфаркте миокарда весьма велико.
При повторных инфарктах миокарда с аналогичными изменениями ЭКГ им предшествует, как правило, период «электрокардиографической стабильности» продолжительностью от нескольких месяцев до нескольких лет.

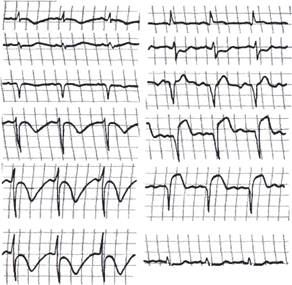
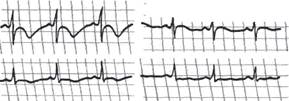
Рис. 34. ЭКГ при повторном инфаркте миокарда
и трансмуральном рецидиве.
Объяснения в тексте
В этих случаях внезапное «улучшение» ЭКГ, особенно при наличии какого-либо ухудшения клинической картины, настораживает опытного врача.
При рецидиве же ложноположительная динамика ЭКГ наблюдается, когда ЭКГ и при обычном течении инфаркта миокарда может подвергаться быстрым изменениям.
В этих условиях положительная динамика ЭКГ при отсутствии значительного ухудшения состояния больного может приниматься врачом за улучшение течения процесса.
Значительно реже встречается другой вариант ложноположительной динамики ЭКГ, при котором исчезают признаки инфаркта миокарда без появления указаний на рецидив.
Это может происходить при локализации инфаркта и рецидива в противоположных областях сердечной мышцы со взаимной «нейтрализацией» электрокардиографической картины.
Больной 56 лет перенес трансмуральный инфаркт миокарда переднеперегородочной области. В дальнейшем на ЭКГ оставались стабильные рубцовые изменения (рис. 35, а). На эхокардиограмме отмечалась зона дискинезии в передней стенке левого желудочка и межжелудочковой перегородке.
Через 3 года больной перенес тяжелый приступ ангинозных болей с характерной динамикой уровня ферментов, лейкоцитозом и последующим увеличением СОЭ. На ЭКГ возникла и сохранилась ложноположительная динамика (рис. 35, б).
На эхокардиограмме отмечено появление участка дискинезии в заднедиафрагмальном отделе левого желудочка.
Ситуация со взаимной нейтрализацией признаков инфаркта и рецидива особенно опасна, если оба случая произошли до госпитализации и ЭКГ была снята лишь после второго из них.
В главе 8 отмечались трудности электрокардиографической диагностики инфаркта миокарда при некоторых нарушениях сердечного ритма и проводимости.
В еще большей степени это относится к диагностике рецидива, поскольку аритмии могут явиться не признаком рецидива, а лишь поздним осложнением инфаркта миокарда.
Больная 76 лет доставлена в клинику в тяжелом состоянии с повторным трансмуральным инфарктом миокарда нижней стенки левого желудочка, осложненным кардиогенным шоком, нарушением ритма сердца (атриовентрикулярный ритм, экстрасистолия, переходящая блокада левой ножки предсердно-желудочкового пучка).
В течение нескольких дней пребывания в стационаре у больной исчезли нарушения внутрижелудочковой проводимости, восстановился синусовый ритм (рис. 36, а).
Через 32 дня возникло трепетание предсердий с проведением импульсов 2 : 1, 3 : 1, затем — мерцательная тахиаритмия с быстрым прогрессированием недостаточности кровообращения.
По витальным показаниям разрядом дефибриллятора восстановлен синусовый ритм, однако отмечалась суправентрикулярная бигеминия и групповая экстрасистолия (рис. 36, б).
Характерные данные лабораторных исследований (лейкоцитоз, гиперферментемия), клинические данные (тяжелые нарушения ритма сердца с последующим нарастанием застойной недостаточности кровообращения) дали основание диагностировать рецидив инфаркта миокарда.
Постепенно состояние улучшилось, однако на фоне относительного благополучия на 42-й день после рецидива инфаркта миокарда вновь возникла мерцательная аритмия, а через сутки наступила смерть.
Патологоанатомическое исследование: инфаркт миокарда и рецидив некроза в задней стенке левого желудочка и межжелудочковой перегородке на фоне гипертонической болезни. Крупноочаговый кардиосклероз. Отек легких.
Необходимо также отметить, что у значительной части больных можно, диагностируя с уверенностью рецидив инфаркта миокарда, лишь весьма ориентировочно высказываться о его локализации.
Особенности клинической картины, электрокардиографической динамики и лабораторных показателей приводят к тому, что определить масштаб рецидива, массу некроза миокарда у многих больных можно лишь весьма приблизительно.
Обычная ошибка в таких случаях — преуменьшение размера рецидива инфаркта миокарда.
Повторный инфаркт миокарда в большинстве случаев не представляет особой сложности для диагностики.
Однако, возникая на фоне рубцовых изменений (постинфарктного кардиосклероза), он чаще, чем первый инфаркт, протекает без выраженного ангинозного статуса [Шишкин С.С, 1963; Попов В.Г., 1971].
Электрокардиографические варианты повторного инфаркта миокарда сходны с описанными в разделе о рецидивирующем инфаркте миокарда.
Как и при последнем, просмотр предшествующих приступу электрокардиограмм чрезвычайно важен и может иметь решающее диагностическое значение.
Больная 60 лет госпитализирована через сутки после затяжного приступа стенокардии.
Со слов больной, 3 года назад перенесла обширный тяжелый инфаркт миокарда.
При поступлении состояние удовлетворительное.
На основании данных анамнеза, ЭКГ, умеренной гиперферментемии, числа лейкоцитов при поступлении 9,1 • 109/л, СОЭ 16 мм/ч было высказано предположение об эндокардиальном или интрамуральном повторном инфаркте миокарда передней стенки левого желудочка в зоне рубца после первого — трансмурального — инфаркта миокарда.
Течение заболевания — без осложнений, больной было разрешено вставать с 4-го дня болезни.
Через неделю была получена электрокардиограмма полугодовой давности, где имелись лишь негативные зубцы Т в отведениях V2 — V4.
He вызывает сомнений, что перенесенный в прошлом «обширный, тяжелый» инфаркт миокарда в действительности таковым не являлся, а поводом для настоя-
щей госпитализации явился трансмуральный инфаркт миокарда.
Основной причиной ошибочной оценки повторного инфаркта миокарда были чрезмерное доверие к рассказу пациентки и умеренные сдвиги лабораторных показателей.
Важной особенностью повторного инфаркта миокарда является возможность возникновения отека легких и даже кардиогенного шока при относительно небольших некрозах, если рубцы после предыдущих инфарктов миокарда занимают большую площадь.
Дата добавления: 2018-02-15; просмотров: 5631; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!
