ГОСУДАРСТВЕННОЕ БЮДЖЕТНОЕ ПРОФЕССИОНАЛЬНОЕ ОБРАЗОВАТЕЛЬНОЕ УЧРЕЖДЕНИЕ РЕСПУБЛИКИ КРЫМ
«КЕРЧЕНСКИЙ ПОЛИТЕХНИЧЕСКИЙ КОЛЛЕДЖ»
| СОГЛАСОВАНО Председатель ПЦК __________/___________ Ю.А. Зимина | ЭКЗАМЕНАЦИОННЫЙ БИЛЕТ по программе промежуточной аттестации по дисциплине ОУД.10 Химия | № билета | Профессия |
| 27 | 43.01.09. |
1.Оксиды, их состав. Основные и кислотные оксиды. Химические свойства. Получение оксидов. 2. Закончить следующие уравнения реакций, характеризующие данных веществ. Указать тип химических реакций. а) CH4 + Cl2 → в) C2H4 + H2 → б) C3H6 + O2 → 3 .В трёх пробирках находятся растворы солей; нитрат натрия, хлорид натрия и сульфат натрия. Как определить, в какой пробирке находится сульфат натрия?
__________________________
Задание 1 оценивается в 1 балл
|
|
|
Задание 2 оценивается в 2 балла
Задание 3 оценивается в 2 балла Подпись преподавателя ___________
Пояснительная записка.
Учебный план и рабочая программа ГБПОУ РК «КПТ», предусматривает промежуточный контроль в форме экзамена по дисциплине «Химия». Экзамен проводиться на завершающем этапе освоения учебной дисциплины «Химия», на втором курсе. Экзамен проводиться в форме набора контрольных заданий в виде экзаменационных билетов, устно. (согласованно на ЦМК протокол №___ от ___2018г.)
Экзамен по дисциплине «Химия» преследуют цель оценить работу обучающегося за курс обучения, полученные теоретические и практические знания, их прочность, развитие творческого мышления, приобретение навыков самостоятельной работы, умение синтезировать полученные знания и применять их к решению практических задач.
Соответственно объему учебного материала, обязательного для усвоения, определено оптимальное число билетов в каждом комплекте: 21 билет на профильном уровне. Каждый билет включает два теоретических вопроса и задание практико-ориентированного характера (расчетную задачу или лабораторный опыт). Для экзамена рекомендованы лишь те лабораторные опыты, которые по своему содержанию отвечают:
|
|
|
требованиям стандарта, соответствуют перечню учебного оборудования, а также имеющие профессиональную направленность, в соответствии с выбранной профессией.
Примерное время, отводимое на подготовку к ответу: 25– 30 минут по билету комплекта профильного уровня;
При оценивании ответа приоритетное значение имеет соответствие знаний требованиям государственного образовательного стандарта к уровню общеобразовательной подготовки по химии.
Критерий оценивания ответов обучающихся на экзамене
Оценка «отлично»
Дан полный, развернутый ответ на поставленные вопросы, показана совокупность осознанных знаний по дисциплине, доказательно раскрыты основные положения вопросов; в ответе прослеживается четкая структура, логическая последовательность, отражающая сущность раскрываемых понятий, теорий, явлений. Знание по дисциплине демонстрируется на фоне понимания её в системе данной науки и междисциплинарных связей. Ответ изложен литературным языком с использованием специальных терминов. Могут быть допущены недочеты в определении понятий, исправленные студентами самостоятельно в процессе ответа. Задача решена верно, упражнения выполнены верно.
|
|
|
Оценка «хорошо»
Дан полный, развернутый ответ на поставленные вопросы, показано умение выделить существенные и несущественные признаки, причинно-следственные связи. Ответ четко структурирован, логичен, изложен литературным языком с использованием специальных химических терминов. Могут быть допущены 2-3 неточности или незначительные ошибки, исправленные студентами с помощью преподавателя. Допущены незначительные ошибки при решении задачи, выполнении упражнений.
Оценка «удовлетворительно»
Дан недостаточно полный и недостаточно развернутый ответ. Логика и последовательность изложения имеют нарушения. Допущены ошибки в раскрытии понятий, употреблении терминов. Студент не способен самостоятельно выделить существенные и несущественные признаки и причинно-следственные связи. В ответе отсутствуют выводы. Умение раскрыть значение обобщенных знаний не показано. Речевое оформление требует поправок, коррекции. Допущены ошибки при решении задачи и выполнении упражнений.
Оценка «неудовлетворительно»
Ответ представляет собой разрозненные знания с существенными ошибками по вопросу. Присутствуют фрагментарность, нелогичность изложения. Студент не осознает связь обсуждаемого вопроса по билету с другими объектами дисциплины. Отсутствуют выводы, конкретизация и доказательность изложения. Речь неграмотная, химическая терминология не используется. Дополнительные и уточняющие вопросы преподавателя не приводят к коррекции ответа студента. Задача и упражнения не решены.
|
|
|
Вспомогательный материал к билетам: (лично для вас!!!)
Mg → MgO → MgCl2 → Mg(OH)2 → MgO → Mg
2Mg + O2 = 2MgO
MgCl2 + 2NaOH = Mg(OH)2 + 2NaCl
Mg(OH)2 = MgO + H2O
MgO + H2 = Mg + H2O

Эектролиз раствора ацетата калия:
K(-) (K+) – не восстанавливается, щелочной металл
2H2O + 2ē = H2+ 2OH– | 2
А(+) 2CH3COO––2ē = CH3-CH3 + 2CO2 | 2
Суммарное уравнение:
2CH3COO– + 2H2O = H2+ 2OH– + CH3-CH3 + 2CO2
Или 2CH3COOK + 2H2O = H2+ 2KOH + CH3-CH3 + 2CO2
При нагревании этана в присутствии катализатора Ni, Pt, происходит дегидрирование, X – этен: CH3-CH3  CH2=CH2 + H2
CH2=CH2 + H2
Следующая стадия – гидратация этена:
CH2=CH2 + H2O  CH3-CH2OH;
CH3-CH2OH;
Перманганат калия в кислой среде – сильный окислитель и окисляет спирты до карбоновых кислот:
5C2H5OH + 4KMnO4 + 6H2SO4 = 5CH3COOH + 4MnSO4 + 2K2SO4 + 11H2O
Наконец, взаимодействие уксусной кислоты и спирта приведет к образованию сложного эфира:
CH3COOH + C2H5OH = CH3COOC2H5 + H2O
Задание 2
1) CaC2 + 2H2O → Ca(OH)2 + C2H2
2) C2H2 + H2O 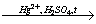 CH3СHO
CH3СHO
3) 5CH3СHO + 2KMnO4 + 3H2SO4 → 5CH3COOH + K2SO4 + 2MnSO4 + 3H2O
4) 2CH3COOH + CaCO3 → (CH3COO)2Ca + H2O + CO2
5) (CH3COO)2Ca  CaCO3 + (CH3)2CO
CaCO3 + (CH3)2CO
Задание 3
1) Al4C3 + 12H2O= 3CH4 + 4 Al(OH)3
2) 2 CH4C2H2 + 3H2
3) C2H2 + H2O 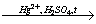 CH3СHO
CH3СHO
4) 3CH3СHO + 2KMnO4 + 3H2O → 2CH3COOK+ CH3COOH+ 2MnO2 + H2O
5) CH3COOK + KOH  CH4 + K2CO3
CH4 + K2CO3
Задание 4
1) CaC2 + 2H2O → Ca(OH)2 + C2H2
2) C2H2 + H2O 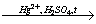 CH3СHO
CH3СHO
3) 5CH3СHO + 2KMnO4 + 3H2SO4 → 5CH3COOH + K2SO4 + 2MnSO4 + 3H2O
4) 2CH3COOH + Cl2 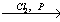 CH2ClCOOH + HCl
CH2ClCOOH + HCl
5) CH2ClCOOH + NH3 CH2(NH2)COOH + HCl
20) CaC2  X1
X1  X2→ H3C–COOH
X2→ H3C–COOH  X3→ (CH3)2–C=O
X3→ (CH3)2–C=O
Задание 5
1) CaC2 + 2H2O → Ca(OH)2 + C2H2
2) Н-С≡С-Н  H3C – COH
H3C – COH
3) H3C–COH +2Сu(ОН)2 → H3C–COOH +Сu2О + 2Н2О
4) 2H3C–COOH + Ba(OH)2 →(СН3COO)2Ba + 2Н2О
5) (СН3COO)2Ba (к)  (CH3)2–C=O + BaCO3
(CH3)2–C=O + BaCO3
Задание 6
1) Н-С≡С-Н  H3C – COH
H3C – COH
2) 5CH3СHO + 2KMnO4 + 3H2SO4 → 5CH3COOH + K2SO4 + 2MnSO4 + 3H2O
3) H3C–COOH + NaOH→СН3COONa + Н2О
4) СН3COONa + CH3I СН3COOCH3 + NaI
5) СН3COOCH3 + H2O  CH3COOH + CH3OH
CH3COOH + CH3OH
Задание 7
1) CH3OK+ H2O 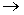 KOH + CH3OH
KOH + CH3OH
2) CH3OH + HBr 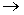 CH3Br + H2O
CH3Br + H2O
1) CaC2 + 2H2O → Ca(OH)2 + C2H2
2) C2H2 + H2 → C2H4
3) C2H4 + H2 → С2H6
4) 2С2H6 + 7O2 → 4CO2 + 6H2O
Цепочка превращений:
CaC2 → C2H2 → C2H4 → С2H6 → CO2
Химические уравнения (органическая химия)
3) 2CH3Br + 2Na  С2H6 + 2NaBr
С2H6 + 2NaBr
4) С2H6  C2H4 + H2
C2H4 + H2
5) 2C2H4 + O2  2CH3CHO
2CH3CHO
Тип реакции может подсказать сравнение состава исходного и получаемого веществ. Так, для первого превращения видно, что необходимо окислить альдегид в щелочной среде, например:
CH3CHO + 2KMnO4 + 3KOH CH3COOK + 2K2MnO4 + 2H2O
CH3COOK + HCl = CH3COOH + KCl
CH3COOH + C2H5OH  CH3COOC2H5 + H2O
CH3COOC2H5 + H2O
Чтобы из эфира получить ацетат, надо провести его гидролиз в щелочной среде, причем в качестве щелочи взять гидроксид кальция:
2CH3COOC2H5 + Ca(OH)2  (CH3COO)2Ca + 2C2H5OH
(CH3COO)2Ca + 2C2H5OH
Особую сложность может вызвать последнее превращение, поскольку способы получения кетонов в базовом курсе химии обычно не рассматриваются. Для его осуществления проводят пиролиз (термическое разложение) ацетата кальция:
(CH3COO)2Ca  (CH3)2CO + CaCO3
(CH3)2CO + CaCO3
Задание 9
1) CH3CHO + H2  C2H5OH
C2H5OH
2) C2H5OH + HBr C2H5Br + H2O
3) C2H5Br + KOH (спирт) C2H4 + KBr + H2O
4) 2C2H4 + O2  2 CH3CHO
2 CH3CHO
5) CH3CHO + Ag2O + NH3 CH3COONH4 + 2Ag
Задание 10:
1) CH3COOH + KOH CH3COOK + H2O
2) CH3COOK + 2H2O 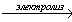 H2+ 2KOH + CH3-CH3 + 2CO2
H2+ 2KOH + CH3-CH3 + 2CO2
3) CH3-CH3 + Cl2  CH3-CH2Cl + HCl
CH3-CH2Cl + HCl
4) CH3-CH2Cl + NaOH (водн) CH3-CH2-OH +NaCl
5) 2CH3-CH2-OH  H2O + CH3-CH2-O-CH2-CH3
H2O + CH3-CH2-O-CH2-CH3
Задание 11
1) C2H5OH  CH2=CH2 + H2O
CH2=CH2 + H2O
2) 3CH2=CH2 + 2KMnO4 + 4H2O 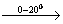 3CH2OH-CH2OH + 2MnO2 + 2KOH
3CH2OH-CH2OH + 2MnO2 + 2KOH
3) CH2OH-CH2OH + 2HBr 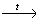 CH2BrCH2Br +2H2O
CH2BrCH2Br +2H2O
4) CH2BrCH2Br +2KOH (спирт) 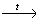 Н-С≡С-Н + 2H2O +2KBr
Н-С≡С-Н + 2H2O +2KBr
5) Н-С≡С-Н +H2O 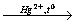
Задание 12
1) CH2BrCH2CH2Br + Zn 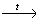 CH2=CH2CH3 + ZnCl2
CH2=CH2CH3 + ZnCl2
2) CH2=CH2CH3+ HBr 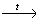 CH3-CH2BrCH3
CH3-CH2BrCH3
3) CH3-CH2BrCH3 +KOH (спирт) CH2=CH2CH3 + KBr
4) CH2=CH2CH3 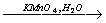 CH2(OH)-CH(OH)-CH3
CH2(OH)-CH(OH)-CH3
5) CH2(OH)-CH(OH)-CH3 + 2HBr  CH2BrCH2BrCH3 + 2H2O
CH2BrCH2BrCH3 + 2H2O
Задание 13
1) 2CH4 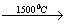 C2H2 + 3H2
C2H2 + 3H2
2) 3C2H2  C6H6
C6H6
3) C6H6 + CH3Cl  C6H5CH3 + HCl
C6H5CH3 + HCl
4) C6H5CH3  C6H5-COOH
C6H5-COOH
5) C6H5-COOH 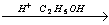 C6H5-COOC2H5 +H2O
C6H5-COOC2H5 +H2O
Задание 14
1) Al4C3 + 12H2O= 3CH4 + 4 Al(OH)3
2) 2CH4  C2H2 + 3H2
C2H2 + 3H2
3) 3C2H2  C6H6
C6H6
4) C6H6 + CH3Cl  C6H5CH3 + HCl
C6H5CH3 + HCl
5) C6H5CH3 + Cl2  C6H5CH2Cl +HCl
C6H5CH2Cl +HCl
Задание 15:
1) H2CCl-CH2-CH3 + KOH (водн) KCl + H2COH-CH2-CH3
2) H2COH-CH2-CH3 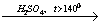 H2C=CH2-CH3 + H2O
H2C=CH2-CH3 + H2O
3) H2C=CH2-CH3 + HCl H3C-CH2Cl-CH3
4) H3C-CH2Cl-CH3 + KOH (спирт) H2C=CH2-CH3 + KCl
5) 
Задание 16 и 17
1) С2H4 + Cl2 CH2Cl-CH2Cl
2) CH2Cl-CH2Cl + 2KOH (спирт) C2H2 +2KCl + 2H2O
3) 3C2H2  C6H6
C6H6
4) C6H6 + CH3Cl  C6H5CH3 + HCl
C6H5CH3 + HCl
5) 5H3C–C6H5+6КМnО4 + 9Н2SO4→ 5C6H5CООН +3К2SO4+ 6МnSО4+14Н2O (возможно использование другого окислителя)
Задание 18:
1) CH3CH2CH2OH + НСl→ CH3CH2CH2Сl + Н2O
2) CH3CH2CH2Сl + 2Nа  C6H14 +2NаСl
C6H14 +2NаСl
3) C6H14  C6H6 + 4Н2
C6H6 + 4Н2
4) C6H6 + СН3Сl  H3C–C6H5+ НСl
H3C–C6H5+ НСl
5) 5H3C–C6H5+6КМnО4 + 9Н2SO4→ 5C6H5CООН +3К2SO4+ 6МnSО4+14Н2O (возможно использование другого окислителя)
Задание 19
1) 3C2H2  C6H6
C6H6
2) C6H6 + С2Н5Cl  HCl+ C6H5С2Н5
HCl+ C6H5С2Н5
3) C6H5С2Н5 + Br2 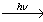 C6H5СНBrСH3 + HBr
C6H5СНBrСH3 + HBr
4) C6H5СНBrСH3 + KOH (спирт) 
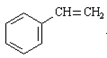 + KBr + H2O
+ KBr + H2O
5) 3  +2KMnO4 + 4H2O
+2KMnO4 + 4H2O 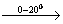 3
3  + 2MnO2 + 2KOH
+ 2MnO2 + 2KOH
Задание 20
1) 3C2H2  C6H6
C6H6
2) C6H6 + С2Н5Cl  HCl+ C6H5С2Н5
HCl+ C6H5С2Н5
3) C6H5С2Н5 + Cl2 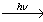 C6H5СНClСH3 + HCl
C6H5СНClСH3 + HCl
4) C6H5СНClСH3 + KOH (спирт) 
 + KCl + H2O
+ KCl + H2O
5) n ( 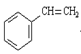 )
) 

Задание 21
1) C6H6 + CH3Cl  C6H5CH3 + HCl
C6H5CH3 + HCl
2) 5H3C–C6H5+6КМnО4 + 9Н2SO4→ 5C6H5CООН +3К2SO4+ 6МnSО4+14Н2O
3) C6H5CООН + CH3OH  C6H5CООCH3 +H2O
C6H5CООCH3 +H2O
4) C6H5CООCH3 + NaOH  C6H5CООNa + CH3OH
C6H5CООNa + CH3OH
5) 2CH3OH  CH3-O-CH3 + H2O
CH3-O-CH3 + H2O
Задание 22:
1) C6H12O6 2C2H5OH + 2CO2 (р-я идет в присутствии ферментов)
2) C2H5OH + HCl C2H5Сl + H2O
3) C2H5Сl + C6H6  CH3–CH2–C6H5
CH3–CH2–C6H5
4) CH3–CH2–C6H5 + Сl2  CH3–CH2–C6H4Cl + HCl
CH3–CH2–C6H4Cl + HCl
5) CH3–CH2–C6H4Cl + 6[O] C6H4Cl–COOH + 2H2O + CO2
Задание 23:
1) 3C2H2  C6H6
C6H6
2) C6H6 + Cl2  C6H5Cl + HСl
C6H5Cl + HСl
3) C6H5Cl + CH3Cl + 2Na  C6H5CH3 + 2NaCl
C6H5CH3 + 2NaCl
4) C6H5CH3 + HNO3 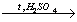 NO2–C6H4–CH3 + H2O
NO2–C6H4–CH3 + H2O
5) 5NO2–C6H4–CH3 + 6КМnО4 + 9Н2SO4→ 5NO2–C6H4–CООН +3К2SO4+ 6МnSО4 + 14Н2O (возможно использование другого окислителя)
Задание 24:
1) CH3-CH2-CH(CH3)-CH3 + Br2  CH3-CH2-CBr(CH3)-CH3 + HBr
CH3-CH2-CBr(CH3)-CH3 + HBr
2) CH3-CH2-CBr(CH3)-CH3 + KOH  CH3-CH2=C(CH3)-CH3 + H2O +KBr
CH3-CH2=C(CH3)-CH3 + H2O +KBr
3) CH3-CH2-CBr(CH3)-CH3 + HBr  CH3-CH2-CBr(CH3)-CH3
CH3-CH2-CBr(CH3)-CH3
4) CH3-CH2-CBr(CH3)-CH3 + 2Na  2NaBr +
2NaBr +
5) 2C10H22 + 31 O220 CO2 + 22 H2O
Задание 25:
CH4 + O2 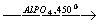 HCHO + H2O
HCHO + H2O
HCHO + H2  CH3OH
CH3OH
2CH3OH + 2Na2CH3ONa +H2
CH3ONa + HCl CH3OH +NaCl
5CH3OH + 2KMnO4 +3H2SO4  5HCHO + 2MnSO4 + K2SO4 + 8H2O
5HCHO + 2MnSO4 + K2SO4 + 8H2O
Задание 26:
1) CH3COO-CH2CH2CH3 +KOH  CH3COOK + CH2CH2CH3OH
CH3COOK + CH2CH2CH3OH
2) CH3COOK + KOH  CH4 + K2CO3
CH4 + K2CO3
3) 2CH4  C2H2 + 3H2
C2H2 + 3H2
4) C2H2 + CH3COOH  СН3СООСН=СН2 +H2O
СН3СООСН=СН2 +H2O
5) СН3СООСН=СН2 + Br2 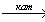 СН3СООСНBr-СН2Br
СН3СООСНBr-СН2Br
Задание 27:
1) CH3-CH2-CHO + 2Сu(OH)2 CH3-CH2-COOH + Сu2О + 2Н2О
2) CH3-CH2-COOH + Cl2  CH3-CHCl-COOH + HCl
CH3-CHCl-COOH + HCl
3) CH3-CHCl-COOH +NaOH (спирт) CH2=CH-COOH +NaCl + H2O
4) CH2=CH-COOH + CH3OH 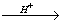 CH2=CH-COOCH3 + H2O
CH2=CH-COOCH3 + H2O
5) nCH2=CH-COOCH3 
Задание 28:
Смотри ответ на задание №1
Сложность данной цепочки в том, что если не знать первой реакции, понять о каких веществах идет речь в остальной ее части невозможно.
Задание 29:
C2H5OH  CH2=CH2+H2O
CH2=CH2+H2O
CH2=CH2  HC≡CH + H2
HC≡CH + H2
HC≡CH + 2[Ag(NH3)2]OH AgC≡CAg +4NH3 + 2H2O
AgC≡CAg + 2HCl HC≡CH + 2AgCl
3HC≡CH + 8KMnO4 3K2C2O4 + 2KOH + 2H2O + 8 MnO2
Дата добавления: 2021-05-18; просмотров: 54; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!
