Выполнение лабораторной работы.
Конспект урока изучения нового материала в 10 классе
По теме «Химические свойства многоатомных спиртов».
Автор: Табачная Ольга Вячеславовна, учитель химии МБОУ лицей № 2, г. Бугульма, Республика Татарстан
Описание материала: конспект урока для учащихся 10 класса с углубленным изучением химии (химико – биологический класс). По тематическому планированию это урок № 49 в теме 6 – спирты и фенолы. По теме «Многоатомные спирты» - это второй урок. На уроке осуществляется фронтальный опрос, индивидуальная работа, работа в парах при выполнении лабораторной работы, использование презентации, демонстрация видеофрагментов (при необходимости)
| Тема | Физические и химические свойства многоатомных спиртов |
| Цель | Сформировать у учащихся понятие об особых свойствах многоатомных спиртов через организацию исследовательской деятельности на уроке |
| Задачи | ü рассмотреть физические и химические свойства многоатомных спиртов на примере этиленгликоля и глицерина; ü выявить общие и специфические свойства многоатомных спиртов; ü развивать навыки анализа, планирования деятельности, умение прогнозировать результат при выполнении химического эксперимента, умение работать в парах. ü обеспечить формирование познавательных, коммуникативных, регулятивных универсальных учебных действий обучающихся; ü использовать возможности ИКТ и информационных источников при выполнении домашних заданий и представлении результатов. ü создание условий для применения знаний и умений в практической деятельности и повседневной жизни ü создание условий для осознания необходимости грамотного отношения к своему здоровью и окружающей среде. |
| Планируемый результат | · Знать физические свойства этиленгликоля и глицерина; · Знать отличительные особенности химических свойств многоатомных спиртов; · Знать и соблюдать правила техники безопасности при выполнении лабораторной работы; · Уметь объяснять сходство и отличие в химических свойствах одно – и многоатомных спиртов; · Уметь отличать многоатомные спирты от представителей других классов с помощью качественных реакций; · Уметь объяснять механизм реакций, объясняющих химические свойства многоатомных спиртов и писать уравнения данных химических реакций; · Уметь использовать возможности ИКТ для получения необходимой информации |
| Основные понятия | · Многоатомные спирты; · Функциональная группа; · Кислотные свойства; · Основные свойства; · Качественная реакция; |
| Межпредметные связи | Биология, история. |
| Ресурсы: основные дополнительные | Новошинский И.И., Новошинская Н.С. Органическая химия: учебник для 10 (11) класса общеобразовательных учреждений: профильный уровень. – М.: ООО «Русское слово – учебник», 2010. – 368 с.: ил. Дополнительная литература ü Болтромеюк В.В. Органическая химия: пособие для подготовки к централизованному тестированию. – Минск: Тетра – Системс, 2013. – 256 с ü Горковенко М.Ю. Поурочные разработки по химии к учебным комплектам О.С.Габриеляна и др., Г.Е.Рудзитиса и др., Л.С.Гузея и др. 10 (11) класс. М.: «ВАКО» - 320 с. (В помощь школьному учителю) ü Журнал «Химия в школе» ü Фестиваль педагогических идей. Открытый урок. http://festival.1september.ru/ ü Электронная химическая библиотека http://himlib.ru/index.php?book=6&page=265 ü Социальная сеть работников образования http://nsportal.ru/ ü Сеть творческих учителей/химоза http://www.it-n.ru/ ü Википедия – свободная энциклопедия ü ХиMuК.ru – химическая энциклопедия |
| Организация пространства | Индивидуальная и фронтальная работа, работа в парах (поведение лабораторной работы, взаимопроверка, взаимопомощь). |
| Приемы и средства обучения: | Опора на имеющиеся знания обучающихся, сравнение и анализ, компьютер, мультимедийный проектор, презентация, видеоопыты, проведение лабораторных опытов. |
| Оборудование | Компьютер, мультимедийный проектор. На столах учащихся лотки с реактивами: штатив с пробирками, этиленгликоль или глицерин (по группам), этанол, раствор гидроксида натрия, раствор сульфата меди (II), вода, инструктивные карточки для проведения опытов. |
| Виды учебной деятельности обучающихся | Коммуникативные УУД: - обеспечение возможности сотрудничества: умение слышать, слушать и понимать партнера, оказывать поддержку друг другу и эффективно сотрудничать как с учителем, так и со сверстниками, построение речевых высказываний, работа с информацией, построение вопросов. Личностные УУД: готовность и способность обучающихся к саморазвитию, мотивации к обучению и познанию, самоопределение, ценностно - смысловые установки обучающихся, отражающие их индивидуально-личностные позиции, социальные компетенции, личностные качества; Регулятивные УУД – целеполагание, самоконтроль, самооценка. Познавательные УУД – общие учебные действия, подготовка и решение практических задач, овладение межпредметными понятиями, расширение опыта специфического для предметной области (химии), деятельности по получению нового знания, его преобразованию и применению, а также систему основополагающих элементов научного знания, лежащих в основе современной научной картины мира. |
| Этапы урока | 1. Организационный момент 2. Мотивация 3. Актуализация опорных знаний 4. Изучение нового материала 5. Выполнение лабораторной работы 6. Домашнее задание 7. Рефлексия |
|
|
|
|
|
|
|
|
|
|
|
|
Ход урока
Организационный момент.
Учитель: здравствуйте ребята, садитесь.
Мотивация
Учитель: в своё время французский писатель и философ эпохи возрождения Мишель де Монтень сказал: «Нет стремления более естественного, чем стремление к знаниям». Этими словами мне хочется начать наш урок. Я думаю, что в результате сегодняшнего занятия ваше стремление будет реализовано полностью.
Актуализация опорных знаний.
Учитель: на прошлом уроке мы начали изучать материал о многоатомных спиртах. Итак, вспомним изученный материал:
Общие способы получения многоатомных спиртов у доски выполняют два ученика (после выполнения задания – объясняют своё решение)
Фронтальный беседа (блиц - опрос) по вопросам:
1. В чём сходство одно – и многоатомных спиртов?
2. В чём отличие одно – и многоатомных спиртов?
3. В чём отличие в названиях многоатомных спиртов?
4. Какие спирты называются гликолями?
5. Каково систематическое название этиленгликоля, глицерина?
6. Как по физическим свойствам отличить многоатомные спирты от одноатомных?
7. У каких спиртов, одно – или многоатомных, сильнее выражены кислотные свойства? Почему?
8. Как получают глицерин?
9. Как получают этиленгликоль?
10. Какие химические свойства характерны для этанола как представителя одноатомных спиртов?
Изучение нового материала
Учитель: многоатомные спирты обладают аналогичными, по сравнению с одноатомными спиртами, свойствами. Но они, в отличие от последних, вступают в реакции как с участием одной, так и нескольких гидроксильных групп (в зависимости от молярного соотношения исходных веществ и условий проведения реакции).
1 свойство: взаимодействие со щелочными металлами.
Этиленгликоль при этом образует однозамещённый гликолят
2HO—CH2—CH2—OH + 2Na → 2HO—CH2—CH2—ONa + H2 (вещества в эквивалентном соотношении)
или двухзамещённый гликолят: HO—CH2—CH2—OH + 2Na → NaO—CH2—CH2—ONa + H2 (натрий в избытке)
Глицерин в такой реакции образует глицераты трёх типов: моно – ди – и тризамещённые глицераты
Демонстрационный опыт: Учитель демонстрирует взаимодействие глицерина с натрием, а учащиеся самостоятельно пишут реакцию с образованием трёхзамещённого глицерата натрия, с последующей проверкой (если невозможно провести демонстрацию, можно заменить видеофрагментом)
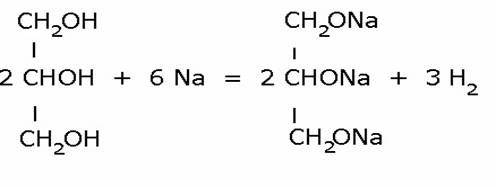
2 свойство: взаимодействие с растворами щелочей – свойство, отличное от свойств одноатомных. Это доказывает более сильные кислотные свойства многоатомных спиртов. В данных реакциях образуются только моноалкоголяты. Ди- и триалкоголяты не образуются, так как они подвергаются гидролизу с образованием монозамещённого продукта.
CH2-OH CH2-O-Na CH2-OH CH2-O-Na
│ │ │ + NaOH → │ + H2O
CH-OH + NaOH → CH-OН + H2O CH2-OH CH2-OH
│ │
CH2-OH CH2-OН
3 свойство: взаимодействие с гидроксидом меди (II). Эта реакция используется для качественного определения многоатомных спиртов.
Выполнение лабораторной работы.
Учащиеся выполняют лабораторный опыт по инструктивной карточке, записывают наблюдения.
Инструктивная карточка: в трёх пробирках (I, II, III) получите гидроксид меди (II) при взаимодействии гидроксида натрия с сульфатом меди (II). К полученному голубому осадку (во все пробирки) по каплям добавляйте этанол (в I), этиленгликоль (во II), глицерин (в III). Пробирки периодически встряхивайте. Отметьте, какие изменения и в каких пробирках вы наблюдаете.
Учащиеся отмечают растворение осадка гидроксида меди (II) и образование раствора тёмно - синего цвета в пробирках II и III.
Учитель: запишем уравнения данных реакций:
Для глицерина:
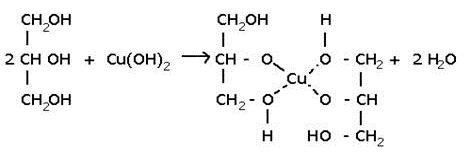
пунктирными линиями показаны связи, образованные по донорно – акцепторному механизму.
В упрощённом виде эта реакция выглядит так:

Для этанола эта реакция не характерна, для этиленгликоля – возможна:
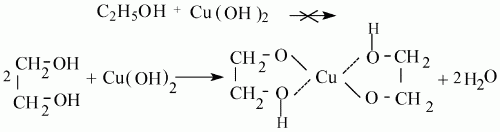 тёмно – синий раствор гликолята меди (II)
тёмно – синий раствор гликолята меди (II)
В упрощённом виде эта реакция выглядит так:
CH2-OH CH2 - O
│ + Cu (OH) → │ Cu + H2O
CH2-OH CH2 - O
4 свойство: образование сложных эфиров при взаимодействии с карбоновыми и минеральными кислотами. В реакции может принимать участие разное число гидроксильных групп, в зависимости от молярного соотношения реагентов.
Вопрос учителя: как называется данная реакция? При каких условиях она осуществляется?
Ответ учащихся (возможный): данная реакция называется реакцией этерификации. Она происходит в присутствии минеральных кислот.
CH2-OH О CH2-OH О
│ + ║ ↔ │ ║ + H2O
CH2-O- H Н – О – С – С2Н5 CH2 - O – С – С2Н5 ацетилгликолят
В качестве исходных реагентов в данных реакциях часто используют не сами кислоты, а их ангидриды или галогенангидриды:
О О
║ ║
CH2- O - H + Cl - С – СН3 CH2 - O - С – СН3
О О
║ ║
CH- O - H + Cl - С – СН3 → CH - O - С – СН3 + 3 HCl
О О
║ ║
CH2- O - H + C l - С – СН3 CH2 - O - С – СН3 триацетил (триглицерид уксусной кислоты)
Из сложных эфиров, образованных многоатомными спиртами и неорганическими кислотами, наиболее известен нитроглицерин, или тринитрат глицерина, или тринитроглицерид (нитроглицерин).
CH2- O - H + Н - О - NO2 CH2 - O - NO2
CH- O - H + Н - О - NO2 → CH - O - NO2 + 3 H2O
CH2- O - H + Н - О - NO2 CH2 - O - NO2
В чистом виде это тяжёлая маслянистая жидкость.
Вопрос учителя: что вам ещё известно о данном веществе?
Ответ учащихся (возможный): тринитроглицерин используется как взрывчатое вещество, а также используется в медицине.
Дополнение учителя: нитроглицерин взрывается при сотрясении или ударе, при этом образуется большое количество газообразных веществ:
CH2 - O - NO2
4 CH - O - NO2 → N2 + 12 СО2 + О2 + 10 Н2О
CH2 - O - NO2
Для безопасности при приготовлении взрывчатых веществ (динамита, различных видов пороха) его используют не в чистом виде, а в смеси с различными пористыми веществами (древесный уголь песок, глина, туф (легкая, сцементированная, пористая горная порода), инфузорная земля (скопления кремнеземистых панцирей диатомовых водорослей и других микроскопических организмов) и пр.).
Динамит был изобретён Альфредом Нобелем в Гамбурге в 1867 году.
В медицине нитроглицерин используется в качестве сосудорасширяющего средство при заболеваниях сердца (стенокардии)
5 свойство: многоатомные спирты, как и одноатомные, вступают в реакции дегидратации, при этом образуются разные продукты:
А) при внутримолекулярной дегидратации этиленгликоля сначала образуется виниловый спирт, а затем уксусный альдегид О
║
СН2 – СН – ОН → [Н2С = СН – ОН] → СН3 - С - Н
│ │ - Н2О виниловый спирт уксусный альдегид
ОН Н
Б) при межмолекулярной дегидратации этиленгликоля могут образовываться продукты циклического строения:
СН2 – О – Н Н – О – СН2 СН2 – О – СН2
│ + → │ │
СН2 – О – Н Н – О – СН2 СН2 – О – СН2 1,4 – диоксан (диэтилендиоксид)
1,4 – диоксан 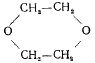 способен проникать в кожу человека через шампунь, пену для ванн и другие средства гигиены. Учёными он рассматривается как возможный человеческий канцероген, способный принести вред при многократном использовании средств, его содержащих.
способен проникать в кожу человека через шампунь, пену для ванн и другие средства гигиены. Учёными он рассматривается как возможный человеческий канцероген, способный принести вред при многократном использовании средств, его содержащих.
Также при межмолекулярной дегидратации могут образоваться продукты линейного строения:
СН2 – СН2 – О – Н + Н – О – СН2 – СН2 → СН2 – СН2 – О – СН2 – СН2 + Н2О
│ │ │ │
ОН ОН ОН ОН
При межмолекулярной дегидратации глицерина при действии слабых водоотнимающих средств могут образовываться полиглицериновые алкоголи, например 
Вопрос учителя: к какому классу веществ мы можем отнести полученное соединение?
Ответ учащихся (возможный): данное соединение можно отнести как к двухатомным спиртам, так как оно содержит две гидроксогруппы, так и к простым эфирам, та как есть группа – О – .
При действии сильных водоотнимающих средств (KHSO4, H3BO3, безводный MgSO4) из глицерина получается акролеин:
CH2 – ОН
│ KHSO4 O
СН – ОН CH2 = CH – C
│ H
CH2 – ОН
6 свойство: многоатомные спирты взаимодействуют с галогеноводородами.
Вопрос учителя: о проявлении каких свойств многоатомных спиртов свидетельствует данная реакция? Между какими атомами в спиртах будет происходить разрыв связи?
Ответ учащихся (возможный): взаимодействие многоатомных спиртов с галогеноводородами говорит о проявлении основных свойств. В данных реакциях в спирте будет разрываться связь С – ОН.
Дополнение учителя: так как гидроксильные группы влияют друг на друга, замещение на галоген каждой последующей гидроксильной группы происходит труднее.
СН2 – О – Н СН2 – Br СН2 – Br
│ + HBr → │ + HBr → │
СН2 – О – Н - H2O СН2 – ОH - H2O СН2 – Br
этандиол – 1,2 2 - бромэтанол 1,2 – дибромэтан
Как и в случае одноатомных спиртов, в данных реакциях лучше использовать не галогеноводороды, а хлориды фосфора (PCl3, PCl5) или тионилхлорид (SOCl2):
CH2 - OH CH2 - Cl CH2 - OH CH2 – Cl
│ │ │ │
CH - OH + 3 PCl5 → CH - Cl + 3 POCl3 + 3 HCl или CH - OH + 3 SOCl2 → CH – Cl + 3 SO2 + 3 HCl
│ │ │ │
CH2 - ОН CH2 – Cl CH2 - OH CH2 - Cl
7 свойство: многоатомные спирты подвергаются окислению, причём этот процесс происходит сложно, многостадийно и в зависимости от условий проведения реакции и природы окислителя будут образовываться разные продукты. Так при окислении этиленгликоля в кислой среде гидроксогруппы сначала образуют альдегидные группы, а конечным продуктом является щавелевая кислота.  В нейтральной и щелочной среде образуются соли щавелевой кислоты – оксалаты.
В нейтральной и щелочной среде образуются соли щавелевой кислоты – оксалаты.
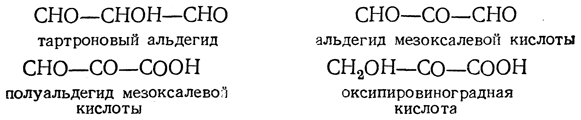
Глицерин, являясь одновременно и первичным, и вторичным спиртом, в зависимости от условий окисляется сначала с образованием кето – или альдегидных групп, которые затем превращаются в карбоксильные, что приводит к образованию набора различных веществ:

Можно предполагать образование также следующих продуктов:
8 свойство: при сильном нагревании в присутствии кислорода многоатомные спирты горят с образованием углекислого газа и воды.
Домашнее задание
1) Записи в тетради.
2) Записать уравнение реакции горения: 1 вариант – этиленгликоля; 2 вариант – глицерина
3) Записать уравнение реакции окисления: 1 вариант – глицерина перманганатом калия в кислой среде с образованием глицериновой кислоты; 2 вариант – этиленгликоля дихроматом калия в кислой среде до щавелевой кислоты. Реакции уравнять методом электронного баланса.
4) Из учебника: §32, упр. 1,3 устно, упр. 4 или 6 (на выбор),5 письменно
Рефлексия
Закончите одно из предложений:
1) На уроке мне было понятно…………
2) Из сегодняшнего материала мне не совсем понятно……
3) Для более полного понимания сегодняшней темы мне нужно……..
4) На сегодняшнем уроке…….
·
В заключение сегодняшнего урока я надеюсь, что слова Жана Батиста Мольера « Как приятно знать, что ты что-то узнал» в какой – то мере каждый из вас может отнести к себе.
Дата добавления: 2021-04-24; просмотров: 125; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!
