Закрепление нового материала.
Проверка знаний по ранее изученному материалу
Химический диктант.
Вы уже многое знаете о кислородсодержащих органических соединениях. Предлагаю вам проверить свои знания в ходе выполнения небольшого химического диктанта (если вы согласны с утверждением, ставите цифру 1, если нет – цифру 0). Цифры записывайте в строчку:
1. В молекулах одноатомных спиртов углеводородный радикал связан с одной гидроксогруппой.
2. Глицерин относится к многоатомным спиртам.
3. Качественной реакцией на многоатомные спирты является реакция с Cu(OH)2.
4. Для одноатомных спиртов характерна реакция гидрирования.
5. Из альдегида можно получить одноатомный спирт реакцией гидрирования.
6. Для альдегидов характерна реакция «серебряного зеркала».
7. При взаимодействии альдегидов с Cu(OH)2 (при нагревании) образуются карбоновые кислоты.
8. В состав одноосновных предельных карбоновых кислот входит карбоксильная функциональная группа.
9. Карбоновые кислоты, как и неорганические, взаимодействуют с металлами, оксидами металлов, основаниями, солями слабых кислот, спиртами.
10. Хлоруксусная кислота является более сильной, чем уксусная.
11. Все животные жиры – твердые.
12. Сложные эфиры применяются в пищевой промышленности как ароматизаторы.
Проверьте свои ответы и выставьте себе оценку.
Код ответа: 111011101101.
«5» - все ответы правильные; «3» - 3-4 неверных ответа;
|
|
|
«4» - 1-2 неверных ответа; «2» - 5 и более неверных ответов
Изложение нового материала.
Углеводы, их состав и классификация.
Знакомством с углеводами мы завершаем изучение кислородсодержащих органических веществ. С соединениями этого класса вы уже знакомы из курса биологии и имеете представление о роли углеводов в природе, их значении для жизни. Сегодня мы рассмотрим классификацию углеводов и еще раз остановимся на их роли в природе, чтобы в конце урока мы смогли ответить на вопрос: «Что же значат углеводы для жизниКакие вещества называются углеводами?
1. Почему – «углеводы»? Исключения их общей формулы.
2. Классификация углеводов по способности гидролизоваться.
3. Моносахариды: пентозы, гексозы. Д.о. – глюкоза.
4. Дисахариды. Мальтоза, лактоза. Д.о. - сахароза
5. Полисахариды. Д.о. – крахмал, вата, древесина.
6. Роль углеводов в природе и жизни человека.
Углеводы - обширный класс природных соединений, которые играют важную роль в жизни человека, животных и растений.
Значение углеводов для живых организмов, для жизни трудно переоценить, они участвуют во всех жизненно важных процессах. Одна из важнейших реакций, протекающих в природе – реакция фотосинтеза. Ежегодно зеленые растения и бактерии поглощают в процессе фотосинтеза около 200 млрд. тонн углекислого газа. При этом в атмосферу высвобождается приблизительно 130 млрд. тонн кислорода и синтезируется 50 млрд. тонн органических соединений.
|
|
|
Углеводы аккумулируют солнечную энергию и сами являются источником энергии для живых организмов.
Название «углеводы» эти соединения получили потому, что состав многих из них выражается общей формулой Сn(H2O)m, т.е. формально являются соединениями углерода и воды. С развитием химии углеводов обнаружены соединения, состав которых не отвечает приведенной формуле, но обладающие свойствами веществ своего класса (например, дезоксирибоза С5Н10О4). В то же время есть вещества, соответствующие общей формуле углеводов, но не проявляющие их свойства (например, спирт инозит С6Н12О6).
Классификация углеводов
Все углеводы можно разделить на две группы: простые углеводы (моносахариды) и сложные углеводы.
Простые углеводы (моносахариды) – это простейшие углеводы, не гидролизующиеся с образованием более простых углеводов.
Сложные углеводы – это углеводы, молекулы которых состоят их двух или более числа остатков моносахаридов и разлагаются на эти моносахариды при гидролизе.
|
|
|
Одним из важнейших моносахаридов является глюкоза. Молекулярная формула глюкозы: С6Н12О6. Следовательно, глюкоза относится к кислородсодержащим органическим веществам.
Физические свойства и нахождение в природе
Глюкозу называют также виноградным сахаром, так как она содержится в большом количестве в виноградном соке. Кроме винограда глюкоза находится и в других сладких плодах и даже в разных частях растений.
Она является обязательным компонентом крови и тканей животных и непосредственным источником энергии для клеточных реакций. Уровень глюкозы в крови человека постоянен и находится в пределах 0,08-0,11%. Во всем объеме крови взрослого человека содержится 5-6 г. глюкозы. Такого количества достаточно для покрытия энергетических затрат организма в течение 15 мин. его жизнедеятельности. При некоторых патологиях, например, при заболевании сахарным диабетом, содержание глюкозы в крови повышается, и избыток её выводится с мочой. При этом количество глюкозы в моче может возрасти до 12% против обычного – 0,1%.
Глюкоза представляет собой бесцветное кристаллическое вещество, хорошо растворимое в воде, сладкое на вкус («глюкос» — сладкий).
|
|
|
Наиболее важная из кетоз- фруктоза. Она содержится во фруктах, в пчелином меде.
Строение.Особенности состава молекулы глюкозы мы рассмотрим в ходе лабораторного опыта.
Лабораторный опыт.
1) Получите гидроксид меди: к раствору гидроксида натрия прилейте несколько капель раствора сульфата меди (II), так, чтобы щелочь осталась в избытке; к осадку прилейте раствор глюкозы, встряхните пробирку. Что наблюдаете? (Получили ярко-синий раствор).
н.у.
C6H12O6 + Cu(OH)2 → ярко-синий раствор
? Для каких веществ эта реакция является качественной?
Вывод: глюкоза является многоатомным спиртом.
2) Нагрейте этот раствор. Обратите внимание на происходящие изменения:
t0 t0
ярко-синий раствор → желтый осадок → красный осадок
? Наличие какой группы в молекуле глюкозы доказали этой реакцией?
Вывод: глюкоза является альдегидом. (Слайд 12-13)
Из этих опытов делаем вывод: глюкоза является альдегидоспиртом.
В состав глюкозы входит 5 гидроксогрупп, это доказано реакцией ее с уксусной кислотой. Глюкоза образует сложный эфир с пятью молекулами уксусной кислоты.
Н Н Н ОН Н
| | | | |
Н ― С ― С ― С ― С ― С ― С = О или СН2ОН ― (СНОН)4 ― С = О
| | | | | | |
ОН ОН ОН Н ОН Н Н
Изомерия.
У глюкозы, как и у других органических соединений, есть изомер – фруктоза. Ее молекулярная формула такая же, как и у глюкозы – C6H12O6, но фруктоза является кетоноспиртом
СН2ОН ― (СНОН)3 ― С ― СН2ОН.
||
О
Химические свойства
Химические свойства моносахаридов обусловлены особенностями их строения.
Рассмотрим химические свойства на примере глюкозы.
1. Реакции с участием альдегидной группы глюкозы
а) восстановление (гидрирование) с образованием многоатомного спирта сорбита
СН=О СН2ОН
│ kat, t0 │
(СНОН)4 + Н2 → (СНОН)4
│ │
СН2ОН СН2ОН
б) окисление
реакция «серебряного зеркала»( с аммиачным раствором оксида серебра, t 0 ),
реакция с гидроксидом меди ( II ) Cu ( OH )2 в щелочной среде, t 0 )
CH=O COOH
│ NH4OH, t0 │
(CHOH)4 + Ag2O → (CHOH)4
│ │
CH2OH CH2OH
Продуктом окисления является глюконовая кислота (соль этой кислоты – глюконат кальция – известное лекарственное средство).
CH=O COOH
│ t0 │
(CHOH)4 + 2Cu(OH)2 → (CHOH)4 + Cu2O↓ + 2H2O
│ голубой │ кирпично-красный
CH2OH CH2OH
Эти реакции являются качественными на глюкозу как альдегид.
Под действием сильных окислителей (например, азотной кислоты) образуется двухосновная глюкаровая кислота.
CH=O COOH
│ t0 │
(CHOH)4 + HNO3 → (CHOH)4
│ │
CH2OH COOH
2. Реакция глюкозы с участием гидроксильных групп (т.е. свойства глюкозы как многоатомного спирта)
а) взаимодействие с Cu ( OH )2 на холоду с образованием глюконата меди (II) – качественная реакция на глюкозу как многоатомный спирт.
3. Брожение (ферментация) моносахаридов
а) спиртовое брожение
С6Н12О6 → 2С2Н5ОН + 2СО2
б) маслянокислое брожение
С6Н12О6 → СН3 ─СН2 ─СН2 ─СООН + 2Н2↑ + 2СО2↑
в) молочнокислое брожение
С6Н12О6 → 2СН3 ─ СН ─ СООН
│
ОН
Получение:
Глюкоза образуется в природе в процессе фотосинтеза, протекающего под действием солнечного света в листьях растений.
Суммарное уравнение фотосинтеза:
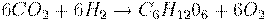
В живых организмах происходит окисление глюкозы под действием кислорода воздуха по обратной реакции:
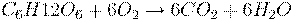
Применение:
- в медицине, микробиологической промышленности;
- для получения этанола;
- в кондитерской промышленности в составе патоки;
- для изготовления зеркал и елочных украшений;
- в текстильной промышленности.
Закрепление нового материала.
Задание 1
Из чего можно получить больше этилового спирта: из 1 кг глюкозы или 1 кг крахмала? Ответ обоснуйте, не прибегая к расчетам.
Ответ: из 1 кг крахмала, т.к. при его гидролизе образуется больше спирта, чем 1 кг глюкозы. Крахмал- полимер, мономерами которого являются молекулы глюкозы.
Задание 2
В среднем сладкоежки кладут 2 чайные ложки сахара на стакан чая. Зная, что в такой ложке помещается 7 г сахара, а объем стакана 200 мл, рассчитайте массовую долю сахарозы в растворе (плотность чая считать равной 1 г/мл).
Решение:
m (двух чайных ложек сахара) = 7+7= 14г;
m (чая) = ρ . V = 1г/мл ٠ 200мл = 200г;
m (раствора чая) = m (чая) + m (двух чайных ложек сахара) = 200г + 14г = 214г;
ω (сахарозы) = m (двух чайных ложек сахара) . 100% / m (раствора чая) = 14г ٠100% / 214г = 6,5%.
Ответ: ω (сахарозы) = 6,5%.
Задание 3
С помощью каких реакций можно осуществить следующие превращения:
Сахароза 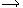 глюкоза
глюкоза 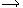 глюконовая кислота?
глюконовая кислота?
сахароза 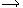 глюкоза:
глюкоза:
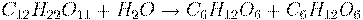
глюкоза 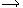 глюконовая кислота
глюконовая кислота
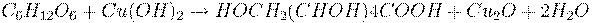
(реакцию проводить при нагревании!)
Резервное задание:
демонстрация опыта
В органическом анализе есть одна замечательная качественная реакция на углеводы. В нее вступают любые сахара: моно-, олиго-и полисахариды, растворимые и нерастворимые в воде, альдозы и кетозы, восстанавливающие и невосстанавливающие. Эта реакция называется пробой Молиша. Если в распоряжении учителя есть спиртовой раствор какого-либо из перечисленных ароматических гидрокси-соединений (резорцин, тимол, а-нафтол), он сумеет показать детям эту красивую реакцию.
В чисто вымытую пробирку наливают 1 мл воды и добавляют несколько крупинок сахарозы, или кристалликов глюкозы, или кусочек фильтровальной бумаги (целлюлоза). В раствор добавляют 2-3 капли раствора резорцина.
Пробирку закрепляют в штативе наклонно и по стенке осторожно наливают 1-2 мл концентрированной серной кислоты.
Пробирку поворачивают в вертикальное положение. В месте соприкосновения серной кислоты с водным раствором появляется красивое ярко-красное кольцо, свидетельствующее о наличие в исследуемой пробе углевода.
Итог:
Мы рассмотрели классификацию углеводов, физические и химические свойства глюкозы, ее реакции окисления (с гидроксидом меди (II), аммиачным раствором нитрата серебра), восстановления (водородом), особое свойство глюкозы – реакции брожения.
Домашнее задание:
1. Решить задачу: Даже великие химики нередко ошибались. Одним из первых определил элементный состав сахарозы А. Л. Лавуазье и получил следующие результаты: углерод — 28%, водород — 8%, кислород — 64%. Вычислите действительное содержание этих элементов в сахарозе, зная ее молекулярную формулу С12Н22О11.
2. Как распознать при помощи одного реактива глицерин, уксусный альдегид, уксусную кислоту, глюкозу? Напишите уравнения реакций
Литература:
1. Габриелян О. Химия 10кл.: Учебник для общеобразовательных учреждений. -М.:Дрофа,2009.-304с.
2. Габриелян, О. С., Остроумов, И. Г. Настольная книга учителя химии. 10 класс. - М.: Дрофа, 2001.-536с.
3. Кузьменко Н. Е., Еремин В. В. Начала химии. Современный курс для поступающих в ВУЗы.- М.: «Экзамен», 2001.-720с.
Дата добавления: 2021-04-15; просмотров: 127; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!
