Согласно правилам испытания иммунобиологических препаратов испытания должны выглядеть следующим образом:
- литературный обзор;
- выделение нового штамма вируса (согласно постулатам Коха);
- культивирование вирусного штамма;
- верификация вирусного штамма;
- постановка серии экспериментов, корректируемых по ходу получения новых данных;
- разработка и создание лабораторных количеств вакцины;
- доклинические испытания:
- установление токсичности;
- проверка мутагенного, канцерогенного и тератогенного эффектов;
- определение эффективности препарата и проверка эффекта антителозависимого усиления;
- установление оптимальной дозировки.
Для определения эффективности препарата необходимо две группы подопытных животных: иммунизированная и контрольная. Обе группы должны быть заражены патогеном, против которого сделана прививка, чтобы проверить, насколько разрабатываемый препарат защищает от заражения. В этом же исследовании следовало проверить и ADE эффект со вскрытием трупов погибших животных. Этого не было сделано при разработке всех рассматриваемых вакцин.
При использовании РНК-вакцин необходим контроль изменения экспрессии генов в различных тканях по сравнению с контрольной группой животных, после вакцинации и после заражения, если оно произошло.
В случае ДНК-вакцин на основе аденовирусных транспортеров необходим контроль опасности геномного редактирования, т.е. необходимо было провести генетический скрининг животных до вакцинации, затем вакцинировать и через несколько дней снова провести генетический скрининг тех же самых животных, причем по разным тканям, чтобы исключить или выявить тканеспецифичность.
|
|
|
При испытании любого типа иммунопрофилактического препарата следовало получить хотя бы одно поколение (лучше 2 – 5 с вакцинацией каждого поколения) здорового потомства от двух вакцинированных родителей и от гетерогенной по признаку вакцинации пары (вакцинированный/не вакцинированный).
Только после подробного исследования можно было переходить к клиническим испытаниям на людях. Чего в случае разработки вакцин, рассматриваемых в настоящем заключении, – не было.
ТЕПЕРЬ РАССМОТРИМ ПОРЯДОК ПРОВЕДЕНИЯ КЛИНИЧЕСКИХ ИСПЫТАНИЙ.
- I фаза клинических испытаний:
Предполагает от 20 до 100 добровольных участников. На этом этапе проводятся фактически все те же эксперименты, которые проводились прежде на животных, исключая все риски, основываясь на полученных прежде данных. Такое повторение исследований необходимо, поскольку результаты, полученные на животных, не всегда с точностью воспроизводятся на людях. Результаты, полученные на одной расе людей, могут быть невоспроизводимы на другой расе. Также необходимо брать во внимание особенности групп испытуемых (возраст, пол, статус здоровья и многое другое).
|
|
|
- II фаза клинических испытаний:
Возможно только после получения успешных результатов в ходе I фазы, предполагает от 100 до 500 участников
- III фаза клинических испытаний:
Предполагает несколько тысяч испытуемых.
- Масштабирование производства вакцин;
- Контроль качества;
- Регистрация;
- Постмаркетинговые испытания.
Весь цикл исследований должен занимать по научным данным от 5 до 15 лет [60;61;62;63;64;65;66;67;68;]
Вакцина — это, прежде всего, фармакологический препарат. И поскольку вакцинация – это, прежде всего, профилактика, а не лечение, то препарат назначается не больным, а здоровым людям, следовательно, и количество реципиентов этого препарата не сопоставимо больше, чем в случае с лекарственными препаратами. Тогда предъявляемая строгость к тестированию иммунопрофилактической продукции должна быть не меньше, а больше.
Для примера приведем небольшой расчет. Если какое-либо серьезное побочное явление проявляется всего лишь в 0,1% случаев, то для выявления одного такого случая нам нужно как минимум 1000 испытуемых. Но если такой препарат примут 1 миллиард человек, мы получим 1 миллион пострадавших!
|
|
|
При разработке любого фармакологического препарата необходимо сопоставление польза/вред, и перевес должен быть в сторону пользы. Существует градация допустимости тех или иных побочных эффектов. Например, такие нежелательные эффекты, как тошнота и рвота, допустимы при лечении тяжелых онкологических больных, но никак не допустимы при лечении, например, подростковых акне. С учетом того, что препараты для иммунопрофилактики предназначены для здоровых людей, стандартно допустимые нежелательные явления для лекарственных препаратов неприемлемы для вакцин.
В случае же разработки отечественных вакцин имелись явные нарушения. Во-первых, ни один из разработчиков вакцин (КовиВак; Гам-Ковид-Вак; Гам-Ковид-Вак-Лио; ЭпиВакКорона) не предоставил данных по доклиническому исследованию вакцин на животных. Были глобально нарушены сроки разработки и испытания вакцин.
Вместо положенных минумум пяти лет, вакцина для профилактики новой коронавирусной инфекции КовиВак была зарегистрирована в течении 11 месяцев; вакцина Гам-Ковид-Вак; Гам-Ковид-Вак-Лио были разработаны и зарегистрированы в течении 4х месяцев; Вакцина ЭпиВакКорона была зарегистрирована после 7 месяцев исследований.
|
|
|
Если внимательно изучить данные в ходе I/II фазы клинических испытаний Спутника V с участием 76 вакцинированных волонтеров, то мы видим 206 нежелательных явлений [69].
Согласно народным отчетам в чате Telegram, созданном Институтом им. Гамалеи, около 70% людей, которые приняли участие в массовой вакцинации вакциной Спутник V, объявленной с 18 января 2021 г., испытывали гриппоподобные проявления, боль в суставах и теле, а около 80% отмечали повышение температуры уже после первой дозы препарата. Также были отмечены случаи спутанности сознания, эйфории, неврологические и сердечно-сосудистые расстройства, аллергические реакции, нейтропения и многое другое. Были даже по заявлению родственников погибших смертельные случаи, которые, однако, не были зафиксированы как поствакцинальные осложнения.
Кроме того, согласно официальной инструкции Минздрава, препарат Спутник V имеет ряд ограничений, среди которых тяжелые аллергические реакции в анамнезе, хронические заболевания, беременность и период лактации. Однако согласно все тем же народным отчетам, порядка 30% участников страдали хроническими заболеваниями, среди которых были аллергии, псориаз, астма, отеки Квинке в анамнезе, диабет, сердечно-сосудистые заболевания, ожирение и т.д. Более 60% вакцинированных были вынуждены прибегнуть к применению фармакологических средств для облегчения поствакцинальных нежелательных явлений.
Таким образом, мы видим, что те этапы, которые были необходимы для регистрации вакцины — доклинические испытания, I , II и III этап с достаточным количеством добровольцев — были нарушены. Сроки испытаний сокращены, этапы объединены в одно, количество добровольцев сокращено почти в 4 раза – ЧТО НЕДОПУСТИМО, НЕНАУЧНО и НЕБЕЗОПАСНО для жизни и здоровья тех, кто будет применять данные препараты.
То есть по заявлению разработчиков, защитный титр антител неизвестен. Как долго длится защита от заражения – не установлено. Таким образом, нет никакой целесообразности и необходимости проведения такой иммунопрофилактической программы. Все сроки производства вакцины были нарушены и сокращены. Не было доклинических испытаний на животных для уточнения антителозависимого усиления инфекции. ДНК-вакцины и РНК вакцины несут прямую угрозу бесконтрольного редактирования (изменения) генома человека, а чтобы собрать достоверную статистику и тщательно изучить все собранные данные по поствакцинальным осложнениям и изменениям генома человека, нужно от 15 до 25 лет и статистически достоверное количество участников исследования.
А по многолетнему опыту медицинского сообщества – в период эпидемий категорически запрещено проводить вакцинацию от возбудителя заболевания, распространяющегося в данную эпидемию. [70]
ОТВЕТ СПЕЦИАЛИСТОВ НА ВОПРОС №2: Вакцины для профилактики коронавирусной инфекции, вызываемой вирусом SARS-CoV-2, в том числе «Гам-Ковид-Вак» (торговая марка "Спутник V"), «Гам-КОВИД-Вак-Лио», «ЭпиВакКорона», «Ковивак», не являются качественными, эффективными и безопасными для человека. При разработке вакцин ПРОЙДЕНЫ ДАЛЕКО НЕ ВСЕ требуемые научными нормами виды и этапы испытаний, а в пройденных этапах имеются явные нарушения.
Вопрос №3. Формируют ли у человека активный или пассивный иммунитет вакцины для профилактики коронавирусной инфекции, вызываемой вирусом SARS-CoV-2, в том числе «Гам-Ковид-Вак» (торговая марка «Спутник V»), «Гам-КОВИД-Вак-Лио»,«ЭпиВакКорона», «Ковивак»? Если формируют – то на какой период времени?
В ответе на первый вопрос мы рассматривали инструкции к препаратам «Гам-Ковид-Вак» (торговая марка "Спутник V"), «Гам-КОВИД-Вак-Лио»,«ЭпиВакКорона», «Ковивак», где было подробно разобрано, что выработка антител после применения данных препаратов неизвестна и разработчиками не изучалась. Соответственно, если нет защитного титра антител, то и не формируется ни активный, ни пассивный иммунитет. В Российской Федерации активно используются препараты «Гам-Ковид-Вак» (торговая марка "Спутник V"), «Гам-КОВИД-Вак-Лио». Нами были изучены публикации разработчиков данных препаратов, и мы нашли многочисленные ошибки, а также подтверждения, что данные препараты абсолютно неэффективны.
До сих пор не опубликованы результаты доклинических исследований, которые являются ключевыми в вопросах эффективности и безопасности, и это не удивительно, ведь за такой короткий срок этого этапа попросту не было. Прямое обращение Независимой Ассоциации Врачей России к Институту им. Гамалеи по данному вопросу было оставлено без ответа. (Приложение №1- письмо в институт Гамалеи регистрационный номер 131; Приложение №2 — ответ из института Гамалеи).
I и II фазы клинических испытаний институтом Гамалеи вакцин «Гам-Ковид-Вак» (торговая марка "Спутник V"), «Гам-КОВИД-Вак-Лио») объединены в одну. В ходе III фазы клинических испытаний вакцин «Гам-Ковид-Вак» (торговая марка "Спутник V"), «Гам-КОВИД-Вак-Лио» приняли участие 20 тыс. испытуемых вместо анонсируемых 40 тыс [71].
Sheena Cruickshank, иммунолог из Манчестерского университета Великобритании, считает, что результаты открытого нерандомизированного исследования объединенной I и II фазы клинических испытаний "Спутник V" могут привести к переоценке эффективности этого препарата, поскольку в таком случае ассоциация между медицинским вмешательством и полученным результатом может зависеть от стороннего фактора, например, влияния врача [72].
В протоколе открытого исследования безопасности, переносимости и иммуногенности вакцины GamCOVID-Vac Lyo против COVID-19 («Спутник V») указано, что она исследовалась с участием 38 добровольцев, из них 9 человек получили компонент I, 9 человек получили компонент II, 20 человек получили бустерную дозу, т.е. оба компонента с промежутком в 3 недели. В исследовании зарегистрировано, что у всех испытуемых в ответ на введение препарата выработались антитела, причем какая-то часть из них оказалась, по заявлению авторов, именно вируснейтрализующими, а также выработались специфические компоненты клеточного иммунитета – Т лимфоциты – CD4+ и CD8+. Наличие антител было установлено методом иммуноферментного анализа (ELISA). Однако этот метод не позволяет различить между собой нейтрализующие и только связывающие антитела.
Что касается выработки Т лимфоцитов CD4+ и CD8+, как было показано в случае с RSV -вирусом, клеточная память этих компонентов способна индуцировать иммунопатологии при последующем заражении после проведения вакцинации. Одним из основных механизмов контроля вирусной инфекции является клеточная цитотоксичность, которая может действовать антителозависимым или независимым образом и обеспечивается различными эффекторными клетками. Роль CD8 T-клеток в контроле инфекции и влиянии на патологический исход различных типов инфекции была продемонстрирована в многочисленных исследованиях на животных. Ответ Т-клеток CD8 является важной связью между врожденным иммунитетом и иммунным ответом, опосредованным антителами. Кроме того, эти клетки играют значительную роль в развитии аутоиммунных заболеваний. Проще говоря, в норме работа этих клеток должна сводиться к балансу между защитными и саморазрушающими эффектами. Этот баланс может быть нарушен в результате вакцинации [73; 74].
В ходе клинических испытаний не было проведено исследований по заражению иммунизированных пациентов, а доклинические исследования — вовсе отсутствуют. Таким образом, не была протестирована должным образом эффективность препарата GamCOVID-Vac; GamCOVID-Vac- Lyo , и не были выполнены эксперименты, исключающие опасность возникновения иммунопатологий.
Согласно данным III фазы клинических испытаний, естественная заболеваемость в группе плацебо составила 1,3% [75], что само по себе ставит под сомнение целесообразность проведения такой иммунопрофилактической программы. И хотя, согласно авторам, в иммунизированной группе заболеваемость была снижена до 0,1%, естественное заражение вакцинированных людей все же происходит. При этом в группе вакцинированных было 3 смертельных случая, хотя исследователи не связывают их с проведенной иммунопрофилактикой (объяснения не предоставлены).
Согласно официальным данным стопкоронавирус.рф [76] по состоянию на 24 апреля 2021 в России выявлено 4 753 789 случаев заражения, из них в настоящее время выздоровело 4 380 468 человек и 107 900 человек умерло. Отсюда летальность составляет 2,26% от переболевших (итого около 3 смертей на 10 000 человек), смертность составляет менее 0,03, а процент уже выздоровевших (без учета тех, кто болен в данный момент) составляет более 92%.
Таким образом, ни о какой иммунопрофилактике не может быть и речи, так как 92% от заболевших самостоятельно выздоравливают. Само инициирование создания вакцины для профилактики коронавирусной инфекции, вызываемой вирусом SARS-CoV-2, не соответствует целесообразности и необходимости по всем медицинским нормам.А сам препарат не может быть назван вакциной, так как не формирует абсолютно никакого иммунного ответа.
ОТВЕТ СПЕЦИАЛИСТОВ НА ВОПРОС №3: Вакцины для профилактики коронавирусной инфекции, вызываемой вирусом SARS-CoV-2, в том числе «Гам-Ковид-Вак» (торговая марка «Спутник V»), «Гам-КОВИД-Вак-Лио», «ЭпиВакКорона», «Ковивак», не формируют у человека активный и пассивный иммунитет к такой инфекционной болезни, как коронавирусная инфекция, вызываемая вирусом SARS-CoV-2.
Вопрос №4. Ликвидируют ли такую инфекционную болезнь как коронавирусная инфекция, вызываемая вирусом SARS-CoV-2, профилактические прививки вакцинами для профилактики коронавирусной инфекции, вызываемой вирусом SARS-CoV-2, в том числе вакцинами «Гам-Ковид-Вак» (торговая марка «Спутник V»), «Гам-КОВИД-Вак-Лио»,«ЭпиВакКорона», «Ковивак»?
Для ответа на вопрос необходимо проанализировать эффективность иммунопрофилактических препаратов для профилактики новой коронавирусной инфекции согласно уровням заболеваемости в различных странах, приступившим к массовой вакцинации. Многие страны уже запустили массовую вакцинацию, и мы имеем статистические данные, которые ответят на все вопросы.
Согласно официальной статистике в таблице приведен сравнительный анализ эпидемиологической ситуации по некоторым (случайно выбранным) странам в зависимости от проведения иммунопрофилактики против SARS-CoV-2 и гриппа. Грипп так же, как и SARS-CoV-2 , является вирусом группы ОРВИ, и на графиках, и по данным таблицы хорошо видно, что после вакцинации от вирусов группы ОРВИ — заболеваемость увеличивается. Учитывая, что грипп вида А и новая коронавирусная инфекция имеют сходную клиническую картину и являются респираторными вирусами, мы видим по данным таблицы, что вакцинация от вирусов группы ОРВИ провоцирует рост заболеваемости. И в случаях с гриппом, и в случаях с вирусом SARS-CoV-2. Соответственно в России и Белоруссии — с большой долей вероятности может ожидаться рост заболеваемости, связанный с проведенной вакцинацией. Что наглядно видно на примере других стран и в случае с вирусом гриппа
| Страна | Россия |
| Периоды повышенной заболеваемости (волны) гриппа | 1) 30 марта - 26 августа 2020; 2) 25 сентября 2020 - 12 апреля 2021 |
| Начала вакцинации против гриппа | 1 сентября 2020 |
| Условия вакцинации против гриппа | Между пиками |
| Результат | Заболеваемость увеличилась почти в 3 раза по сравнению с первой волной |
| Начало вакцинации против SARS-CoV-2 | 10 декабря 2020 - начало, 18 января 2021- массовая вакцинация |
| Условия вакцинации против SARS-CoV-2 | на пике заболеваемости |
| Используемый препарат | Спутник V |
| Результат | Ожидается |
| Страна | Белоруссия |
| Периоды повышенной заболеваемости (волны) | 1) март - август 2020; 2) август – по н.в. |
| Начала вакцинации против гриппа | 15 сентября 2020 |
| Условия вакцинации против гриппа | Между пиками |
| Результат | Увеличение заболеваемости гриппом более чем в 2 раза |
| Начало вакцинации против SARS-CoV-2 | 29 декабря 2020 |
| Условия вакцинации против SARS-CoV-2 | на пике заболеваемости |
| Используемый препарат | Спутник V |
| Результат | Ожидается |
| Страна | Израиль |
| Периоды повышенной заболеваемости (волны)гриппа | 1) 30 июня - 25 октября 2020; 2) 27 ноября 2020 - 4 апреля 2021 |
| Начала вакцинации против гриппа | 9 сентября 2020 |
| Условия вакцинации против гриппа | На подъеме |
| Результат | Увеличение заболеваемости |
| Начало вакцинации против SARS-CoV-2 | 20 декабря 2020 |
| Условия вакцинации против SARS-CoV-2 | Начало следующей волны, почти между пиками |
| Используемый препарат | Pfrizer |
| Результат | Заболеваемость SARS-CoV-2 увеличилась примерно на 40% по сравнению с первой волной |
| Страна | Южная Корея |
| Периоды повышенной заболеваемости (волны) гриппа | 1) февраль - апрель 2020; 2) август - октябрь 2020; 3) октябрь 2020 – по н.в. |
| Начала вакцинации против гриппа | осень (октябрь) 2020 |
| Условия вакцинации против гриппа | Между пиками |
| Результат | значительное увеличение заболеваемости гриппом , в 3 и более раз |
| Начало вакцинации против SARS-CoV-2 | 15 февраля 2021 |
| Условия вакцинации против SARS-CoV-2 | на фоне заболеваемости |
| Используемый препарат | AstraZeneca, Pfizer |
| Результат | заметное увеличение заболеваемости SARS-CoV-2 |
| Страна | Германия |
| Периоды повышенной заболеваемости (волны) гриппа | 1) март- май 2020; 2) сентябрь 2020- по н.в. |
| Начала вакцинации против гриппа | осень (октябрь) 2020 |
| Условия вакцинации против гриппа | Между пиками |
| Результат | Увеличение заболеваемости |
| Начало вакцинации против SARS-CoV-2 | 27 декабря 2020 |
| Условия вакцинации против SARS-CoV-2 | на пике заболеваемости |
| Используемый препарат | Pfizer |
| Результат | Спад и новый подъем заболеваемости SARS-CoV-2 |
| Страна | Швеция |
| Периоды повышенной заболеваемости (волны) гриппа | 1) 20 октября 2020 – по н.в. |
| Начала вакцинации против гриппа | 9 сентября 2020 |
| Условия вакцинации против гриппа | Отсутствие заболеваемости |
| Результат | Увеличение заболеваемости, которая началась только после введения ограничительных мер |
| Начало вакцинации против SARS-CoV-2 | - |
| Условия вакцинации против SARS-CoV-2 | - |
| Используемый препарат | - |
| Результат | - |
| Страна | Гвинея |
| Периоды повышенной заболеваемости (волны) гриппа | 1) апрель - декабрь 2020; 2) февраль - апрель 2021 |
| Начала вакцинации против гриппа | Нет данных |
| Условия вакцинации против гриппа | Нет данных |
| Результат | Нет данных |
| Начало вакцинации против SARS-CoV-2 | 30 декабря 2020 |
| Условия вакцинации против SARS-CoV-2 | между не явно выраженными пиками |
| Используемый препарат | Спутник V |
| Результат | Увеличение заболеваемости SARS-CoV-2 |
| Страна | Тунис |
| Периоды повышенной заболеваемости (волны) гриппа | 1) август - декабрь 2020; 2) декабрь - март 2021; 3) 24 марта 2021 – по н.в. |
| Начала вакцинации против гриппа | - |
| Условия вакцинации против гриппа | - |
| Результат | - |
| Начало вакцинации против SARS-CoV-2 | 9 марта 2021 |
| Условия вакцинации против SARS-CoV-2 | Между пиками |
| Используемый препарат | Спутник V |
| Результат | Увеличение заболеваемости SARS-CoV-2 |
| Страна | Бразилия |
| Периоды повышенной заболеваемости (волны) гриппа | 1) апрель - ноябрь 2020; 2) ноябрь 2020 – по н.в. |
| Начала вакцинации против гриппа | - |
| Условия вакцинации против гриппа | - |
| Результат | - |
| Начало вакцинации против SARS-CoV-2 | 13 января 2021 |
| Условия вакцинации против SARS-CoV-2 | на подъеме |
| Используемый препарат | Спутник V |
| Результат | Увеличение заболеваемости SARS-CoV-2 |
| Страна | Венгрия |
| Периоды повышенной заболеваемости (волны) гриппа | 1) 6 сентября 2020 - 25 января 2021; 2) 11 февраля 2021 – по н.в. |
| Начала вакцинации против гриппа | - |
| Условия вакцинации против гриппа | - |
| Результат | - |
| Начало вакцинации против SARS-CoV-2 | 11 февраля 2021 |
| Условия вакцинации против SARS-CoV-2 | Между пиками |
| Используемый препарат | Спутник V, AstraZeneca, Sinopharm |
| Результат | заболеваемость SARS-CoV-2 увеличилась примерно на 40% по сравнению с первой волной |
| Страна | Индия |
| Периоды повышенной заболеваемости (волны) гриппа | 1) июнь - декабрь 2020; 2) февраль 2021 – по н.в. |
| Начала вакцинации против гриппа | - |
| Условия вакцинации против гриппа | - |
| Результат | - |
| Начало вакцинации против SARS-CoV-2 | 16 января 2021 |
| Условия вакцинации против SARS-CoV-2 | Между пиками |
| Используемый препарат | Спутник V, AstraZeneca |
| Результат | Резкое увеличение заболеваемости SARS-CoV-2 |
| Страна | Англия |
| Периоды повышенной заболеваемости (волны) гриппа | 1) март - май 2020; 2) сентябрь - декабрь 2020; 3) декабрь 2020 - апрель 2021 |
| Начала вакцинации против гриппа | - |
| Условия вакцинации против гриппа | - |
| Результат | - |
| Начало вакцинации против SARS-CoV-2 | 8 декабря 2020 |
| Условия вакцинации против SARS-CoV-2 | Между пиками на фоне заболеваемости |
| Используемый препарат | Pfizer |
| Результат | Резкое увеличение заболеваемости SARS-CoV-2 |
| Страна | Канада |
| Периоды повышенной заболеваемости (волны) гриппа | 1) Не явно выраженное нарастание заболеваемости; 2) С сентября 2020 - по н.в. |
| Начала вакцинации против гриппа | - |
| Условия вакцинации против гриппа | - |
| Результат | - |
| Начало вакцинации против SARS-CoV-2 | 14 ноября 2020 |
| Условия вакцинации против SARS-CoV-2 | На подъеме |
| Используемый препарат | Pfizer |
| Результат | Увеличение заболеваемости SARS-CoV-2 |
| Страна | Норвегия |
| Периоды повышенной заболеваемости (волны) гриппа | 1) март - май 2020; 2) сентябрь 2020 - |
| Начала вакцинации против гриппа | - |
| Условия вакцинации против гриппа | - |
| Результат | - |
| Начало вакцинации против SARS-CoV-2 | 28 декабря 2020 |
| Условия вакцинации против SARS-CoV-2 | На пике заболеваемости |
| Используемый препарат | Pfizer, AstraZeneca |
| Результат | Преодоление пика и новая волна с усиленной заболеваемостью SARS-CoV-2 |
Ряд стран, включая Россию, начали вакцинацию против новой коронавирусной инфекции на пике заболеваемости, что противоречит медицинским нормам, выработанным с течением времени на основании опыта большого количества специалистов и стран. Совершенно очевидно, что практически каждой последующей волне предшествовал этап массовой вакцинации (либо против гриппа, либо против коронавируса). Опираясь уже на данные постмаркетинговых испытаний, можно сказать, что вакцинация против коронавирусной инфекции, вызываемой вирусом SARS-CoV-2, усугубляет эпидемиологическую ситуацию и никак не способствует её улучшению.
Графическое изображение данных, представленных в таблице выше [77]:
- цифры по вертикали - количество случаев; даты по горизонтали — даты за 2020 - 2021 год

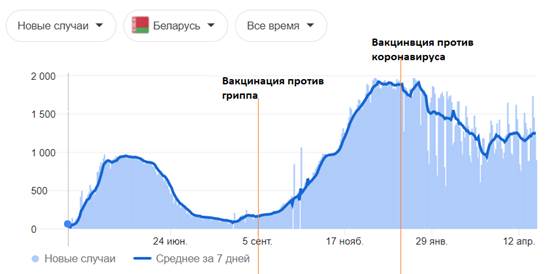
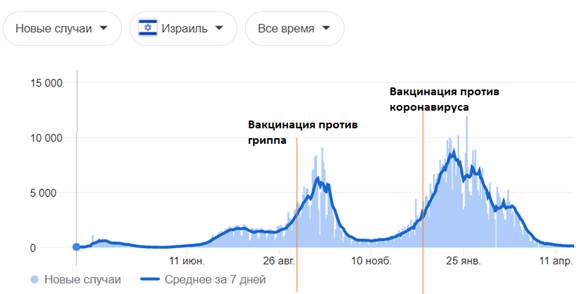
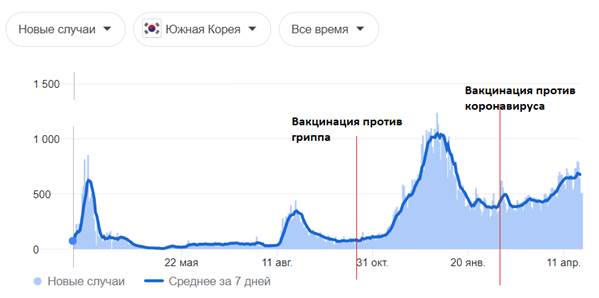
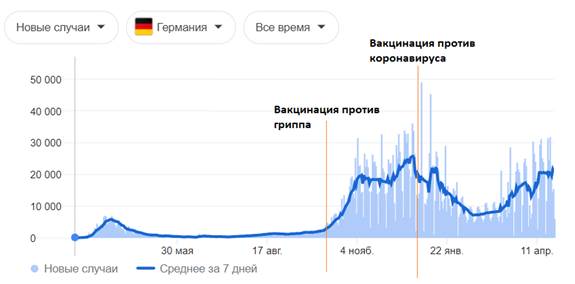
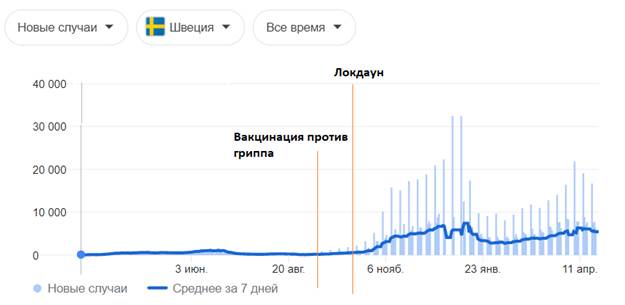
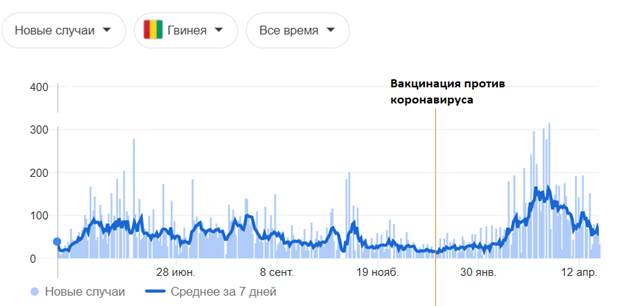

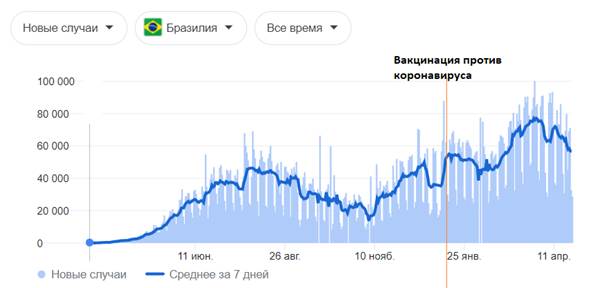
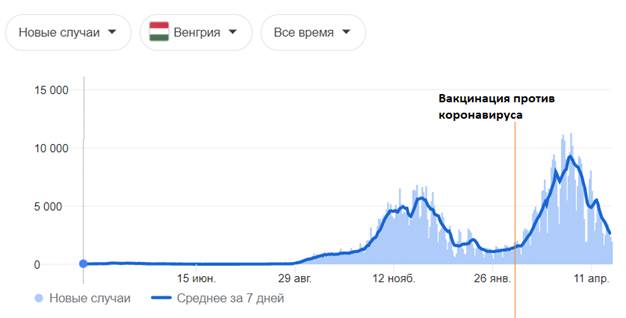
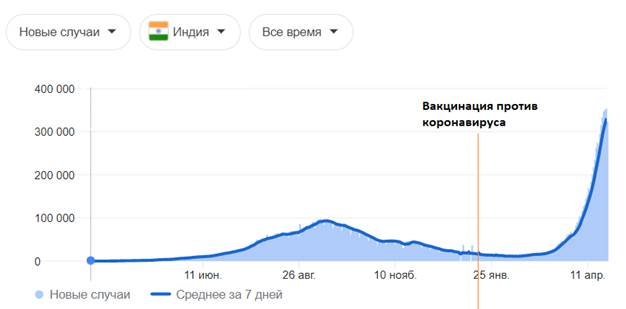
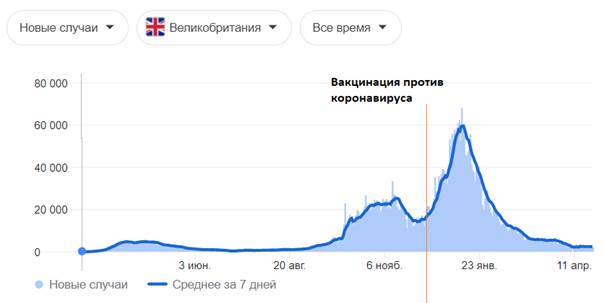
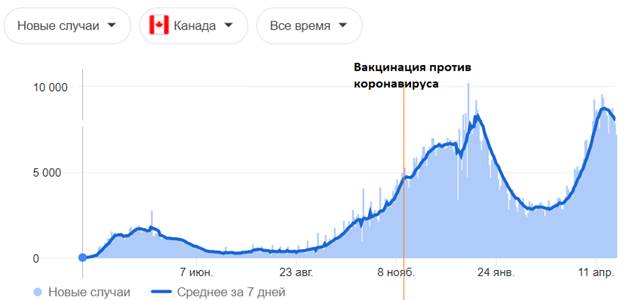
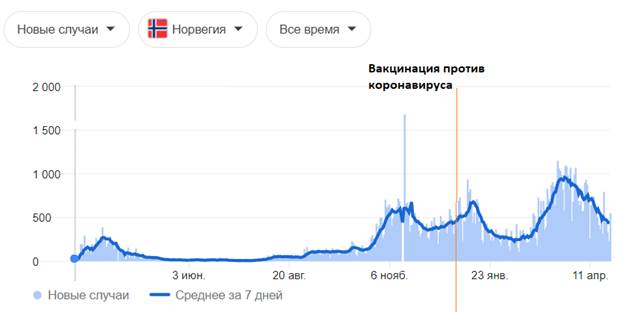
После проведенных исследований разработчиками вакцин не выяснено, создается ли защитный титр антител у испытуемых, о чем прописано в инструкциях к препаратам и в фармакопейных статьях. Если нет защитного титра антител, соответственно не может быть сформировано иммунитета к вирусу SARS-CoV-2и не может быть его ликвидация данными препаратами. На приведенных графиках и таблицах в исследовании замечено, чтопрофилактические прививки против коронавирусной инфекции, направленные на выработку связывающих антител к S-белкам коронавируса, приводят к развитию побочных эффектов и к летальным исходам. Таким образом, профилактические прививки от новой коронавирусной инфекции SARS-CoV-2 вызывают не ликвидацию, а напротив, рост заболеваемости коронавирусной инфекцией.
ОТВЕТ СПЕЦИАЛИСТОВ НА ВОПРОС №4: Профилактические прививки вакцинами для профилактики коронавирусной инфекции, вызываемой вирусом SARS-CoV-2, в том числе вакцинами «Гам-Ковид-Вак» (торговая марка «Спутник V»), «Гам-КОВИД-Вак-Лио», «ЭпиВакКорона», «Ковивак», не ликвидируют такую инфекционную болезнь, как коронавирусная инфекция, вызываемая вирусом SARS-CoV-2.
Вопрос №5: К акое соотношение ожидаемой пользы к возможному риску применения вакцин для профилактики коронавирусной инфекции, вызываемой вирусом SARS-CoV-2, в том числе «Гам-Ковид-Вак» (торговая марка «Спутник V»), «Гам-КОВИД-Вак-Лио»,«ЭпиВакКорона», «Ковивак»?
Статистики осложнений или смертности после вакцинации отечественными препаратами для профилактики коронавирусной инфекции, вызываемой вирусом SARS-CoV-2, официальные источники не приводят.
Однако достоверно известно, что существующие зарубежные препараты разработаны на тех же принципах, что и отечественные. Одинаковый механизм действия препаратов с большой вероятностью будет вызывать и сходные реакции организмов человека, включая осложнения и летальность.
Действительно, действие исследуемых отечественных и зарубежных иммунопрофилактических препаратов для профилактики SARS-CoV-2 направлено на выработку связывающих антител к S-белкам вируса SARS-CoV-2 [шиповидный белок/ S -белок/ Спайк/ «спайковый» белок/ булавообразный белок/ Spike Glycoprotein (S) – белок, который образует «корону» коронавируса и обеспечивает ему вход в клетку, а его участки вызывают наиболее сильный иммунный ответ у переболевших COVID-19 людей]
Следовательно, можно утверждать, что побочные эффекты и летальные исходы после проведения процедуры иммунизации ассоциированы именно с выработкой антител к S-белкам. И от применения любых иммунопрофилактических препаратов против SARS - CoV -2, в том числе «Гам-Ковид-Вак», «Гам-Ковид-Вак-Лио», «ЭпиВакКорона», «Ковивак», будут развиваться подобные последствия.
В таблице ниже приведены сведения о летальных случаях, связанных с применением иммунопрофилактических препаратов, разработанных в других странах (Pfizer; Moderna; AstraZeneса; Janssen). Статистка собрана с официального сайта EudraVigilance - Европейские отчеты о предполагаемых побочных реакциях на лекарства [78].
| Reaction group | Группа реакции от органов и систем организма | Название препарата | Количество смертельных случаев |
| Blood and lymphatic system disorders | Заболевания крови и лимфатической системы | COVID-19 MRNA VACCINE PFIZER-BIONTECH (TOZINAMERAN) | 40 |
| Cardiac disorders | Сердечные расстройства | COVID-19 MRNA VACCINE PFIZER-BIONTECH (TOZINAMERAN) | 522 |
| Congenital, familial and genetic disorders | Врожденные, семейные и генетические нарушения | COVID-19 MRNA VACCINE PFIZER-BIONTECH (TOZINAMERAN) | 3 |
| Ear and labyrinth disorders | Нарушения уха | COVID-19 MRNA VACCINE PFIZER-BIONTECH (TOZINAMERAN) | 3 |
| Endocrine disorders | Эндокринные расстройства | COVID-19 MRNA VACCINE PFIZER-BIONTECH (TOZINAMERAN) | 0 |
| Blood and lymphatic system disorders | Заболевания крови и лимфатической системы | COVID-19 MRNA VACCINE MODERNA (CX-024414) | 16 |
| Cardiac disorders | Сердечные расстройства | COVID-19 MRNA VACCINE MODERNA (CX-024414) | 231 |
| Congenital, familial and genetic disorders | Врожденные, семейные и генетические нарушения | COVID-19 MRNA VACCINE MODERNA (CX-024414) | 2 |
| Ear and labyrinth disorders | Нарушения уха | COVID-19 MRNA VACCINE MODERNA (CX-024414) | 0 |
| Endocrine disorders | Эндокринные расстройства | COVID-19 MRNA VACCINE MODERNA (CX-024414) | 1 |
| Eye disorders | Заболевания глаз | COVID-19 MRNA VACCINE PFIZER-BIONTECH (TOZINAMERAN) | 6 |
| Gastrointestinal disorders | Желудочно-кишечные расстройства | COVID-19 MRNA VACCINE PFIZER-BIONTECH (TOZINAMERAN) | 227 |
| General disorders and administration site conditions | Общие расстройства и состояния в месте введения | COVID-19 MRNA VACCINE PFIZER-BIONTECH (TOZINAMERAN) | 1459 |
| Hepatobiliary disorders | Гепатобилиарные расстройства | COVID-19 MRNA VACCINE PFIZER-BIONTECH (TOZINAMERAN) | 16 |
| Immune system disorders | Со стороны иммунной системы | COVID-19 MRNA VACCINE PFIZER-BIONTECH (TOZINAMERAN) | 20 |
| Infections and infestations | Инфекции и инвазии | COVID-19 MRNA VACCINE PFIZER-BIONTECH (TOZINAMERAN) | 527 |
| Injury, poisoning and procedural complications | Травмы, отравления и процедурные осложнения | COVID-19 MRNA VACCINE PFIZER-BIONTECH (TOZINAMERAN) | 89 |
| Investigations | Расследования | COVID-19 MRNA VACCINE PFIZER-BIONTECH (TOZINAMERAN) | 168 |
| Metabolism and nutrition disorders | Нарушения обмена веществ и питания | COVID-19 MRNA VACCINE PFIZER-BIONTECH (TOZINAMERAN) | 91 |
| Musculoskeletal and connective tissue disorders | Опорно-двигательный аппарат и соединительная ткань | COVID-19 MRNA VACCINE PFIZER-BIONTECH (TOZINAMERAN) | 47 |
| Neoplasms benign, malignant and unspecified (incl cysts and polyps) | Доброкачественные, злокачественные и неуточненные новообразования (включая кисты и полипы) | COVID-19 MRNA VACCINE PFIZER-BIONTECH (TOZINAMERAN) | 7 |
| Nervous system disorders | Расстройства нервной системы | COVID-19 MRNA VACCINE PFIZER-BIONTECH (TOZINAMERAN) | 425 |
| Pregnancy, puerperium and perinatal conditions | Беременность, послеродовой период и перинатальные состояния | COVID-19 MRNA VACCINE PFIZER-BIONTECH (TOZINAMERAN) | 7 |
| Product issues | Проблемы с продуктом | COVID-19 MRNA VACCINE PFIZER-BIONTECH (TOZINAMERAN) | 0 |
| Psychiatric disorders | Психиатрические расстройства | COVID-19 MRNA VACCINE PFIZER-BIONTECH (TOZINAMERAN) | 63 |
| Renal and urinary disorders | Со стороны почек и мочевыводящих путей | COVID-19 MRNA VACCINE PFIZER-BIONTECH (TOZINAMERAN) | 66 |
| Reproductive system and breast disorders | Репродуктивная система и заболевания груди | COVID-19 MRNA VACCINE PFIZER-BIONTECH (TOZINAMERAN) | 1 |
| Respiratory, thoracic and mediastinal disorders | Респираторные, торакальные и средостенные расстройства. | COVID-19 MRNA VACCINE PFIZER-BIONTECH (TOZINAMERAN) | 523 |
| Skin and subcutaneous tissue disorders | Заболевания кожи и подкожной клетчатки | COVID-19 MRNA VACCINE PFIZER-BIONTECH (TOZINAMERAN) | 35 |
| Social circumstances | Социальные обстоятельства | COVID-19 MRNA VACCINE PFIZER-BIONTECH (TOZINAMERAN) | 6 |
| Surgical and medical procedures | Хирургические и лечебные процедуры | COVID-19 MRNA VACCINE PFIZER-BIONTECH (TOZINAMERAN) | 8 |
| Vascular disorders | Сосудистые расстройства | COVID-19 MRNA VACCINE PFIZER-BIONTECH (TOZINAMERAN) | 165 |
| Eye disorders | Заболевания глаз | COVID-19 MRNA VACCINE MODERNA (CX-024414) | 3 |
| Gastrointestinal disorders | Желудочно-кишечные расстройства | COVID-19 MRNA VACCINE MODERNA (CX-024414) | 80 |
| General disorders and administration site conditions | Общие расстройства и состояния в месте введения | COVID-19 MRNA VACCINE MODERNA (CX-024414) | 1012 |
| Hepatobiliary disorders | Гепатобилиарные расстройства | COVID-19 MRNA VACCINE MODERNA (CX-024414) | 3 |
| Immune system disorders | Со стороны иммунной системы | COVID-19 MRNA VACCINE MODERNA (CX-024414) | 3 |
| Infections and infestations | Инфекции и инвазии | COVID-19 MRNA VACCINE MODERNA (CX-024414) | 118 |
| Injury, poisoning and procedural complications | Травмы, отравления и процедурные осложнения | COVID-19 MRNA VACCINE MODERNA (CX-024414) | 44 |
| Investigations | Расследования | COVID-19 MRNA VACCINE MODERNA (CX-024414) | 60 |
| Metabolism and nutrition disorders | Нарушения обмена веществ и питания | COVID-19 MRNA VACCINE MODERNA (CX-024414) | 47 |
| Musculoskeletal and connective tissue disorders | Опорно-двигательный аппарат и соединительная ткань | COVID-19 MRNA VACCINE MODERNA (CX-024414) | 47 |
| Neoplasms benign, malignant and unspecified (incl cysts and polyps) | Доброкачественные, злокачественные и неуточненные новообразования (включая кисты и полипы) | COVID-19 MRNA VACCINE MODERNA (CX-024414) | 8 |
| Nervous system disorders | Расстройства нервной системы | COVID-19 MRNA VACCINE MODERNA (CX-024414) | 244 |
| Pregnancy, puerperium and perinatal conditions | Беременность, послеродовой период и перинатальные состояния | COVID-19 MRNA VACCINE MODERNA (CX-024414) | 0 |
| Product issues | Проблемы с продуктом | COVID-19 MRNA VACCINE MODERNA (CX-024414) | 0 |
| Psychiatric disorders | Психиатрические расстройства | COVID-19 MRNA VACCINE MODERNA (CX-024414) | 31 |
| Renal and urinary disorders | Со стороны почек и мочевыводящих путей | COVID-19 MRNA VACCINE MODERNA (CX-024414) | 23 |
| Reproductive system and breast disorders | Репродуктивная система и заболевания груди | COVID-19 MRNA VACCINE MODERNA (CX-024414) | 1 |
| Respiratory, thoracic and mediastinal disorders | Респираторные, торакальные и средостенные расстройства. | COVID-19 MRNA VACCINE MODERNA (CX-024414) | 197 |
| Skin and subcutaneous tissue disorders | Заболевания кожи и подкожной клетчатки | COVID-19 MRNA VACCINE MODERNA (CX-024414) | 19 |
| Social circumstances | Социальные обстоятельства | COVID-19 MRNA VACCINE MODERNA (CX-024414) | 6 |
| Surgical and medical procedures | Хирургические и лечебные процедуры | COVID-19 MRNA VACCINE MODERNA (CX-024414) | 13 |
| Vascular disorders | Сосудистые расстройства | COVID-19 MRNA VACCINE MODERNA (CX-024414) | 74 |
| Blood and lymphatic system disorders | Заболевания крови и лимфатической системы | COVID-19 VACCINE ASTRAZENECA (CHADOX1 NCOV-19) | 64 |
| Cardiac disorders | Сердечные расстройства | COVID-19 VACCINE ASTRAZENECA (CHADOX1 NCOV-19) | 199 |
| Congenital, familial and genetic disorders | Врожденные, семейные и генетические нарушения | COVID-19 VACCINE ASTRAZENECA (CHADOX1 NCOV-19) | 2 |
| Ear and labyrinth disorders | Нарушения уха | COVID-19 VACCINE ASTRAZENECA (CHADOX1 NCOV-19) | 0 |
| Endocrine disorders | Эндокринные расстройства | COVID-19 VACCINE ASTRAZENECA (CHADOX1 NCOV-19) | 2 |
| Eye disorders | Заболевания глаз | COVID-19 VACCINE ASTRAZENECA (CHADOX1 NCOV-19) | 5 |
| Gastrointestinal disorders | Желудочно-кишечные расстройства | COVID-19 VACCINE ASTRAZENECA (CHADOX1 NCOV-19) | 62 |
| General disorders and administration site conditions | Общие расстройства и состояния в месте введения | COVID-19 VACCINE ASTRAZENECA (CHADOX1 NCOV-19) | 495 |
| Hepatobiliary disorders | Гепатобилиарные расстройства | COVID-19 VACCINE ASTRAZENECA (CHADOX1 NCOV-19) | 13 |
| Immune system disorders | Со стороны иммунной системы | COVID-19 VACCINE ASTRAZENECA (CHADOX1 NCOV-19) | 7 |
| Infections and infestations | Инфекции и инвазии | COVID-19 VACCINE ASTRAZENECA (CHADOX1 NCOV-19) | 99 |
| Injury, poisoning and procedural complications | Травмы, отравления и процедурные осложнения | COVID-19 VACCINE ASTRAZENECA (CHADOX1 NCOV-19) | 18 |
| Investigations | Расследования | COVID-19 VACCINE ASTRAZENECA (CHADOX1 NCOV-19) | 21 |
| Metabolism and nutrition disorders | Нарушения обмена веществ и питания | COVID-19 VACCINE ASTRAZENECA (CHADOX1 NCOV-19) | 18 |
| Musculoskeletal and connective tissue disorders | Опорно-двигательный аппарат и соединительная ткань | COVID-19 VACCINE ASTRAZENECA (CHADOX1 NCOV-19) | 16 |
| Neoplasms benign, malignant and unspecified (incl cysts and polyps) | Доброкачественные, злокачественные и неуточненные новообразования (включая кисты и полипы) | COVID-19 VACCINE ASTRAZENECA (CHADOX1 NCOV-19) | 4 |
| Nervous system disorders | Расстройства нервной системы | COVID-19 VACCINE ASTRAZENECA (CHADOX1 NCOV-19) | 244 |
| Pregnancy, puerperium and perinatal conditions | Беременность, послеродовой период и перинатальные состояния | COVID-19 VACCINE ASTRAZENECA (CHADOX1 NCOV-19) | 0 |
| Product issues | Проблемы с продуктом | COVID-19 VACCINE ASTRAZENECA (CHADOX1 NCOV-19) | 0 |
| Psychiatric disorders | Психиатрические расстройства | COVID-19 VACCINE ASTRAZENECA (CHADOX1 NCOV-19) | 12 |
| Renal and urinary disorders | Со стороны почек и мочевыводящих путей | COVID-19 VACCINE ASTRAZENECA (CHADOX1 NCOV-19) | 11 |
| Reproductive system and breast disorders | Репродуктивная система и заболевания груди | COVID-19 VACCINE ASTRAZENECA (CHADOX1 NCOV-19) | 0 |
| Respiratory, thoracic and mediastinal disorders | Респираторные, торакальные и средостенные расстройства. | COVID-19 VACCINE ASTRAZENECA (CHADOX1 NCOV-19) | 171 |
| Skin and subcutaneous tissue disorders | Заболевания кожи и подкожной клетчатки | COVID-19 VACCINE ASTRAZENECA (CHADOX1 NCOV-19) | 10 |
| Social circumstances | Социальные обстоятельства | COVID-19 VACCINE ASTRAZENECA (CHADOX1 NCOV-19) | 3 |
| Surgical and medical procedures | Хирургические и лечебные процедуры | COVID-19 VACCINE ASTRAZENECA (CHADOX1 NCOV-19) | 12 |
| Vascular disorders | Сосудистые расстройства | COVID-19 VACCINE ASTRAZENECA (CHADOX1 NCOV-19) | 91 |
| Blood and lymphatic system disorders | Заболевания крови и лимфатической системы | COVID-19 VACCINE JANSSEN (AD26.COV2.S) | 0 |
| Cardiac disorders | Сердечные расстройства | COVID-19 VACCINE JANSSEN (AD26.COV2.S) | 10 |
| Congenital, familial and genetic disorders | Врожденные, семейные и генетические нарушения | COVID-19 VACCINE JANSSEN (AD26.COV2.S) | 0 |
| Ear and labyrinth disorders | Нарушения уха | COVID-19 VACCINE JANSSEN (AD26.COV2.S) | 0 |
| Endocrine disorders | Эндокринные расстройства | COVID-19 VACCINE JANSSEN (AD26.COV2.S) | 0 |
| Eye disorders | Заболевания глаз | COVID-19 VACCINE JANSSEN (AD26.COV2.S) | 0 |
| Gastrointestinal disorders | Желудочно-кишечные расстройства | COVID-19 VACCINE JANSSEN (AD26.COV2.S) | 0 |
| General disorders and administration site conditions | Общие расстройства и состояния в месте введения | COVID-19 VACCINE JANSSEN (AD26.COV2.S) | 14 |
| Hepatobiliary disorders | Гепатобилиарные расстройства | COVID-19 VACCINE JANSSEN (AD26.COV2.S) | 0 |
| Immune system disorders | Со стороны иммунной системы | COVID-19 VACCINE JANSSEN (AD26.COV2.S) | 0 |
| Infections and infestations | Инфекции и инвазии | COVID-19 VACCINE JANSSEN (AD26.COV2.S) | 0 |
| Injury, poisoning and procedural complications | Травмы, отравления и процедурные осложнения | COVID-19 VACCINE JANSSEN (AD26.COV2.S) | 0 |
| Investigations | Расследования | COVID-19 VACCINE JANSSEN (AD26.COV2.S) | 0 |
| Metabolism and nutrition disorders | Нарушения обмена веществ и питания | COVID-19 VACCINE JANSSEN (AD26.COV2.S) | 0 |
| Musculoskeletal and connective tissue disorders | Опорно-двигательный аппарат и соединительная ткань | COVID-19 VACCINE JANSSEN (AD26.COV2.S) | 0 |
| Neoplasms benign, malignant and unspecified (incl cysts and polyps) | Доброкачественные, злокачественные и неуточненные новообразования (включая кисты и полипы) | COVID-19 VACCINE JANSSEN (AD26.COV2.S) | 1 |
| Nervous system disorders | Расстройства нервной системы | COVID-19 VACCINE JANSSEN (AD26.COV2.S) | 0 |
| Pregnancy, puerperium and perinatal conditions | Беременность, послеродовой период и перинатальные состояния | COVID-19 VACCINE JANSSEN (AD26.COV2.S) | 0 |
| Product issues | Проблемы с продуктом | COVID-19 VACCINE JANSSEN (AD26.COV2.S) | 1 |
| Psychiatric disorders | Психиатрические расстройства | COVID-19 VACCINE JANSSEN (AD26.COV2.S) | 0 |
| Renal and urinary disorders | Со стороны почек и мочевыводящих путей | COVID-19 VACCINE JANSSEN (AD26.COV2.S) | 1 |
| Reproductive system and breast disorders | Репродуктивная система и заболевания груди | COVID-19 VACCINE JANSSEN (AD26.COV2.S) | 0 |
| Respiratory, thoracic and mediastinal disorders | Респираторные, торакальные и средостенные расстройства. | COVID-19 VACCINE JANSSEN (AD26.COV2.S) | 3 |
| Skin and subcutaneous tissue disorders | Заболевания кожи и подкожной клетчатки | COVID-19 VACCINE JANSSEN (AD26.COV2.S) | 0 |
| Social circumstances | Социальные обстоятельства | COVID-19 VACCINE JANSSEN (AD26.COV2.S) | 0 |
| Surgical and medical procedures | Хирургические и лечебные процедуры | COVID-19 VACCINE JANSSEN (AD26.COV2.S) | 0 |
| Vascular disorders | Сосудистые расстройства | COVID-19 VACCINE JANSSEN (AD26.COV2.S) | 8 |
| Blood and lymphatic system disorders | Заболевания крови и лимфатической системы | COVID-19 MRNA VACCINE PFIZER-BIONTECH (TOZINAMERAN) | 40 |
Дата добавления: 2021-07-19; просмотров: 35; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!
