ЗАДАНИЯ НА КОНТРОЛЬНУЮ РАБОТУ
МИНИСТЕРСТВО ОБРАЗОВАНИЯ И НАУКИ УКРАИНЫ
ВОСТОЧНОУКРАИНСКИЙ НАЦИОНАЛЬНЫЙ УНИВЕРСИТЕТ
ИМ. ВЛАДИМИРА ДАЛЯ
Методические указания
к контрольным работам по дисциплине
“КОРРОЗИЯ И ЗАЩИТА МЕТАЛЛОВ И КОНСТРУКЦИЙ ОТ КОРРОИИ”
(для студентов заочного отделения, обучающихся по направлению
“Инженерное материаловедение”)
У т в е р ж д е н о
на заседании кафедры «Прикладного материаловедения».
Протокол №__от 02. 2003 года.
Луганск ВНУ 2003_
УДК 620.197.
Методические указания и контрольные задания по курсу “Защита металлов и конструкций от коррозии” (для студентов, обучающихся по направлению “Инженерное материаловедение”) /Сост.: Рябичева Л.А., Карташова Л.И., Колодяжная Л.Г.. - Луганск: Изд-во Восточноукр. нац. ун-та, им В. Даля 2003.-27 с.
Приведены методические указания и контрольные задания практического значения, необходимые для выполнения самостоятельной работы по дисциплине “Защита металлов и конструкций от коррозии”. Предложены качественные и количественные задачи по оценке коррозионных разрушений, даны методические рекомендации по решению различных типов задач
Составители: Л. А. Рябичева, проф.
Л. И. Карташова, доц.
Л.Г. Колодяжная, ассист.
Отв. за выпуск Л.А. Рябичева, проф.
Рецензент А.Т. Цыркин, доц.
ВВЕДЕНИЕ
Самостоятельная работа по дисциплине «Защита металлов и конструкций от коррозии» позволяет систематизировать и обобщить знания после ее изучения.
Цель выполнения самостоятельной работы: усвоить знания по газовой и электрохимической коррозии, методам защиты металлов и конструкций от коррозии, которые будут использованы студентами в практической и профессиональной деятельности.
Задачи дисциплины:
- раскрыть физико-химическую сущность коррозионных процессов;
- научить студентов правильно оценивать коррозионную стойкость материалов;
- правильно выбирать материалы для различных деталей и конструкций;
- использовать различные виды защиты металлов и конструкций от коррозии.
В результате изучения дисциплины студент должен:
знать сущность коррозии, взаимосвязь внутренних и внешних факторов влияющих на механизм и кинетику химической и электрохимической коррозии, классификацию коррозионных разрушений, методы защиты материалов от коррозионных разрушений;
уметь анализировать причины, вызвавшие коррозию, правильно выбирать материал для конструкций, работающих в агрессивных средах, количественно оценивать коррозионные разрушения, выбирать эффективные и экономически рациональные меры защиты от коррозии, работать и анализировать справочную и методическую литературу.
иметь представление о современных перспективах развития коррозионных исследований.
СОДЕРЖАНИЕ ДИСЦИПЛИНЫ
1. Лекционные занятия
2. Цель проведения лекций – ознакомить студентов с видами коррозионных разрушений, с механизмами газовой и электрохимической коррозии, с внешними и внутренними факторами, влияющими на коррозию, с видами защиты. Изучить коррозионно-стойкие материалы и возможности их применения
Содержание лекционных занятий
Химическая коррозия металлов.
Внутренние факторы химической коррозии: влияние химического состава, влияние внутренних напряжений и качества обработки поверхности металлических изделий.
Внешние факторы химической коррозии: влияние температуры нагрева и времени выдержки, влияние химического состава газовой среды, давления и скорости движения газов.
Выбор жаропрочных материалов для работы в коррозионных средах.
Электрохимическая коррозия металлов.
Поляризация электродных процессов. Электрохимическая кинетика анодных и катодных процессов.
Коррозионные процессы с кислородной деполяризацией. Схема процесса и виды поляризации. Защита металлов от коррозии в нейтральных электролитах.
Коррозионные процессы с водородной деполяризацией. Схема процесса и виды поляризации. Защита металлов от коррозии в растворах кислот.
Коррозионно-стойкие металлические материалы.
Хромоникелевые и хромомарганцево-никелевые аустенитные и аустенитно- ферритные стали. Область применения. Влияние содержания хрома и никеля, углерода, карбидных фаз на коррозионную стойкость и склонность к межкристаллитной коррозии. Особенности структуры и свойств. Способность к пассивации в кислотах. Применение.
Высокопрочные нержавеющие стали с неустойчивым аустенитом. Область применения, структура и свойства.
Высоколегированные коррозионно-стойкие стали. Область применения, структура и свойства.
Электрохимическая защита.
Теоретические основы протекторной и катодной защиты. Критерии защиты. Комплексная защита. Покрытия, применяемые в случае катодной защиты. Протекторная защита. Материалы протекторов. Катодная защита.
Анодная защита. Параметры защиты. Ингибиторная защита. Ингибиторы коррозии. Неорганические и органические ингибиторы. Примеры использования ингибиторной защиты.
ТЕМАТИКА ЛАБОРАТОРНЫХ РАБОТ
Цель проведения лабораторных занятий: изучить основные причины коррозии материалов, научить использовать конструкционные материалы, покрытия для защиты в коррозионных средах.
| № | Названия лабораторных работ | Число часов |
| 1 | Влияние внутренних и внешних факторов на Электрохимическую коррозию стали. | 2 |
| 2 | Изучение влияния ингибиторов на скорость коррозии. | 2 |
| 3 | Исследование качества антикоррозионных покрытий. | 2 |
| 4 | Исследование свойств антикоррозионных материалов. | 2 |
ЗАДАНИЯ НА КОНТРОЛЬНУЮ РАБОТУ
Выполнение самостоятельной работы в общей системе работ обусловлено необходимостью закрепления материала по дисциплине студентами и совершенствования навыков работы с литературой.
Контрольные задания составлены с учетом современных требований подготовки будущего специалиста, с ориентацией его на производственную деятельность.
Подбор заданий и задач осуществлялся таким образом, чтобы охватить все темы программы. В содержание заданий самостоятельной работы положен принцип развития творческого мышления студента. Задания носят практическую и профессиональную направленность, включают как репродуктивный /1-3/ вопросы, так и продуктивный уровни сложности /4-5/ вопросы.
При оценивании заданий будут учитываться: правильность, рациональность, полнота выполнения заданий. Задания должны быть оформлены в соответствии с общепринятыми требованиями.
Вариант 1
1. Каковы основные причины коррозии металлов?
2. Коррозия металлов с водородной деполяризацией.
3. Адсорбционные ингибиторы.
4. Подземный трубопровод подвергается наибольшей коррозии под влиянием «блуждающего тока». Объясните механизм коррозии. Предложите схему протекторной защиты трубопровода. Объясните принцип ее действия с точки зрения электрохимической защиты.
5. Рассчитайте коэффициент ингибирования ( 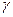 ) и защитное действие ингибитора (
) и защитное действие ингибитора ( 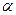 в%)-К3 [Fe(CN)6] для различных материалов
в%)-К3 [Fe(CN)6] для различных материалов
| Материал | Площадь образца, см2 | Ττ, ч | Изменение массы (m0-m1) образцов, г | Скорость коррозии в среде HCI+HNO3 | Коэффи-циент ингибиро-вания | Защитное действие ингибитора | |||
| До ингибирования | После ингибирования | Без ингибитора | С ингибитором |
| |||||
| Cт.3 | 19 | 1 | 0,3418 | 0,1632 |
| ||||
| 30Х13 | 15 | 1 | 0,0315 | 0,0474 |
| ||||
| 12Х18Н9 | 24 | 1 | 0,0098 | 0,0081 |
| ||||
| 12Х18Н10Т | 20 | 1 | 0,0090 | 0,0122 |
| ||||
Вариант 2
1 Объясните влияние хрома на коррозионную стойкость стали.
2 Какую информацию о коррозионном процессе можно извлечь из анодной поляризационной кривой?
3 Приведите кратко классификацию ингибиторов коррозии.
4 Трубы и котлы теплоэнергетических установок, в которых существует замкнутый водяной цикл, подвергаются электрохимической коррозии. Объясните механизм этого вида коррозии, роль кислорода в его протекании.
5 Определите показатель коррозии (Δm г / c м 2 ) при сплошной коррозии для различных марок сталей и рабочих сред с ингибиторами. Сделайте вывод о влиянии ингибитора на показатель коррозии.
| Марка стали | Площадь образцов, см2 | Коррозионная среда HNO3+HCI и ингибитор | Масса образца, г | Δm г/cм2 | |
| До испытаний | После испытаний | ||||
| Ст 3 | 20 | Мочевина | 46,9363 | 46,637 | |
| 40Х | 15 | Мочевина | 19,9313 | 19,856 | |
| 08Х18Н9 | 24 | Мочевина | 9,2485 | 9,2376 | |
| 0,4Х18Н10Т | 20 | Мочевина | 75,5532 | 75,542 | |
Вариант 3
1. Что такое коррозия под напряжением?
2. Что такое анодные и катодные покрытия? Приведите примеры.
3. Что такое скорость коррозии? Приведите примеры.
4. Паровой котел, поставленный на консервацию на длительное время, был продут воздухом с добавками ингибиторов. Объясните механизм коррозионного процесса в котле и роль ингибиторов в нем. Какие существуют ингибиторы с электрохимических позиций?
5. Определите показатель коррозии (Dm г / c м 2 ) при сплошной коррозии для заданных марок сталей и рабочих сред с окислителем.
| Марка стали | Площадь образцов, см2 | Коррозионная среда HNO3+HCI и окислитель | Масса образца, г | Dm, г/cм2 | |
| До испытаний | После испытаний | ||||
| Ст 3 | 20 | CrO3 | 48,3221 | 47,9864 | |
| 40Х | 15 | CrO3 | 21,5059 | 21,4926 | |
| 12Х18Н9 | 24 | CrO3 | 9,1442 | 9,1352 | |
| 12Х18Н10Т | 20 | CrO3 | 78,8062 | 78,7960 | |
Вариант 4
1.Что такое катодный и анодный процессы в явлениях электрохимической коррозии?
2.Какие металлы чаще всего используются в качестве протекторов для защиты конструкций из железа? Почему?
3.Как рассчитать глубинный показатель коррозии (Δh) в случае равномерной коррозии?
4.Крылья автомобиля изготавливаются из стали 08. Расшифруйте марку стали. Какому виду коррозии они подвергаются? Объясните ее механизм. Опишите технологию нанесения защитного покрытия.
6. Рассчитайте коэффициент ингибирования ( 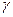 ) и защитное действие ингибитора (
) и защитное действие ингибитора ( 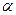 в%)-К4 [Fe(CN)6 ] для различных материалов
в%)-К4 [Fe(CN)6 ] для различных материалов
| Материал | Площадь образца, см2 | Ττ, ч | Изменение массы (m0-m1) образцов, г | Скорость коррозии в среде HCI+HNO3 | Коэффи-циент ингибиро-вания | Защитное действие ингибитора | |||
| До ингибирования | После ингибирования | Без ингибитора | С ингибитором |
| |||||
| Cт.3 | 20 | 1 | 0,2260 | 0,0970 |
| ||||
| Ст.3 | 15 | 1 | 0,8835 | 0,0155 |
| ||||
| 30Х13 | 24 | 1 | 0,1880 | 0,0162 |
| ||||
| 12Х18Н10Т | 20 | 1 | 0,0090 | 0,0107 |
| ||||
Вариант 5
1. Как происходит атмосферная коррозия (pH  7) луженого железа при нарушении покрытия?
7) луженого железа при нарушении покрытия?
2. Что такое ток коррозии?
3. Как рассчитать показатель изменения массы в случае газовой коррозии?
4. Для стальных свай морского сооружения применена протекторная защита от коррозии. Объясните механизм коррозии свай в морской воде и принцип протекторной защиты с электрохимических позиций.
5. Определите показатель коррозионной стойкости при сплошной коррозии (t1) – время проникновения на допустимую глубину, год, для изделий из заданной марки стали.
| Марка стали | ρ, г/см3 | Площадь образцов, см2 | Изменение размеров (l0-lk), образцов (допустимое), cм | Изменение массы образцов (m0-m1) в среде HNO3+HCl+KF.HF в (г) | Глубина проникновения коррозии (h), см | Линейная скорость (U1) коррозии, см/ч | Время проникновения на допустимую глубину, t1, год | |
| Через 1ч | Через 2 ч | |||||||
| Ст 3 | 7,8 | 20 | 0,5 | 0,3156 | 03140 | |||
| 40Х | 7,85 | 15 | 0,5 | 0,0356 | 0,7120 | |||
| 12Х18Н9 | 7,9 | 24 | 0,5 | 0,0086 | 0,0172 | |||
Вариант 6
1.В каких случаях используется катодная протекторная защита?
2.Раскройте понятие поляризация?
3.Какова классификация ингибиторов?
4.Вал из стали 14Х17Н2 работает в газовой среде при температуре 4000С. Какому виду коррозии он подвергается. Объясните ее механизм. Расшифруйте марку стали. Объясните влияние химического состава на коррозионную стойкость. Что такое скорость коррозии?
5. Определите показатель коррозии (Dm г / c м 2 ) при сплошной коррозии для различных марок сталей и различных рабочих сред
| Марка стали | Площадь образцов, см2 | Масса образца, г | Dm г/cм2 | ||
| До исследования | После коррозии | ||||
| В 5% растворе HNO3 | В 10% растворе HNO3 | ||||
| Ст 3 | 20 | 44,2840 43,5483 | 44,1925 - | - 43,3459 | |
| 40Х | 15 | 19,7762 19,7630 | 19,7630 - | - 19,7469 | |
| 12Х18Н9 | 20 | 8,9314 8,8757 | 8,9221 - | - 8,8677 | |
Вариант 7
1. Коррозия металлов с кислородной деполяризацией.
2. Металлические покрытия.
3. Что такое коэффициент ингибирования?
4. При построении американской яхты «Зов моря» для обшивки корпуса использовали листы из сплава монеля (Ni-27%; Cu – 2-3%; Mn – 1,2-1,8%), который обладает очень высокой коррозионной стойкостью. Листы обшивки соединили стальными заклепками. После испытательного рейса яхта была продана на металлолом, т.к листы обшивки отвалились от корпуса яхты. Объясните причину разрушения корпуса на основе теории электрохимической коррозии. (Приведите схему электрохимического процесса).
5. Рассчитайте коэффициент ингибирования ( 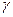 ) и защитное действие ингибитора –KF HF(
) и защитное действие ингибитора –KF HF( 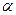 в%)- для различных материалов
в%)- для различных материалов
| Материал | Площадь образца, см2 | Ττ, ч | Изменение массы (m0-m1) образцов, г | Скорость коррозии в среде HCI+HNO3 | Коэффи-циент ингибиро-вания | Защитное действие ингибитора | |||
| До ингибирования | После ингибирования | Без нгибитора KF.HF | С ингибитором KF.HF |
| |||||
| 30Х13 | 15 | 1 | 0,1880 | 0,0356 |
| ||||
| 12Х18Н9 | 24 | 1 | 0,0090 | 0,0092 |
| ||||
| 12Х18Н10Т | 20 | 1 | 0,0089 | 0,0088 |
| ||||
Вариант 8
1.Сформулируйте отличие электрохимической коррозии от химической.
2.Какова роль продуктов коррозии в коррозионных процессах? Приведите примеры.
3.Какие существуют методы защиты от коррозии? Охарактеризуйте кратко сущность каждого из них.
4.Клапаны автомобильных и тракторных двигателей изготавливаются из стали 40Х10С2Н. В процессе работы они нагреваются до температуры 600°С. Какое влияние оказывает температура на процесс окисления? Каким уравнением выражается зависимость скорости газовой коррозии от температуры? Расшифруйте марку стали и укажите роль легирующих элементов на процесс коррозии.
5.Рассчитайте коэффициент ингибирования ( 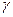 ) и защитное действие ингибитора (
) и защитное действие ингибитора ( 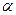 в%)-К4[Fe(CN)6] для различных материалов
в%)-К4[Fe(CN)6] для различных материалов
| Материал | Площадь образца, см2 | Ττ, ч | Изменение массы (m0-m1) образцов, г | Скорость коррозии в среде Na2 S2O8 | Коэффи-циент ингибиро-вания | Защитное действие ингибитора | |||
| До ингибирования | После ингибирования | Без ингибитора | С ингибитором |
| |||||
| СЧ-15 | 5 | 1 | 0,8935 | 0,4823 |
| ||||
| Ст.3 | 19 | 1 | 0,8835 | 0,8404 |
| ||||
| 30Х13 | 15 | 1 | 0,1880 | 0,1900 |
| ||||
Вариант 9
1.Что такое катодный и анодный процессы в явлениях электрохимической коррозии?
2.Что такое ингибиторы? В каких случаях они применяются?
3.Как происходит атмосферная коррозия оцинкованного железа при нарушении покрытия?
4.Крепежные детали делают при температуре 800°С. Какому виду коррозии они подвергаются? Какое влияние оказывает температура на процесс окисления. Из предложенных марок сталей (15Х и 12Х17) выберите сталь для изготовления деталей. Опишите влияние химического состава на коррозионную стойкость выбранной стали.
5. Рассчитайте коэффициент ингибирования ( 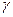 )и защитное действие ингибитора (
)и защитное действие ингибитора ( 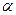 в%)-Na2C2O4-натрий щавелевокислый для различных материалов
в%)-Na2C2O4-натрий щавелевокислый для различных материалов
| Материал | Площадь образца, см2 | Ττ, ч | Изменение массы (m0-m1) образцов, г | Скорость коррозии в среде HCI+ HNO3 | Коэффи-циент ингибиро-вания | Защитное действие ингибитора | ||
| До до ингибирования | после ингибирования | Без ингибитора | С ингибитор.м | |||||
| Cт.3 | 20 | 1 | 0,2260 | 0,0303 | ||||
| 12Х13 | 15 | 1 | 0,0315 | 0,0160 | ||||
| 08Х18Н10 | 24 | 1 | 0,0090 | 0,0116 | ||||
| 0,4Х18Н10Т | 20 | 1 | 0,0090 | 0,0106 | ||||
Вариант 1 0
1. Охарактеризуйте изменение показателя коррозии при изменении содержания углерода в стали.
2. В каких случаях лучше всего использовать анодною защиту от коррозии?
3. Как определить толщину слоя покрытия расчетным и экспериментальным методом?
4. 25-тонная железнодорожная стальная цистерна наполнена соляной кислотой. Какому виду коррозии она подвергается ? Объясните ее механизм. В кислоту добавили ингибитор. Укажите его влияние на процесс коррозии. Что такое коэффициент игибирования и величена защитного ингибирования?
5. Определите показатель коррозионной стойкости при сплошной коррозии (t1) – время проникновения на допустимую глубину, год, для изделий из заданной марки стали.
| Марка стали | ρ, г/см3 | Площадь образцов, см2 | Изменение размеров (l0-lk), образцов (допустимое), cм | Изменение массы образцов (m0-m1) в среде HNO3+HCl+Cu(NО3)2 в (г) во времени | Глубина проникновения коррозии (h), см | Линейная скорость (U1) коррозии, см/ч | Время проникновения на допустимую глубину, t1, год | |
| Через 0,25ч | Через 0,5ч | |||||||
| Ст 3 | 7,8 | 20 | 0,5 | 0,1361 | 0,2720 | |||
| 0,8Х13 | 8,2 | 15 | 0,5 | 0,0093 | 0,1860 | |||
| 12Х18Н9 | 9,8 | 24 | 0,5 | 0,0060 | 0,0100 | |||
Вариант 11
1.Механизм защиты от коррозии лакокрасочными покрытиями.
2.Факторы, влияющие на характер газовой коррозии.
3.Законы роста оксидных пленок.
4.Болты из стали 1 работают при температуре 500°С. Какой коррозии они подвергаются. Для защиты болтов от окисления использовано хромирование. Объясните, что это за способ и механизм защиты болтов хромом.
5.Определите показатель коррозионной стойкости при сплошной коррозии (t m) – время уменьшения массы на единицу площади на допустимую заданную величину, год, для изделий из заданной марки стали.
| Марка стали | Площадь образцов, см2 | Допустимая Dm, г/см2 | Изменение массы образцов (m0-m1) в (г), в среде HCl+HNO3+Cu(NО3)2 | Скорость убыли массы, Um, г/см2.ч | Время τm уменьшения массы на единицу площади на допустимую Dm, год | |
| Через 0,25ч | Через 0,5ч | |||||
| Ст 3 | 20 | 2,34 | 0,1361 | 0,2720 | ||
| 30Х13 | 15 | 4,1 | 0,0093 | 0,1860 | ||
| 0,8Х18Н10 | 24 | 4,9 | 0,0060 | 0,0100 | ||
Вариант 12
1.Раскройте механизм роста оксидных пленок.
2.Что такое «пассивация»?
3.Укажите технологические факторы, обеспечивающие защиту металлоконструкций от коррозии.
4.Шестерня из стали 09Х17Н3СЛ работает при температуре 700°С в газовой среде. Какому виду коррозии она подвергается? Объясните ее механизм. Расшифруйте марку стали. Объясните влияние химического состава на жаростойкость стали. Каким уравнением выражается зависимость скорости газовой коррозии от температуры?
5. Определите показатель коррозионной стойкости при сплошной коррозии (tm) – время уменьшения массы на единицу площади на допустимую заданную величину, год, для изделий из разных марок стали.
| Марка стали | Площадь образцов, см2 | Допустимая потеря массы на единице площади, Dm, г/см2 | Изменение массы образцов (m0-m1) в (г), в среде HNO3+HCl | Скорость убыли массы,(Um), г/см2*ч | tm, год | |
| Через 0,25ч Без ингиб | Через 0,25ч С ингиб К4(Fe(CN)6) | |||||
| Ст 3 | 20 | 2,34 | 0,2260 | 0,0970 | ||
| 40 Х | 15 | 4,1 | 0,0315 | 0,0155 | ||
| 12Х18Н9 | 24 | 4,9 | 0,0098 | 0,0162 | ||
| 12Х18Н10Т | 20 | 5,0 | 0,0090 | 0,0107 | ||
Вариант 13
1.Что такое ингибиторная защита.
2.Раскройте понятие «деполяризация».
3.Приведите кратко классификацию коррозионных процессов.
4.Барабан стиральной машины, выполненный из стали 12Х18Н9, разорвался на участке сварного шва через несколько часов эксплуатации. После ремонта шов разрушился вновь. Металлографическими исследованиями установлена межкристаллитная коррозия (МКК) на участке нагрева металла в зоне шва. Объясните механизм коррозии, ее причины. Какой легирующий элемент следует добавить в сталь с целью повышения устойчивости к МКК.
5.Определите показатель коррозионной стойкости при сплошной коррозии (t1) – время проникновения на допустимую глубину, год, для изделий из заданной марки стали.
| Марка стали | ρ, г/см3 | Площадь образцов, см2 | Изменение размеров (l0-lk), образцов (допустимое), cм | Изменение массы образцов (m0-m1) в среде HNO3+HCl+CuSO4 в (г) | Глубина проникновения коррозии (h), см | Линейная скорость (U1) коррозии, см/ч | Время проникновения на допустимую глубину, t1, год | |
| Через 1ч | Через 2 ч | |||||||
| Ст 3 | 7,85 | 20 | 0,5 | 0,1753 | 03306 | |||
| 0,8Х13 | 7,76 | 15 | 0,5 | 0,0157 | 0,0164 | |||
| 12Х18Н9 | 7,9 | 24 | 0,5 | 0,0092 | 0,0090 | |||
Вариант 1 4
1.Сформулируйте отличие электрохимической коррозии от химической.
2.Какова роль продуктов коррозии в коррозионных процессах? Приведите примеры.
3. Какие существуют методы защиты от коррозии? Охарактеризуйте кратко сущность каждого из них.
4. Клапаны автомобильных и тракторных двигателей изготавливаются из стали 40Х10С2М. В процессе работы они нагреваются до температуры 600С. Какое влияние оказывает температура на процесс окисления? Каким уравнением выражается зависимость скорости газовой коррозии от температуры? Расшифруйте марку стали и укажите роль легирующих элементов на процесс коррозии.
5. Рассчитайте скорость убыли массы (Um) и глубину (h) проникновения коррозии для заданных марок стали.
| Марка стали | Площадь образцов, см2 | Изменение массы образцов (m0-m1) в среде HNO3+HCl+CuSO4 во времени, ч | ||
| Через 0,25ч | Через 0,5ч | Через 1ч | ||
| Ст 3 | 20 | 0,1361 | 0,2720 | 0,2849 |
| 12Х13 | 15 | 0,0093 | 0,186 | 0,188 |
| 12Х21Н5Т | 24 | 0,0060 | 0,0086 | 0,0090 |
Принять rст .3.=7,85 г/cм3, r20Х13 =7,67 г/cм3, r12Х21Н5Т =7,7 г/cм3
Вариант 15
1..Что такое катодный и анодный процессы в явлениях электрохимической коррозии?
2.Что такое ингибиторы? В каких случаях они применяются?
3.Как происходит атмосферная коррозия (рН=7) оцинкованного железа при нарушении покрытия?
4.Крепежные детали работают при температуре 800 С. Какому виду коррозии они подвергаются? Какое влияние оказывает температура на процесс окисления? Из предложенных марок сталей (15Х и 12Х17) выберите сталь для изготовления деталей. Опишите влияние химического состава на коррозионную стойкость выбранной стали.
5.Определите показатель коррозионной стойкости при сплошной коррозии (tm) – время уменьшения массы на единицу площади на допустимую заданную величину, год, для изделий из разных марок стали.
| Марка стали | Площадь образцов, см2 | Допустимая потеря массы на единице площади, Dm, г/см2 | Изменение массы образцов (m0-m1) в (г), в среде HNO3+HCl | Скорость убыли массы,(Um), г/см2*ч | tm, год | |
| Через 0,25ч без ингиб | Через 0,25ч с ингиб К3(Fe(CN)6) | |||||
| Ст 3 | 20 | 2,34 | 0,2260 | 0,2160 | ||
| 40 Х | 15 | 4,1 | 0,0315 | 0,0375 | ||
| 12Х18Н9 | 24 | 4,9 | 0,0098 | 0,0081 | ||
| 12Х18Н10Т | 20 | 5,0 | 0,0090 | 0,00122 | ||
Вариант 16
1. Что такое коррозия металлов? Охарактеризуйте зависимость скорости химической коррозии:
а) от температуры нагрева и времени выдержки образца в агрессивной среде,
б) химического состава газовой среды, давления и скорости движения газов.Предложите принципы выбора жаропрочных материалов для работы в коррозионных средах.
3.Антикоррозионные покрытия, методы их нанесения.
4.Клапаны моторов нагреваются до температуры 8000С. Какому виду коррозии они подвергаются? Объясните ее механизм. Для изготовления клапанов назначается сталь 10Х13СЮ. Расшифруйте марку стали и объясните влияние химического состава на процесс газовой коррозии. Как влияет характер обработки поверхности на скорость окисления?
5.Рассчитайте скорость убыли массы (Vm) для заданных марок сталей и рабочих сред. Сделайте вывод о влиянии концентрации нитратной (HNO3) кислоты и химического состава стали на скорость коррозии.
| Марка стали | Площадь образцов, см2 | Изменение массы (m0-m1) образцов в различных растворах HNO3 в течении 1 ч | ||
| 0,5% HNO3(рН=2,4) | 1% HNO3 (рН=2,20) | 2% HNO3 (рН=2,0) | ||
| Ст 3 | 20 | 0,0913 | 0,2050 | 0,3418 |
| 12Х13 | 15 | 0,0130 | 0,0163 | 0,0236 |
Вариант 17 
1. Каков механизм электрохимической коррозии? Что такое контактная коррозия?
2.Подводная часть стального корпуса судна защищается от коррозии протектором, изготовленным из цинка. На чем основана эта защита? Ответ мотивируйте
3.Что такое оксидирование, воронение?
4.Винты из стали 18Х12ВМБФР подвергают газовой коррозии при 750оС. Объясните механизм коррозии. Назовите важнейшие факторы, влияющие на газовую коррозию. Охарактеризуйте влияние хрома на скорость окисления.
5. Рассчитайте скорость убыли массы (Um) и глубину (h) проникновения коррозии для заданных марок стали.
| Марка стали | Площадь образцов, см2 | Изменение массы образцов (m0-m1) в среде HNO3+HCl+CuSO4 во времени, ч | ||
| Через 0,25ч | Через 0,5ч | Через 1ч | ||
| Ст 3 | 20 | 0,1361 | 0,2720 | 0,2849 |
| 12Х13 | 15 | 0,0093 | 0,186 | 0,188 |
| 12Х21Н5Т | 24 | 0,0060 | 0,0086 | 0,0090 |
Принять rст .3.=7,85 г/cм3, r12Х13 =7,72 г/cм3, r12Х21Н5Т =7,9 г/cм3
Вариант 18
1.Особенности коррозии металлов в условиях возникновения пассивности. В каких производственных операциях можно использовать пассивируемость металлов и сплавов в борьбе с коррозией.
2. Чем отличается коррозия железа в кислой среде от коррозии в нейтральной среде?
3. Что такое анодные и катодные покрытия? Приведите примеры.
4.Сварные сосуды для работы в разбавленных растворах нитратной кислоты (НNOз) изготовлены из стали 12Х18Н9. Через определенное время в них обнаружена межкристаллитная коррозия. Объясните, что такое межкристаллитная коррозия и меры борьбы с ней
5. Определите показатель коррозионной стойкости при сплошной коррозии (t m) – время уменьшения массы на единицу площади на допустимую заданную величину, год, для изделий из заданной марки стали.
| Марка стали | Площадь образцов, см2 | Допустимая Dm, г/см2 | Изменение массы образцов (m0-m1) в (г), в среде HCl+HNO3 | Скорость убыли массы, Um, г/см2.ч | Время τm уменьшения массы на единицу площади на допустимую Dm, год | |
| Через 0,25ч без ингибитора | Через 0,25ч с ингибитором К4 | Fe(CN)6 ] | |||||
| Ст 3 | 20 | 2,34 | 0,2260 | 0,0970 | ||
| 30Х13 | 15 | 4,1 | 0,0315 | 0,0155 | ||
| 0,8Х18Н10Т | 24 | 4,9 | 0,0090 | 0,0107 | ||
Вариант 19
1.Раскройте понятие «пассивация» и «депассивация».
2. Укажите наиболее широко применяемые лакокрасочные покрытия.
3. Охарактеризуйте влияние легирующих элементов на скорость окисления.
4.В магистральном трубопроводе образовались трещины с внутренней стороны стенки трубы в напряженной зоне при сварке. Какой вид коррозии произошел? Объясните ее механизм. Какие факторы влияют на этот вид коррозии? Предложите мероприятия, уменьшающие ее.
5.Рассчитайте скорость убыли массы (Vm) для заданных марок сталей и рабочих сред. Сделайте вывод о влиянии концентрации нитратной (HNO3) кислоты и химического состава стали на скорость коррозии.
| Марка стали | Площадь образцов, см2 | Изменение массы (m0-m1) образцов в различных растворах HNO3 в течении 1 ч | ||
| 0,5% HNO3(рН=2,4) | 1% HNO3 (рН=2,20) | 2% HNO3 (рН=2,0) | ||
| Ст 3 | 20 | 0,0913 | 0,2050 | 0,3418 |
| 12Х13 | 15 | 0,0130 | 0,0163 | 0,0236 |
Вариант 20
1.Кинетика химической коррозии металлов.
2. Раскройте механизм точечной коррозии.
3. Каковы электрохимические процессы, происходящие при нанесении металлических покрытий.
4.Одной из важнейших проблем в области добычи нефти в море является долговечность создаваемых стальных сооружений. Какому виду коррозии подвергаются сооружения? Объясните ее механизм. В чем заключается катодная защита, которую широко применяют для защиты металлов в морской воде
5.Определите показатель коррозионной стойкости при сплошной коррозии (t m) – время уменьшения массы на единицу площади на допустимую заданную величину, год, для изделий из заданной марки стали.
| Марка стали | Площадь образцов, см2 | Допустимая Dm, г/см2 | Изменение массы образцов (m0-m1) в (г), в среде HCl+HNO3+FeCI3 | Скорость убыли массы, Um, г/см2.ч | Время τm уменьшения массы на единицу площади на допустимую Dm, год | |
| Через 0,25ч | Через 0,5ч | |||||
| Ст 3 | 20 | 2,34 | 0,1361 | 0,2689 | ||
| 30Х13 | 15 | 4,1 | 0,0093 | 0,0395 | ||
| 0,8Х18Н10 | 24 | 4,9 | 0,0060 | 0,0113 | ||
Вариант 2 1
1.Протекторы, механизм их действия.
2. Основные причины коррозии металлов
3.Химическая коррозия и ее разновидность- жидкостная коррозия.
4.На Северодонецком химкомбинате «Азот» разработали жидкое азотное удобрение, которое имеет очень высокую коррозионную активность. Цистерны с удобрением корродируют со скоростью 2-3 мм в год. Применение анодной защиты снизило скорость коррозии в 6 тыс. раз, 2 до 0,0003 мм в год. Какому виду коррозии подвергаются цистерны? Объясните ее механизм. В чем заключается анодная защита?
5.Определите глубину (h) проникновения коррозии и скорость убыли массы (Um) образцов в течении 1 часа при сплошной коррозии для заданных марок сталей и рабочих сред. Сделайте вывод о влиянии концентрации HCl и химического состава на скорость коррозии.
|
Марка стали |
Площадь образцов, см2 |
Коррозионная среда, | Масса образца, г | Скорость убыли массы Um, г/см2.ч | |
| До испытаний | После испытаний | ||||
| Ст 3 r=7,85 г/cм3 r=7,85г/cм3 r=7,85 г/cм3 | 20 20 20 | 0,5% HCl 1% HCl 2% HCl | 43,5122 43,5028 43,4728 | 43,4822 43,4728 43,4428 | |
| 12Х13 r=7,72 г/cм3 r=7,72 г/cм3 r=7,72 г/cм3 | 15 15 15 | 0,5% HCl 1% HCI 2% HCI | 18,4774 18,4536 20,2814 | 18,4536 18,4036 20,2177 | |
.
Вариант 22
1.Коррозия металлов с кислородной деполяризацией.
2. Металлические покрытия.
3. Что такое коэффициент ингибирования?
4. При построении американской яхты «Зов моря» для обшивки корпуса использовали листы монеля ( Ni -27-29 , Cи-2-3%, Mn-1,2-1,8%), который обладает очень высокой коррозионной стойкостью. Листы обшивки соединили стальными заклепками. После испытательного рейса яхта была продана на металлолом, листы обшивки отвалились от корпуса яхты. Объясните причину разрушения корпуса на основе теории электролитической коррозии. Приведите схему электролитического процесса
5. Определите глубину (h) проникновения коррозии и скорость убыли массы (Um) образцов в течении 1 часа при сплошной коррозии для заданных марок сталей и рабочих сред. Сделайте вывод о влиянии концентрации H2SO4 и химического состава на скорость коррозии.
Марка стали | Площадь образцов, см2 | Коррозионная среда, | Масса образца, г | Скорость убыли массы Um, г/cм2 ч | Глубина проникновения (h), см | ||
| До испытания | После испытаний | ||||||
|
| |||||||
| Ст 3 r=7,85г/cм3 r=7,85г/cм3 | 20 20 | 1% 2SO4 2% 2SO4 | 43,9577 42,9121 | 43,9150 42,8742 |
| ||
| 0,8Х13 r=7.7г/cм3 r=7.7г/cм3 | 15 15 | 1% 2SO4 2% 2SO4 | 19,6020 18,9040 | 19,4265 18,7055 |
| ||
| 12Х18Н9 r=7,9г/cм3 r=7,9г/cм3 | 24 24 | 1%H2SO4 2%H2SO4 | 8,8961 8,9660 | 8,8855 8,9547 |
| ||
Вариант 23
1.Что такое коррозия под напряжением?
2. Что такое анодные и катодные покрытия? Приведите примеры
3. Что такое скорость коррозии? Приведите примеры
4 Паровой котел, поставленный на консервацию на длительное время был продут воздухом с добавками ингибиторов. Объясните механизм коррозионного процесса. В котле и роль ингибиторов в нем. Какие существуют ингибиторы с электрохимических позиций?
5. Определите глубину (h) проникновения коррозии и скорость убыли массы (Um) образцов в течение 1 часа при сплошной коррозии для заданных марок сталей и рабочих сред. Сделайте вывод о влиянии концентрации H3PO4 и химического состава на скорость коррозии.
| Марка стали | Площадь образцов, см2 | Коррозионная среда, %,(рН) | Масса образца, г | Скорость убыли массы Um, г/см2.ч | Глубина проникновения (h), см | |
| До испытания | После испытания | |||||
| Ст 3 r=7,8 /cм3 r=7,8 /cм3 | 20 20 | 1% 3PO4 2%H3PO4 | 43,2717 42,5626 | 43,2364 42,5321 | ||
| Cт 30Х13 r=7.67 г/cм3 r=7.67 г/cм3 | 15 15 | 1%Н3PO4 2%H3PO4 | 19,2817 18,2649 | 19,2649 18,2551 | ||
Вариант 24
1.В чем особенность коррозии в растворах неэлектролитов? Приведите примеры.
2. Подводная часть стального корпуса защищается от коррозии протектором, изготовленным из цинка. На чем основана эта защита? Ответ мотивируйте.
3.Крыша дома покрыта листами. Какому виду коррозии она подвергается?
4..Что такое биокоррозия. Приведите примеры. Объясните ее механизм. Предложите методы защиты крыши от коррозии, дайте их обоснование и характеристику.
5.Определите показатель коррозионной стойкости при сплошной коррозии (t m) – время уменьшения массы на единицу площади на допустимую заданную величину, год, для изделий из заданной марки стали.
| Марка стали | Площадь образцов, см2 | Допустимая Dm, г/см2 | Изменение массы образцов (m0-m1) в (г), в среде НNO3 | Скорость убыли массы, Um, г/см2.ч | Время τm уменьшения массы на единицу площади на допустимую Dm, год | |
| Через 15 мин | Через 30 мин | |||||
| Ст 3 | 20 | 2,34 | 0,1709 | 0,3418 | ||
| 30Х13 | 15 | 4,1 | 0,0125 | 0,0230 | ||
| 0,8Х18Н10 | 24 | 4,9 | 0,0093 | 0,01860 | ||
Вариант 25
1.Какие виды коррозии под механическим напряжением Вы знаете? Приведите примеры.
2.Что такое дренажная защита?
3. Какими показателями пользуются для оценки коррозии? Приведите расчетные формулы.
4.Для изготовления консервных банок применяют жесть. Какому виду коррозии она подвергается? Объясните ее механизм. Для повышения коррозионной стойкости жести используется лужение. Что это за метод? Опишите механизм защиты жести нанесенным покрытием.
5.Определите показатель коррозионной стойкости при сплошной коррозии (t1) – время проникновения на допустимую глубину, год, для изделий из заданной марки стали.
| Марка стали | ρ, г/см3 | Площадь образцов, см2 | Изменение размеров (l0-lk), образцов (допустимое), cм | Изменение массы образцов (m0-m1) в среде H2О в (г) при 600С | Глубина проникновения коррозии (h), см | Линейная скорость (U1) коррозии, см/ч | Время проникновения на допустимую глубину, t1, год | |
| Через 1 ч | Через 2 ч | |||||||
| Ст 3 | 7,8 | 20 | 0,5 | 0,090 | 0,109 | |||
| 12Х13 | 8,2 | 15 | 0,5 | 0,075 | 0,077 | |||
| 12Х21Н5Т | 9,8 | 24 | 0,5 | 0,033 | 0,045 | |||
Вариант 26
1.Что такое газовая коррозия? Приведите примеры.
2. Что такое анодная поляризационная кривая?
3. Какое влияние оказывает структура стали на скорость коррозии в случае деформации?
4.Цинковые покрытия широко применяются для защиты от коррозии стальных емкостей, содержащих бензин. Опишите метод электролитического цинкования стали (приведите схему установки). Объясните механизм защиты стали цинковым покрытием.
5.Определите показатель коррозионной стойкости при сплошной коррозии (t1) – время проникновения на допустимую глубину, год, для изделий из заданной марки стали.
| Марка стали | Ρ, г/см3 | Площадь образцов, см2 | изменение размеров (l0-lk), образцов, допустимое,cм | Изменение массы образцов (m0-m1) в среде HNO3 в (г) | Глубина проникновения коррозии (h), см | Линейная скорость (U1) коррозии, см/ч | Время проникновения на допустимую глубину, t1, год | |
| Через 0,25ч | Через 0,5ч | |||||||
| Ст 3 | 7,85 | 20 | 0,5 | 0,1753 | 03306 | |||
| 0,8Х13 | 7,76 | 15 | 0,5 | 0,0157 | 0,0164 | |||
| 12Х18Н9 | 7,9 | 24 | 0,5 | 0,0092 | 0,0090 | |||
Вариант 27
1. Что такое электрохимическая коррозия?
2. Что такое оксидирование, воронение?
3. Что такое ингибиторы? В каких случаях они применяются?
4. Какому виду коррозии подвергается форма моста, изготовленная из стали. Объясните ее механизм. Предложите методы защиты от коррозии, дайте их обоснование и характеристику.
5. Определите показатель коррозии (Δm) г/см2 при сплошной коррозии для заданных марок сталей и различных рабочих сред и активаторов-хлорид ионов. Сделайте вывод о влиянии активатора.
| Марка стали | Площадь образцов, см2 | Коррозионная среда и активатор | Масса образца, г | Δm, г/см2.ч | |
| До испытания | После испытания | ||||
| Ст 3 | 20 | 1% HNO3 1% HNO3 1%HNO3 | 44,1925 43,1125 42,8763 | 43,9936 42,8763 42,5912 | |
| 12Х13 | 15 | 1%HNO3 1% HNO3 1% HNO3 | 19,3605 18,8822 18,8282 | 19,3324 18,8282 18,6839 | |
Вариант 2 8
1. Чем отличается коррозия железа в кислой среде от коррозии в нейтральной среде?
2. Приведите классификацию коррозионных процессов в виде схем.
3. Особенность ингибиторной защиты.
4. Детали термических печей с рабочей температурой 900-1000С изготовлены из стали 20Х20Н14С2. Какому виду коррозии они подвергаются? Объясните ее механизм. Расшифруйте марку стали и объясните влияние химического состава на межкристаллитную стойкость. Какими параметрами пользуются для оценки газовой коррозии?
5. Определите показатель коррозии (Δm) г/см2 при сплошной коррозии для заданной стали и рабочих сред с различными ингибиторами, Сделайте вывод о влиянии ингибитора на показатель коррозии
| Марка стали | Площадь образцов, см2 | Коррозионная среда и ингибитор | Масса образца, г | Δm, г/см2.ч | |
| До испытания | После испытания | ||||
| Ст 3 | 20 | HNO3+HCI+K3|Fe(CN)6| HNO3+HCI+Na2C2O4 HNO3+HCI+K4[Fe(CN)6] | 48,7159 48,4586 48,8134 | 48,5450 48,4280 48,7159 | |
| 12Х13 | 15 | HNO3+HCI+K3|Fe(CN)6| HNO3+HCI+Na2C2O4 HNO3+HCI+K4[Fe(CN)6] | 20,3219 20,3590 21,6058 | 20,2727 20,3425 21,5892 | |
Указания к решению задач
Определение основных показателей коррозии и коррозионной стойкости при сплошной коррозии металлов и сплавов проводится в соответствии с ГОСТ 9.908-852 «Единая система защиты от коррозии и старения. Металлы и сплавы. Методы определения показателей коррозии и коррозионной стойкости»
Некоторые количественные показатели коррозии и коррозионной стойкости приведены в таблице 1
Таблица 1
Дата добавления: 2021-06-02; просмотров: 69; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!
